Séroquel
Les Informations Présentées Sur Ce Site Ne Constituent Pas Un Avis Médical. Nous Ne Vendons Rien. L'Exactitude De La Traduction N'Est Pas Garantie. Clause De Non-Responsabilité
Résumé
Qu'est-ce que Seroquel?
Seroquel est un médicament sur ordonnance utilisé pour traiter les symptômes de la manie du trouble bipolaire de la schizophrénie I; Épisodes dépressifs du trouble bipolaire; Entretien du trouble bipolaire I; et un trouble dépressif majeur. Seroquel peut être utilisé seul ou avec d'autres médicaments.
Seroquel belongs to a class of drugs called Antipsychotics 2nd Generation; Antimanic Agents.
On ne sait pas si Seroquel est sûr et efficace chez les enfants de moins de 12 ans.
Quels sont les effets secondaires possibles de Seroquel?
Séroquel
Quel type de médicament est des barbituriques
- Mouvements musculaires incontrôlés dans votre visage (mâcher des lèvres fronçant le mouvement de la langue clignotant ou mouvement des yeux)
- Apparence de masque du visage
- Problème avalé
- Problèmes de discours
- étourdissement
- constipation sévère
- Urinée douloureuse ou difficile
- vision floue
- vision du tunnel
- douleurs oculaires
- voir des halos autour des lumières
- muscles très raides (rigides)
- forte fièvre
- transpiration
- confusion
- Roigments cardiaques rapides ou inégaux
- tremblements
- évanouissement
- augmentation de la soif
- Augmentation de la miction
- bouche sèche
- odeur de respiration fruitée
- fièvre
- frissons
- plaies de la bouche
- plaies de la peau
- mal de gorge
- tousser et
- difficulté à respirer
Obtenez de l'aide médicale immédiatement si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires les plus courants de Seroquel comprennent:
- problèmes de parole
- vertiges
- somnolence
- fatigue
- manque d'énergie
- battements cardiaques rapides
- nez encombré
- appétit accru
- prise de poids
- estomac renversé
- vomissement
- constipation
- bouche sèche et
- test de fonction hépatique anormale
Dites au médecin si vous avez un effet secondaire qui vous dérange ou qui ne disparaît pas.
Ce ne sont pas tous les effets secondaires possibles de Seroquel. Pour plus d'informations, demandez à votre médecin ou à votre pharmacien.
Appelez votre médecin pour des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
Dosage pour sérocoul
Adultes plus âgés avec démence Peut avoir un risque légèrement accru de décès lors de la prise de Seroquel. Les préparatifs de dosage sont de 25 50 100 200 300 et 400 mg de comprimés.
Quelles substances ou suppléments de médicaments interagissent avec Seroquel?
Seroquel peut interagir avec un certain nombre d'autres médicaments, mais sans s'y limiter antidépresseur médicaments antifongiques médicaments stéroïdes cimétidine ( Tagamet ) thioridazine ( Melaire ) et le lorazépam ( Ativan ).
Seroquel pendant la grossesse et l'allaitement
Pendant la grossesse, ce médicament ne doit être utilisé que lorsqu'il est clairement nécessaire. Discutez des risques et des avantages avec votre médecin. Seroquel passe dans le lait maternel et peut avoir des effets indésirables sur un nourrisson infirmier. L'allaitement maternel lors de la prise de Seroquel n'est pas recommandé.
Informations Complémentaires
Notre centre de médicaments sur les effets secondaires de Seroquel offre une vue complète des informations sur les médicaments disponibles sur les effets secondaires potentiels lors de la prise de ce médicament.
Informations sur les médicaments de la FDA
- Description de la drogue
- Indications
- Dosage
- Effets secondaires
- Interactions médicamenteuses
- Avertissements
- Surdosage
- Pharmacologie clinique
- Guide des médicaments
AVERTISSEMENT
Accrue de la mortalité chez les patients âgés atteints de psychose liée à la démence; et pensées et comportements suicidaires
Accrue de la mortalité chez les patients âgés atteints de psychose liée à la démence
Les patients âgés atteints de psychose liée à la démence traitée avec des antipsychotiques sont à un risque accru de décès [voir avertissements et PRÉCAUTIONS ]. Seroquel n'est pas approuvé pour le traitement des patients atteints de psychose liée à la démence [voir avertissements et PRÉCAUTIONS ].
Pensées et comportements suicidaires
Les antidépresseurs ont augmenté le risque de pensées suicidaires et de comportement chez les enfants adolescents et jeunes adultes dans des études à court terme. Ces études n'ont pas montré une augmentation du risque de pensées suicidaires et de comportement avec une utilisation d'antidépresseurs chez les patients de plus de 24 ans; Il y a eu une réduction du risque avec l'utilisation d'antidépresseurs chez les patients âgés de 65 ans et plus [voir avertissements et PRÉCAUTIONS ].
Chez les patients de tous âges, qui sont lancés sur un traitement antidépresseur, surveillent étroitement pour l'aggravation et pour l'émergence de pensées et de comportements suicidaires. Conseiller les familles et les soignants de la nécessité d'une observation et d'une communication étroites avec le prescripteur [voir avertissements et PRÉCAUTIONS ].
Seroquel n'est pas approuvé pour une utilisation chez les patients pédiatriques de moins de dix ans [voir Utiliser dans des populations spécifiques ].
Description de Seroquel
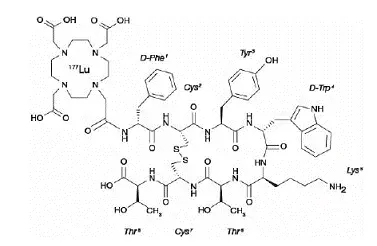
SEROQUEL® (quetiapine fumarate) is a psychotropic agent belonging to a chemical class the dibenzothiazepine derivatives. The chemical designation is 2-[2-(4-dibenzo [bf] [14]thiazepin-11-yl-1-piperazinyl)ethoxy]-ethanol fumarate (2:1) (salt). It is present in tablets as the fumarate salt. All doses and tablet strengths are expressed as milligrams of base not as fumarate salt. Its molecular formula is C42H50N6O4S2• C.4H4O4 et il a un poids moléculaire de 883.11 (sel de fumarate). La formule structurelle est:
 |
Le fumarate de quétiapine est une poudre cristalline blanche à blanc cassé qui est modérément soluble dans l'eau.
Seroquel est fourni pour l'administration orale à 25 mg (pêche ronde) 50 mg (blanc rond) 100 mg (jaune rond) 200 mg (blanc rond) 300 mg (blanc en forme de capsule) et 400 mg (jaune en forme de capsule).
Les ingrédients inactifs sont la povidone dibasic dicalcium phosphate dihydrate microcristalline cellulose glycolate de sodium glycolate lactose monohydrate de magnésium stéarate hypromellose polyéthylène glycol et dioxyde de titane.
Les comprimés de 25 mg contiennent de l'oxyde ferrique rouge et de l'oxyde ferrique jaune et les comprimés de 100 mg et 400 mg ne contiennent que de l'oxyde ferrique jaune.
Utilisations pour Seroquel
Schizophrénie
Seroquel est indiqué pour le traitement de la schizophrénie. L'efficacité de Seroquel dans la schizophrénie a été établie dans trois essais de 6 semaines chez les adultes et un essai de 6 semaines chez les adolescents (13-17 ans). L'efficacité de Seroquel pour le traitement d'entretien de la schizophrénie n'a pas été systématiquement évaluée dans des essais cliniques contrôlés [voir Études cliniques ].
Trouble bipolaire
Seroquel est indiqué pour le traitement aigu des épisodes maniaques associés au trouble bipolaire I à la fois en monothérapie et en complément du lithium ou du divalproex. L'efficacité a été établie dans deux essais de monothérapie de 12 semaines chez l'adulte dans un essai complémentaire de 3 semaines chez l'adulte et dans un essai de monothérapie de 3 semaines chez les patients pédiatriques (10-17 ans) [voir Études cliniques ].
Séroquel est indiqué comme une monothérapie pour le traitement aigu des épisodes dépressifs associés au trouble bipolaire. L'efficacité a été établie dans deux essais de monothérapie de 8 semaines chez les patients adultes souffrant de trouble bipolaire I et bipolaire II [voir Études cliniques ].
Seroquel est indiqué pour le traitement d'entretien du trouble bipolaire I en complément du lithium ou du divalproex. L'efficacité a été établie dans deux essais de maintenance chez les adultes. L'efficacité de la sérocoul comme monothérapie pour le traitement d'entretien du trouble bipolaire n'a pas été systématiquement évaluée dans des essais cliniques contrôlés [voir Études cliniques ].
Considérations spéciales dans le traitement de la schizophrénie pédiatrique et du trouble bipolaire I
La schizophrénie pédiatrique et le trouble bipolaire I sont de graves troubles mentaux, mais le diagnostic peut être difficile. Pour la schizophrénie pédiatrique, les profils des symptômes peuvent être variables et pour les troubles bipolaires I peuvent avoir des schémas variables de périodicité de symptômes maniaques ou mixtes. Il est recommandé que la thérapie médicamenteuse pour la schizophrénie pédiatrique et le trouble bipolaire I soit initiée uniquement après qu'une évaluation diagnostique approfondie ait été réalisée et qu'il ait soigné les risques associés au traitement des médicaments. Le traitement des médicaments pour la schizophrénie pédiatrique et le trouble bipolaire I est indiqué dans le cadre d'un programme de traitement total qui comprend souvent des interventions éducatives psychologiques et sociales.
Dosage pour sérocoul
Instructions d'administration importantes
Seroquel peut être pris avec ou sans nourriture.
Dosage recommandé
La plage de dose de titrage de dose initiale recommandée et la dose de séroquette maximale pour chaque indication approuvée sont affichées dans le tableau 1. Après que les ajustements de dosage initiaux peuvent être faits vers le haut ou vers le bas si nécessaire en fonction de la réponse clinique et de la tolérabilité du patient [voir Études cliniques ].
Tableau 1: Dosage recommandé pour Seroquel
| Indication | Dose initiale et titration | Dose recommandée | Dose maximale |
| Schizophrénie - Adultes | Jour 1: 25 mg deux fois par jour. L'augmentation des incréments de 25 mg-50 mg a divisé deux ou trois fois les jours 2 et 3 à une plage de 300 à 400 mg au jour 4. D'autres ajustements peuvent être effectués par incréments de 25 à 50 mg deux fois par jour par intervalles d'au moins 2 jours. | 150-750 mg / jour | 750 mg / jour |
| Schizophrénie - Adolescents (13-17 years) | Jour 1: 25 mg deux fois par jour. Jour 2: Dossage deux fois par jour totalisant 100 mg. Jour 3: Dossage deux fois par jour totalisant 200 mg. Jour 4: Dossage deux fois par jour totalisant 300 mg. Jour 5: Dossage deux fois par jour totalisant 400 mg. D'autres ajustements ne doivent pas être dans des incréments ne sont pas supérieurs à 100 mg / jour dans la plage de dose recommandée de 400 à 800 mg / jour. Sur la base de la réponse et de la tolérabilité, peut être administrée trois fois par jour. | 400-800 mg / jour | 800 mg / jour |
| Schizophrénie - EntretienBipolaire Manie - Adultes Monothérapie or as an adjunct to lithium or divalproex | Non applicable. Jour 1: Dossage de deux fois par jour totalisant 100 mg.Day 2: Dostotaling de deux fois par jour 200 mg. Jour 3: Dossage deux fois par jour totalisant 300 mg. Jour 4: Dossage deux fois par jour totalisant 400 mg. D'autres ajustements posologiques jusqu'à 800 mg / jour par jour 6 devraient être en augmentation de plus de 200 mg / jour. | 400-800 mg / jour | 800 mg / jour |
| 400-800 mg / jour | 800 mg / jour | ||
| Manie bipolaire - Enfants et adolescents (10 à 17 ans) monothérapie | Jour 1: 25 mg deux fois par jour. Day 2: Twice daily dosingtotaling 100 mg. Jour 3: Dossage deux fois par jour totalisant 200 mg. Jour 4: Dossage deux fois par jour totalisant 300 mg. Jour 5: Dossage deux fois par jour totalisant 400 mg. D'autres ajustements ne doivent pas être dans des incréments ne sont pas supérieurs à 100 mg / jour dans la plage de dose recommandée de 400 à 600 mg / jour. Sur la base de la réponse et de la tolérabilité, peut être administrée trois fois par jour. | 400-600 mg / jour | 600 mg / jour |
| Dépression bipolaire - Adultes | Administrer une fois par jour au coucher. Jour 1: 50 mg Jour 2: 100 mg Jour 3: 200 mg Jour 4: 300 mg | 300 mg / jour | 300 mg / jour |
| Thérapie d'entretien des troubles bipolaires - Adultes | Administrer deux fois par jour totalisant 400 à 800 mg / jour en complément de lithium ou de divalproex. Généralement, en phase d'entretien, les patients ont continué sur la même dose sur laquelle ils ont été stabilisés. | 400-800 mg / jour | 800 mg / jour |
Traitement d'entretien de la schizophrénie et du trouble bipolaire I
Traitement d'entretien
Les patients doivent être réévalués périodiquement pour déterminer la nécessité d'un traitement d'entretien et la dose appropriée pour un tel traitement [voir Études cliniques ].
Modifications de dose chez les patients âgés
Une considération doit être accordée à un rythme plus lent de titration de dose et à une dose cible plus faible chez les personnes âgées et chez les patients affaiblis ou qui ont une prédisposition aux réactions hypotensives [voir Pharmacologie clinique ]. When indicated dose escalation should be performed with caution in these patients.
Les patients âgés doivent être démarrés sur Seroquel 50 mg / jour et la dose peut être augmentée par incréments de 50 mg / jour en fonction de la réponse clinique et de la tolérabilité du patient individuel.
Modifications de la dose chez les patients atteints d'hépatition
Les patients souffrant de troubles hépatiques doivent être lancés sur 25 mg / jour. La dose doit être augmentée quotidiennement par incréments de 25 mg / jour -50 mg / jour à une dose efficace en fonction de la réponse clinique et de la tolérabilité du patient.
Modifications de dose lorsqu'elles sont utilisées avec les inhibiteurs du CYP3A4
La dose de séroquette doit être réduite à un sixième de la dose d'origine lorsqu'elle est co-médicée avec un puissant inhibiteur du CYP3A4 (par exemple, le kétoconazole itraconazole indinavir ritonavir néfazodone etc.). Lorsque l'inhibiteur du CYP3A4 est interrompu, la dose de Seroquel doit être augmentée de 6 fois [voir Pharmacologie clinique et Interactions médicamenteuses ].
Modifications de dose lorsqu'elles sont utilisées avec les inducteurs CYP3A4
La dose de séroquel doit être augmentée jusqu'à 5 fois de la dose d'origine lorsqu'elle est utilisée en combinaison avec un traitement chronique (par exemple plus de 7 à 14 jours) d'un puissant inducteur du CYP3A4 (par exemple, phénytoïne carbamazépine rifampin avasimibe St. John's wort, etc.). La dose doit être titrée en fonction de la réponse clinique et de la tolérabilité du patient individuel. Lorsque l'inducteur du CYP3A4 est interrompu, la dose de Seroquel doit être réduite au niveau d'origine dans les 7 à 14 jours [voir Pharmacologie clinique et Interactions médicamenteuses ].
La réinitiation du traitement chez les patients précédemment interrompus
Bien qu'il n'y ait pas de données pour aborder spécifiquement la réinitiation du traitement, il est recommandé que lors du redémarrage de la thérapie des patients qui sont hors séroquette depuis plus d'une semaine, le calendrier de dosage initial devrait être suivi. Lors du redémarrage des patients qui sont hors séroquette pendant une escalade de dose progressive d'une semaine peuvent ne pas être nécessaires et la dose d'entretien peut être réinitiée.
Passer des antipsychotiques
Il n'y a pas de données systématiquement collectées pour aborder spécifiquement le changement de patients atteints de schizophrénie des antipsychotiques à Seroquel ou concernant l'administration concomitante avec des antipsychotiques. Bien que l'arrêt immédiat du traitement antipsychotique précédent puisse être acceptable pour certains patients atteints de schizophrénie, un arrêt plus progressif peut être plus approprié pour d'autres. Dans tous les cas, la période de chevauchement des antipsychotiques doit être minimisée. Lors du changement de patients atteints de schizophrénie des antipsychotiques de dépôt, s'il est médicalement approprié, déclenche une thérapie séroquette à la place de l'injection programmée suivante. La nécessité de poursuivre les médicaments EPS existantes doit être réévaluée périodiquement.
Comment fourni
Dosage Forms And Strengths
- 25 mg comprimés sont des comprimés de pêche en revêtement de biconvexe identifiés par `` seroquel '' et «25» d'un côté et simple de l'autre côté
- 50 mg comprimés sont des comprimés blancs à revêtement de biconvex blancs identifiés avec `` seroquel '' et «50» d'un côté et simple de l'autre côté
- 100 mg de comprimés sont des comprimés en revêtement de biconvex jaunes identifiés par `` SEROQUE '' et «100» d'un côté et simple de l'autre côté
- 200 mg comprimés sont des comprimés blancs à revêtement biconvex blancs identifiés avec «Seroquel» et «200» d'un côté et simple de l'autre côté
- 300 mg de comprimés sont des comprimés de bicévrés en forme de capsule blancs intagliés avec «Seroquel» d'un côté et «300» de l'autre côté
- 400 mg comprimés sont des comprimés de bicévrée en revêtement biconvexes jaunes intagliés avec «Seroquel» d'un côté et «400» de l'autre côté
Stockage et manipulation
25 mg Tablettes ( NDC 0310-0275-10) Les comprimés en revêtement de film biconvexe de pêche identifiés par «Seroquel» et «25» d'un côté et simple de l'autre côté sont fournis dans des bouteilles de 100 comprimés.
50 mg Tablettes ( NDC 0310-0278-10) Des comprimés de films en revêtement biconvexe blancs blancs identifiés avec «Seroquel» et «50» d'un côté et simple de l'autre côté sont fournis dans des bouteilles de 100 comprimés.
100 mg Tablettes ( NDC 0310-0271-10) Les comprimés en revêtement de film biconvexe jaune identifiés identifiés avec «Seroquel» et «100» d'un côté et simple de l'autre côté sont fournis dans des bouteilles de 100 comprimés.
200 mg Tablettes ( NDC 0310-0272-10) Des comprimés de films en revêtement biconvexe blancs blancs identifiés avec «Seroquel» et «200» d'un côté et simple de l'autre côté sont fournis dans des bouteilles de 100 comprimés.
300 mg Tablettes ( NDC 0310-0274-60) Des comprimés de films biconvexes en forme de capsule blancs intagliés de «Seroquel» d'un côté et «300» de l'autre côté sont fournis dans des bouteilles de 60 comprimés.
400 mg Tablettes ( NDC 0310-0279-10) Des tablettes en revêtement de film bconvexes en forme de capsule jaune intagliées de «Seroquel» d'un côté et «400» de l'autre côté sont fournies dans des bouteilles de 100 comprimés.
Stocker à 25 ° C (77 ° F); Excursions autorisées à 15-30 ° C (59-86 ° F) [voir USP].
Distribué par: AstraZeneca Pharmaceuticals LP Wilmington de 19850. Révisé: janvier 2025.
Effets secondaires for Seroquel
Les effets indésirables suivants sont discutés plus en détail dans d'autres sections de l'étiquetage:
- Accrue de la mortalité chez les patients âgés atteints de psychose liée à la démence [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Pensées et comportements suicidaires chez les adolescents et les jeunes adultes [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Réactions indésirables cérébrovasculaires, y compris les AVC chez les patients âgés atteints de psychose liée à la démence [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Syndrome malin neuroleptique (NMS) [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Changements métaboliques (gain de poids de la dyslipidémie hyperglycémique) [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Dyskinésie tardive [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Hypotension [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Falls [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Augmentation de la pression artérielle (enfants et adolescents) [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Leukopénia neutropénie et l'agranulocytose [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Cataractes [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Prolongation QT [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Convulsions [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Hypothyroïdie [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Hyperprolactinémie [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Potentiel de déficience cognitive et motrice [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Régulation de la température corporelle [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Dysphagie [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Syndrome d'arrêt [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Effets anticholinergiques (antimuscariniques) [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
Expérience d'étude clinique
Étant donné que les études cliniques sont menées dans des conditions très variables les taux d'effets indésirables observés dans les études cliniques d'un médicament ne peuvent pas être directement comparés aux taux dans les études cliniques d'un autre médicament et peuvent ne pas refléter les taux observés dans la pratique.
Adultes
Les informations ci-dessous sont dérivées d'une base de données d'essais cliniques pour Seroquel composée de plus de 4300 patients. Cette base de données comprend 698 patients exposés à Seroquel pour le traitement de la dépression bipolaire 405 patients exposés à Seroquel pour le traitement de la manie bipolaire aiguë (monothérapie et thérapie complémentaire) 646 patients exposés à la séroquette pour le traitement d'entretien du trouble bipolaire I en tant que traitement auxiliaire et à environ 2600 patients et / ou normaux exposés à 1 ou plus doses de séroquage.
Parmi ces environ 4300 sujets environ 4000 (2300 dans la schizophrénie 405 dans la manie bipolaire aiguë 698 dans la dépression bipolaire et 646 pour le traitement d'entretien du trouble bipolaire I) étaient des patients qui ont participé à plusieurs essais d'efficacité et leur expérience correspondait à environ 2400 patients-années. Les conditions et la durée du traitement avec Seroquel variaient considérablement et incluaient (dans les catégories de chevauchement) des phases ouvertes et en double aveugle d'études des patients hospitalisés et des patients externes à dose fixe et à la dose-imitation et à une exposition à court terme ou à plus long terme. Les effets indésirables ont été évalués en collectant les réactions indésirables Résultats des examens physiques des signes vitaux Poids des analyses de laboratoire ECGS et des résultats des examens ophtalmologiques.
Les fréquences déclarées des effets indésirables représentent la proportion d'individus qui ont connu au moins une fois une réaction indésirable du type énuméré.
Réactions indésirables associées à l'arrêt du traitement dans les essais contrôlés par placebo à court terme
Schizophrénie
Dans l'ensemble, il y avait peu de différence dans l'incidence de l'arrêt en raison des effets indésirables (4% pour Seroquel contre 3% pour le placebo) dans un pool d'essais contrôlés. Cependant, les arrêts dus à la somnolence (0,8% Seroquel contre 0% de placebo) et à l'hypotension (0,4% Seroquel contre 0% de placebo) ont été considérés comme liés au médicament [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Trouble bipolaire
Manie
Les arrêts globaux dus aux effets indésirables étaient de 5,7% pour Seroquel contre 5,1% pour le placebo en monothérapie et 3,6% pour Seroquel contre 5,9% pour le placebo en thérapie complémentaire. Dépression: les interruptions globales dues aux effets indésirables étaient de 12,3% pour le séroquette 300 mg contre 19,0% pour le séroquette 600 mg et 5,2% pour le placebo.
Réactions indésirables couramment observées dans les essais contrôlés par placebo à court terme
Dans la thérapie aiguë de la schizophrénie (jusqu'à 6 semaines) et des essais sur la manie bipolaire (jusqu'à 12 semaines), les réactions indésirables les plus couramment observées associées à l'utilisation de la monothérapie séroquette (incidence de 5% ou plus) et observées à un taux sur séroquette au moins deux fois que le PlaceBo était une somnolence (8%) du poids (11%). (5%) et la dyspepsie (5%).
Réactions indésirables se produisant à une incidence de 2% ou plus chez les patients traités par Seroquel dans les essais contrôlés par placebo à court terme
Le prescripteur doit être conscient que les chiffres des tableaux et des tabulations ne peuvent pas être utilisés pour prédire l'incidence des effets secondaires au cours de la pratique médicale habituelle où les caractéristiques des patients et d'autres facteurs diffèrent de celles qui ont prévalu dans les essais cliniques. De même, les fréquences citées ne peuvent pas être comparées aux chiffres obtenus à partir d'autres recherches cliniques impliquant différents traitements et enquêteurs. Les chiffres cités fournissent cependant au médecin prescripteur une base pour estimer la contribution relative des facteurs de médicament et de non-médicament à l'incidence de l'effet secondaire dans la population étudiée.
Le tableau 9 énumère l'incidence arrondi au pourcentage le plus proche de réactions indésirables qui se sont produites pendant le traitement aiguë de la schizophrénie (jusqu'à 6 semaines) et de la manie bipolaire (jusqu'à 12 semaines) dans 2% ou plus des patients traités par Séroquel (doses allant de 75 à 800 mg / jour) où l'incidence dans les patients traitée avec séroquentil était plus que l'incidence dans les patients traités par placebo.
Tableau 9: Incidence des réactions indésirables dans les essais cliniques contrôlés par un placebo de 3 à 12 semaines pour le traitement de la schizophrénie et de la manie bipolaire (monothérapie)
| Terme préféré | Séroquel (n = 719) | PLACEBO (n = 404) |
| Mal de tête | 21% | 14% |
| Agitation | 20% | 17% |
| Somnolence | 18% | 8% |
| Vertiges | 11% | 5% |
| Bouche sèche | 9% | 3% |
| Constipation | 8% | 3% |
| Douleur | 7% | 5% |
| Tachycardie | 6% | 4% |
| Vomissement | 6% | 5% |
| Asthénie | 5% | 3% |
| Dyspepsie | 5% | 1% |
| Prise de poids | 5% | 1% |
| Alt a augmenté | 5% | 1% |
| Anxiété | 4% | 3% |
| Pharyngite | 4% | 3% |
| Éruption cutanée | 4% | 2% |
| Douleurs abdominales | 4% | 1% |
| Hypotension posturale | 4% | 1% |
| Maux de dos | 3% | 1% |
| AST a augmenté | 3% | 1% |
| Rhinite | 3% | 1% |
| Fièvre | 2% | 1% |
| Gastro-entérite | 2% | 0% |
| Amblyopie | 2% | 1% |
Dans la thérapie complémentaire aiguë de la manie bipolaire (jusqu'à 3 semaines) étudie les réactions indésirables les plus couramment observées associées à l'utilisation de Seroquel (incidence de 5% ou plus) et observée à un rythme de séroquel au moins deux fois celle de la constipation de la somnolence (34%) de la bouche sèche (19%) Asthenia (7%) de la constipation (10%) Abdominal Mouth (7%) Hypoension (7%) Pharyngite (6%) et prise de poids (6%).
Le tableau 10 énumère l'incidence arrondi au pourcentage le plus proche des effets indésirables qui se sont produits pendant le traitement (jusqu'à 3 semaines) de manie aiguë chez 2% ou plus des patients traités par sérocoul (doses allant de 100 à 800 mg / jour) utilisées comme traitement auxiliaires à un lithium et à divalproex où les patients traités par Seroquel étaient plus importants que l'incidence dans les patients sur place.
Tableau 10: Incidence des réactions indésirables dans les essais cliniques contrôlés par un placebo de 3 semaines pour le traitement de la manie bipolaire (thérapie auxiliaire)
| Terme préféré | Séroquel (n = 196) | PLACEBO (n = 203) |
| Somnolence | 34% | 9% |
| Bouche sèche | 19% | 3% |
| Mal de tête | 17% | 13% |
| Asthénie | 10% | 4% |
| Constipation | 10% | 5% |
| Vertiges | 9% | 6% |
| Tremblement | 8% | 7% |
| Douleurs abdominales | 7% | 3% |
| Hypotension posturale | 7% | 2% |
| Agitation | 6% | 4% |
| Prise de poids | 6% | 3% |
| Pharyngite | 6% | 3% |
| Maux de dos | 5% | 3% |
| Hypertension | 4% | 3% |
| Rhinite | 4% | 2% |
| Œdème périphérique | 4% | 2% |
| Contraction | 4% | 1% |
| Dyspepsie | 4% | 3% |
| Dépression | 3% | 2% |
| Amblyopie | 3% | 2% |
| Trouble de la parole | 3% | 1% |
| Hypotension | 3% | 1% |
| Niveau hormonal modifié | 3% | 0% |
| Lourdeur | 2% | 1% |
| Infection | 2% | 1% |
| Fièvre | 2% | 1% |
| Hypertension | 2% | 1% |
| Tachycardie | 2% | 1% |
| Appétit accru | 2% | 1% |
| Hypothyroïdie | 2% | 1% |
| Incoordination | 2% | 1% |
| Penser anormal | 2% | 0% |
| Anxiété | 2% | 0% |
| Ataxie | 2% | 0% |
| Sinusite | 2% | 1% |
| Transpiration | 2% | 1% |
| Infection des voies urinaires | 2% | 1% |
Dans les études de dépression bipolaire (jusqu'à 8 semaines), les réactions indésirables les plus fréquemment observées associées à l'utilisation de Seroquet (incidence de 5% ou plus) et observées à un rythme de Seroquel au moins deux fois celle du placebo étaient une somnolence (57%) de la bouche sèche (5%).
Le tableau 11 énumère l'incidence arrondi au pourcentage le plus proche de réactions indésirables qui se sont produites pendant le traitement (jusqu'à 8 semaines) de dépression bipolaire chez 2% ou plus des patients traités par sérocoul (doses de 300 et 600 mg / jour) où l'incidence chez les patients traitées avec Seroquel était supérieure à l'incidence chez les patients traités par placebo.
Tableau 11: Incidence des réactions indésirables dans les essais cliniques contrôlés par un placebo de 8 semaines pour le traitement de la dépression bipolaire
| Terme préféré | Séroquel (n = 698) | PLACEBO (n = 347) |
| Somnolence1 | 57% | 15% |
| Bouche sèche | 44% | 13% |
| Vertiges | 18% | 7% |
| Constipation | 10% | 4% |
| Fatigue | 10% | 8% |
| Dyspepsie | 7% | 4% |
| Vomissement | 5% | 4% |
| Appétit accru | 5% | 3% |
| Léthargie | 5% | 2% |
| Congestion nasale | 5% | 3% |
| Hypotension orthostatique | 4% | 3% |
| Doigt | 4% | 1% |
| Palpitations | 4% | 1% |
| Vision flou | 4% | 2% |
| Le poids a augmenté | 4% | 1% |
| Arthralgie | 3% | 2% |
| Parasthésie | 3% | 2% |
| Toux | 3% | 1% |
| Trouble extrapyramidal | 3% | 1% |
| Irritabilité | 3% | 1% |
| Dysarthrie | 3% | 0% |
| Hypersomnie | 3% | 0% |
| Congestion des sinus | 2% | 1% |
| Rêves anormaux | 2% | 1% |
| Tremblement | 2% | 1% |
| Reflux gastro-œsophagien | 2% | 1% |
| Douleur in Extremity | 2% | 1% |
| Asthénie | 2% | 1% |
| Trouble de l'équilibre | 2% | 1% |
| Hypoesthésie | 2% | 1% |
| Dysphagie | 2% | 0% |
| Syndrome des jambes agitées | 2% | 0% |
| 1. Somnolence combines adverse reaction terms somnolence et sedation |
Les explorations d'interactions sur la base de l'âge et de la race entre les sexes n'ont révélé aucune différence cliniquement significative dans la survenue de réaction indésirable sur la base de ces facteurs démographiques.
Dépendance de la dose des effets indésirables dans les essais contrôlés par placebo à court terme
Réactions indésirables liées à la dose
A provoqué spontanément les données sur les réactions indésirables d'une étude de la schizophrénie comparant cinq doses fixes de séroquette (75 mg 150 mg 300 mg 600 mg et 750 mg / jour) au placebo ont été explorées pour la dose-liaison des réactions indésirables. Les analyses de régression logistique ont révélé une réponse à la dose positive (P<0.05) for the folfaibleing adverse reactions: dyspepsia douleurs abdominales et prise de poids.
Réactions indésirables dans les essais cliniques avec la quétiapine et non répertoriés ailleurs dans l'étiquette
Les effets indésirables suivants ont également été rapportés par la quétiapine: hypersensibilité des cauchemars et élévations dans la créatine sérique phosphokinase (non associée à la SNM) galactorrhée bradycardie (qui peut se produire à ou près de l'initiation du traitement et être associée à l'hypotension et / ou à la synthèse) a diminué les niveaux de plaquettes (et autres événements connexes) des élévations de gamma dans les platelelettes de la gammat Éosinophilie rétention urinaire obstruction intestinale et priapisme.
Symptômes extrapyramidaux (EPS)
Dystonie
Effet de classe
Les symptômes de la dystonie prolongés des contractions anormales des groupes musculaires peuvent survenir chez les individus sensibles au cours des premiers jours de traitement. Les symptômes dystoniques comprennent: les spasmes des muscles du cou progressant parfois vers l'étanchéité de la gorge avaler des difficultés de difficulté à respirer et / ou à la saillie de la langue. Bien que ces symptômes puissent se produire à faibles doses, ils se produisent plus fréquemment et avec une plus grande gravité avec une puissance élevée et à des doses plus élevées de médicaments antipsychotiques de première génération. Un risque élevé de dystonie aiguë est observé chez les hommes et les groupes d'âge plus jeunes.
Quatre méthodes ont été utilisées pour mesurer l'EPS: (1) Score total Simpson-Angus (changement moyen par rapport à la ligne de base) qui évalue l'échelle d'évaluation globale de la parkinsonisme et de l'Akathisia (2) Incidence des plaintes spontanées de rigidité spontanée de rigidité spontanée et de rigidité de la rigidité hypertonia Akathisia Hypertonia. (4) Utilisation de médicaments anticholinergiques pour traiter l'EPS.
Adultes
Les données d'un essai clinique de 6 semaines de schizophrénie comparant cinq doses fixes de séroquette (75 150 300 600 750 mg / jour) ont fourni des preuves de l'absence de symptômes extrapyramidaux (EPS) et de dose-lié à l'EPS associés au traitement séroqueux. Trois méthodes ont été utilisées pour mesurer l'EPS: (1) Score total de Simpson-Angus (changement moyen par rapport à la ligne de base) qui évalue le parkinsonisme et l'akathisia (2) l'incidence des plaintes spontanées de la rigidité spontanée extrapyramidale du syndrome du syndrome d'hypokinésie rigidité et du tremblement du cou) et (3) de l'utilisation de l'EPSICIER.
Dans le tableau 12, l'événement dystonique comprenait la rigidité nucale Hypertonia Dystonia Muscle Rigidité OCULOGYRATION; Le parkinsonisme comprenait une hypokinésie bave des tremblements de rigidité de la roue de régime; Akathisia comprenait l'agitation psychomotrice de l'Akathisia; L'événement dyskinétique comprenait la dyskinésie tardive dyskinésie choréoathétose; et un autre événement extrapyramidal comprenait l'agitation du trouble du trouble extrapyramidal.
hydrocodone APAP 10-325
Tableau 12: Réactions indésirables associées à l'EPS dans un essai de schizophrénie de phase III multiple à court terme contrôlé par placebo (durée de 6 semaines)
| Terme préféré | Séroquel 75 mg / jour | Séroquel 150 mg / jour | Séroquel 300 mg / jour | Séroquel 600 mg / jour | Séroquel 750 mg / jour | Placebo | ||||||
| (N = 53) | (N = 48) | (N = 52) | (N = 51) | (N = 54) | (N = 51) | |||||||
| n | % | n | % | n | % | n | % | n | % | n | % | |
| Événement dystonique | 2 | 3.8 | 2 | 4.2 | 0 | 0.0 | 2 | 3.9 | 3 | 5.6 | 4 | 7.8 |
| Parkinsonisme | 2 | 3.8 | 0 | 0.0 | 1 | 1.9 | 1 | 2.0 | 1 | 1.9 | 4 | 7.8 |
| Doigt | 1 | 1.9 | 1 | 2.1 | 0 | 0.0 | 0 | 0.0 | 1 | 1.9 | 4 | 7.8 |
| Événement dyskinétique | 2 | 3.8 | 0 | 0.0 | 0 | 0.0 | 1 | 2.0 | 0 | 0.0 | 0 | 0.0 |
| Autre événement extrapyramidal | 2 | 3.8 | 0 | 0.0 | 3 | 5.8 | 3 | 5.9 | 1 | 1.9 | 4 | 7.8 |
Parkinsonisme incidence rates as measured by the Simpson-Angus total score for placebo et the five fixed doses (75 150 300 600 750 mg / jour) were: -0.6; -1.0 -1.2; -1.6; -1.8 et -1.8. Le rate of anticholinergic medication use to treat EPS for placebo et the five fixed doses was: 14%; 11%; 10%; 8%; 12% et 11%.
Dans six essais cliniques contrôlés par placebo supplémentaires (3 dans la manie aiguë et 3 dans la schizophrénie) en utilisant des doses variables de Seroquel, il n'y avait aucune différence entre les groupes de traitement Seroquel et placebo dans l'incidence de l'EPS, comme évalué par les scores totaux Simpson-Angus, les plaintes spontanées de l'EPS et l'utilisation de médicaments anticholinnergiques concomitants pour traiter les EPS.
Dans deux essais cliniques contrôlés par placebo pour le traitement de la dépression bipolaire en utilisant 300 mg et 600 mg de séroquette, l'incidence des effets indésirables potentiellement liés à l'EPS était de 12% dans les deux groupes de dose et 6% dans le groupe placebo. Dans ces études, l'incidence des effets indésirables individuels (Akathisia Trouble extrapyramidal Dyskinésie Dystonie Contractions musculaires involontaires L'hyperactivité psychomotrice et la rigidité musculaire) étaient généralement faibles et ne dépassaient 4% dans aucun groupe de traitement.
Les 3 groupes de traitement étaient similaires dans le changement moyen du score total SAS et les barres du score d'évaluation globale à la fin du traitement. L'utilisation de médicaments anticholinergiques concomitants était peu fréquente et similaire dans les trois groupes de traitement.
Enfants et adolescents
Les informations ci-dessous sont dérivées d'une base de données d'essais cliniques pour Seroquel composée de plus de 1000 patients pédiatriques. Cette base de données comprend 677 patients exposés à Seroquel pour le traitement de la schizophrénie et 393 enfants et adolescents (10-17 ans) exposés à Seroquel pour le traitement de la manie bipolaire aiguë.
Réactions indésirables associées à l'arrêt du traitement dans les essais contrôlés par placebo à court terme
Schizophrénie
L'incidence de l'arrêt due aux effets indésirables des patients traités par la quétiapine et traités par placebo était respectivement de 8,2% et 2,7%. L'événement indésirable conduisant à l'arrêt chez 1% ou plus des patients sous sérocoul et à une incidence plus importante que le placebo était une somnolence (2,7% et 0% pour le placebo).
Bipolaire I Mania
L'incidence de l'arrêt due aux effets indésirables des patients traités par la quétiapine et traités par placebo était respectivement de 11,4% et 4,4%. Les effets indésirables conduisant à l'arrêt chez 2% ou plus des patients sous sérocoul et à une incidence plus importante que le placebo étaient une somnolence (4,1% contre 1,1%) et de la fatigue (2,1% contre 0).
Réactions indésirables couramment observées dans les essais contrôlés par placebo à court terme
En thérapie pour la schizophrénie (jusqu'à 6 semaines), les effets indésirables les plus fréquemment observés associés à l'utilisation de la quétiapine chez les adolescents (incidence de 5% ou plus et incidence de la quétiapine au moins deux fois que pour le placebo) étaient des somnolences (34%), les plondements (12%) buccaux secs (7%) tachycardie (7%).
Dans la thérapie bipolaire (jusqu'à 3 semaines), les réactions indésirables les plus couramment observées associées à l'utilisation de la quétiapine chez les enfants et les adolescents (incidence de 5% ou plus et plus d'incidence quétiapine au moins deux fois pour le placebo) ont été une somnolence (53%) Dizziness (18%) Fastigue (11%) Appetite (7%) Bouche sèche (7%) et le poids a augmenté (6%).
Dans un essai SEROQUEL XR aigu (8 semaines) chez les enfants et les adolescents (10-17 ans) avec une dépression bipolaire dans laquelle l'efficacité n'a pas été établie les effets indésirables les plus couramment observés associés à l'utilisation de Seroquel XR (incidence de 5% ou au moins deux fois que pour PlaceBo) étaient des entêtres 7% diarrhée 5% de Fatgue 5% et Nausebo).
Réactions indésirables se produisant à une incidence ≥ 2% chez les patients traités par Seroquel dans les essais contrôlés par placebo à court terme
Schizophrénie (Adolescents 13-17 years old)
Les résultats suivants étaient basés sur un essai contrôlé par un placebo de 6 semaines dans lequel la quétiapine a été administrée à des doses de 400 ou 800 mg / jour.
Le tableau 13 énumère l'incidence arrondi au pourcentage le plus proche des effets indésirables qui se sont produits pendant le traitement (jusqu'à 6 semaines) de schizophrénie chez 2% ou plus des patients traités par sérocoul (doses de 400 ou 800 mg / jour) où l'incidence chez les patients traitées par Seroquel était au moins deux fois l'incidence chez les patients traités par placebo.
Les effets indésirables qui étaient potentiellement liés à la dose avec une fréquence plus élevée dans le groupe 800 mg par rapport au groupe 400 mg comprenaient des étourdissements (8% contre 15%) de la bouche sèche (4% contre 10%) et de la tachycardie (6% contre 11%).
Tableau 13: Incidence des réactions indésirables dans un essai clinique contrôlé par un placebo de 6 semaines pour le traitement de la schizophrénie chez les patients adolescents
| Terme préféré | Séroquel 400 mg (n = 73) | Séroquel 800 mg (n = 74) | Placebo (n = 75) |
| Somnolence1 | 33% | 35% | 11% |
| Vertiges | 8% | 15% | 5% |
| Bouche sèche | 4% | 10% | 1% |
| Tachycardie2 | 6% | 11% | 0% |
| Irritabilité | 3% | 5% | 0% |
| Arthralgie | 1% | 3% | 0% |
| Asthénie | 1% | 3% | 1% |
| Maux de dos | 1% | 3% | 0% |
| Dyspnée | 0% | 3% | 0% |
| Douleurs abdominales | 3% | 1% | 0% |
| Anorexie | 3% | 1% | 0% |
| Abcès dentaire | 3% | 1% | 0% |
| Dyskinésie | 3% | 0% | 0% |
| Épistaxis | 3% | 0% | 1% |
| Rigidité musculaire | 3% | 0% | 0% |
| 1. Somnolence combines adverse reaction terms somnolence et sedation. 2. Tachycardie combines adverse reaction terms tachycardia et sinus tachycardia |
Bipolaire I Mania (Enfants et adolescents 10-17 Years Old)
Les résultats suivants étaient basés sur un essai contrôlé par un placebo de 3 semaines dans lequel la quétiapine a été administrée à des doses de 400 ou 600 mg / jour.
Réactions indésirables couramment observées
Dans la thérapie bipolaire (jusqu'à 3 semaines), les réactions indésirables les plus couramment observées associées à l'utilisation de la quétiapine chez les enfants et les adolescents (incidence de 5% ou plus et plus d'incidence quétiapine au moins deux fois pour le placebo) ont été une somnolence (53%) Dizziness (18%) Fastigue (11%) Appetite (7%) Bouche sèche (7%) et le poids a augmenté (6%).
Le tableau 14 énumère l'incidence arrondi au pourcentage le plus proche des effets indésirables qui se sont produits pendant le traitement (jusqu'à 3 semaines) de manie bipolaire chez 2% ou plus des patients traités par sérocoul (doses de 400 ou 600 mg / jour) où l'incidence chez les patients traitées avec Seroquel était supérieure à l'incidence chez les patients traités par placebo.
Les effets indésirables qui étaient potentiellement liés à la dose avec une fréquence plus élevée dans le groupe 600 mg par rapport au groupe 400 mg comprenaient des nausées somnolence (50% contre 57%) (6% contre 10%) et la tachycardie (6% contre 9%).
Tableau 14: Réactions indésirables dans un essai clinique contrôlé par un placebo de 3 semaines pour le traitement de la manie bipolaire chez les enfants et les patients adolescents
| Terme préféré | Séroquel 400 mg (n = 95) | Séroquel 600 mg (n = 98) | Placebo (n = 90) |
| Somnolence1 | 50% | 57% | 14% |
| Vertiges | 19% | 17% | 2% |
| Nausée | 6% | 10% | 4% |
| Fatigue | 14% | 9% | 4% |
| Appétit accru | 10% | 9% | 1% |
| Tachycardie2 | 6% | 9% | 1% |
| Bouche sèche | 7% | 7% | 0% |
| Vomissement | 8% | 7% | 3% |
| Congestion nasale | 3% | 6% | 2% |
| Le poids a augmenté | 6% | 6% | 0% |
| Irritabilité | 3% | 5% | 1% |
| Pyrexie | 1% | 4% | 1% |
| Agression | 1% | 3% | 0% |
| Raideur musculo-squelettique | 1% | 3% | 1% |
| Surdose accidentel | 0% | 2% | 0% |
| Acné | 3% | 2% | 0% |
| Arthralgie | 4% | 2% | 1% |
| Léthargie | 2% | 2% | 0% |
| Pâleur | 1% | 2% | 0% |
| Malaise | 4% | 2% | 1% |
| Syncope | 2% | 2% | 0% |
| Vision flou | 3% | 2% | 0% |
| Constipation | 4% | 2% | 0% |
| Douleurs à l'oreille | 2% | 0% | 0% |
| Paresthésie | 2% | 0% | 0% |
| Congestion des sinus | 3% | 0% | 0% |
| Soif | 2% | 0% | 0% |
| 1. Somnolence combines adverse reactions terms somnolence et sedation. 2. Tachycardie combines adverse reaction terms tachycardia et sinus tachycardia. |
Symptômes extrapyramidaux
Dans un essai de monothérapie à court terme contrôlé par placebo chez les patients adolescents atteints de schizophrénie (durée de 6 semaines), l'incidence agrégée des symptômes extrapyramidaux était de 12,9% (19/147) pour la sérocoul et 5,3% (4/75) pour le placebo, mais l'incidence des réactions intimes (akathisia teamor La dyskinésie de la rigidité musculaire d'hyperactivité) n'a dépassé 4,1% dans aucun groupe de traitement. Dans un essai de monothérapie contrôlé par placebo à court terme chez les enfants et les adolescents atteints de manie bipolaire (durée de 3 semaines), l'incidence agrégée des symptômes extrapyramidaux était de 3,6% (7/193) ou de séroquel et 1,1% (1/90) pour le placebo.
Le tableau 15 présente une liste des patients atteints d'effets indésirables potentiellement associés aux symptômes extrapyramidaux dans l'essai de monothérapie à court terme contrôlé par placebo chez les adolescents atteints de schizophrénie (durée de 6 semaines).
Dans les tableaux 15 à 16 ans, l'événement dystonique comprenait la rigidité nucale hypertonie et la rigidité musculaire; Le parkinsonisme comprenait la rigidité et les tremblements de la roue de régime; L'Akathisia comprenait uniquement Akathisia; L'événement dyskinétique comprenait la dyskinésie tardive et la dyskinésie et la choréoathétose; et d'autres événements extrapyramidaux comprenaient l'agitation et le trouble extrapyramidal.
Tableau 15: Réactions indésirables associées aux symptômes extrapyramidaux dans l'essai contrôlé par placebo chez les adolescents atteints de schizophrénie (durée de 6 semaines)
| Terme préféré | Séroquel 400 mg/day (N = 73) | Séroquel 800 mg / jour (N = 74) | Tous Séroquel (N = 147) | Placebo (N = 75) | ||||
| n | % | n | % | n | % | n | % | |
| Événement dystonique | 2 | 2.7 | 0 | 0.0 | 2 | 1.4 | 0 | 0.0 |
| Parkinsonisme | 4 | 5.5 | 4 | 5.4 | 8 | 5.4 | 2 | 2.7 |
| Doigt | 3 | 4.1 | 4 | 5.4 | 7 | 4.8 | 3 | 4.0 |
| Événement dyskinétique | 2 | 2.7 | 0 | 0.0 | 2 | 1.4 | 0 | 0.0 |
| Autre événement extrapyramidal | 2 | 2.7 | 2 | 2.7 | 4 | 2.7 | 0 | 0.0 |
Le tableau 16 présente une liste des patients ayant des effets indésirables associés aux symptômes extrapyramidaux dans un essai de monothérapie à court terme contrôlé par placebo chez les enfants et les adolescents atteints de manie bipolaire (durée de 3 semaines).
Tableau 16: Réactions indésirables associées aux symptômes extrapyramidaux dans un essai contrôlé par placebo chez les enfants et les adolescents atteints de manie bipolaire I (durée de 3 semaines)
| Terme préféré1 | Séroquel 400 mg/day (N = 95) | Séroquel 600 mg / jour (N = 98) | Tous Séroquel (N = 193) | Placebo (N = 90) | ||||
| n | % | n | % | n | % | n | % | |
| Parkinsonisme | 2 | 2.1 | 1 | 1.0 | 3 | 1.6 | 1 | 1.1 |
| Doigt | 1 | 1.0 | 1 | 1.0 | 2 | 1.0 | 0 | 0.0 |
| Autre événement extrapyramidal | 1 | 1.1 | 1 | 1.0 | 2 | 1.0 | 0 | 0.0 |
| 1. Il n'y a eu aucune réaction indésirable avec le terme préféré des événements dystoniques ou dyskinétiques. |
ECG de laboratoire et changements de signes vitaux observés dans les études cliniques
Changements de laboratoire
Nombre de neutrophiles
Adultes
Dans les essais cliniques de monothérapie contrôlés par placebo impliquant 3368 patients sous quétiapine et 1515 sur placebo l'incidence d'au moins une occurrence de nombre de neutrophiles <1.0 x 109/ L chez les patients présentant un nombre normal de neutrophiles de base et au moins une mesure du laboratoire de suivi disponible était de 0,3% (10/2967) chez les patients traités par quétiapine par rapport à 0,1% (2/1349) chez les patients traités par placebo [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Élévations de la transaminase
Adultes
Des élévations transitoires et réversibles asymptomatiques dans les transaminases sériques (principalement ALT) ont été signalées. Dans les essais de schizophrénie chez l'adulte, les proportions de patients présentant des élévations de transaminase> 3 fois les limites supérieures de la plage de référence normale dans un pool d'essais contrôlés par placebo de 3 à 6 semaines étaient d'environ 6% (29/483) pour le séroquette par rapport à 1% (3/194) pour le placebo. Dans les essais de manie bipolaire aigus chez l'adulte, les proportions de patients présentant des élévations de transaminase> 3 fois les limites supérieures de la plage de référence normale dans un pool d'essais de 3 à 12 semaines contrôlés par placebo étaient d'environ 1% pour la sérète (3/560) et le placebo (3/294). Ces élévations enzymatiques hépatiques se sont généralement produites au cours des 3 premières semaines de traitement médicamenteuses et sont rapidement revenues à des niveaux de pré-étude avec un traitement en cours avec Seroquel. Dans les essais de dépression bipolaire, les proportions de patients présentant des élévations de transaminase> 3 fois les limites supérieures de la plage de référence normale dans deux essais contrôlés par placebo de 8 semaines étaient de 1% (5/698) pour SéRoQuel et 2% (6/347) pour le placebo.
Diminution de l'hémoglobine
Adultes
À court terme, les essais contrôlés par placebo diminuent hémoglobine à ≤13 g / dL mascules ≤12 g / dL femelles à au moins une occasion se sont produites chez 8,3% (594/7155) de patients traités par quetiapine contre 6,2% (219/3536) des patients traités par placebo. Dans une base de données d'essais cliniques contrôlés et incontrôlés, une diminution de l'hémoglobine à ≤13 g / dL ≤ 12 g / dL de femmes à au moins une occasion s'est produite dans 11% (2277/20729) de patients traités par quetiapine.
Interférence avec les écrans de médicament urinaire
Il y a eu des rapports de littérature suggérant des résultats faux positifs dans les immunoessais enzymatiques d'urine pour la méthadone et le tricyclique antidépresseurs chez les patients qui ont pris la quétiapine. La prudence doit être exercée dans l'interprétation des résultats positifs du dépistage des médicaments d'urine pour ces médicaments et la confirmation par une technique analytique alternative (par exemple, des méthodes chromatographiques) doivent être prises en compte.
Changements d'ECG
Adultes
Les comparaisons entre les groupes pour les essais contrôlés par placebo n'ont révélé aucune différence statistiquement significative séroquette / placebo dans les proportions des patients présentant des changements potentiellement importants dans les paramètres ECG, y compris les intervalles QT QTC et PR. Cependant, les proportions de patients répondant aux critères de tachycardie ont été comparées dans quatre essais cliniques contrôlés par un placebo de 3 à 6 semaines pour le traitement de la schizophrénie révélant une incidence de 1% (4/399) pour Séroquel contre 0,6% (1/156) pour un placebo. Dans les essais de manie bipolaire aiguë (monothérapie), les proportions des patients répondant aux critères de tachycardie étaient de 0,5% (1/192) pour Seroquel contre 0% (0/178) pour le placebo. Dans les essais de manie bipolaire aiguë (complément), les proportions de patients répondant aux mêmes critères étaient de 0,6% (1/166) pour Seroquel contre 0% (0/171) pour le placebo. Dans les essais de dépression bipolaire, aucun patient n'a eu une augmentation de la fréquence cardiaque à> 120 battements par minute. L'utilisation des séroquettes a été associée à une augmentation moyenne de la fréquence cardiaque évaluée par l'ECG de 7 battements par minute par rapport à une augmentation moyenne de 1 battement par minute chez les patients placebo. Cette légère tendance à la tachycardie chez les adultes peut être liée au potentiel de Seroquel pour induire des changements orthostatiques [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Enfants et adolescents
Dans l'essai aigu (6 semaines) de la schizophrénie chez les adolescents, une augmentation de la fréquence cardiaque (> 110 bpm) s'est produite dans 5,2% (3/73) des patients recevant des séroquettes de 400 mg et 8,5% (5/74) des patients recevant du sérocoul 800 mg par rapport à 0% (0/75) des patients recevant placebo. Les augmentations moyennes de la fréquence cardiaque étaient de 3,8 bpm et 11,2 bpm pour les groupes séroqueux de 400 mg et 800 mg respectivement par rapport à une diminution de 3,3 bpm dans le groupe placebo [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Dans l'essai aigu (3 semaines) de la manie bipolaire chez les enfants et les adolescents, une augmentation de la fréquence cardiaque (> 110 bpm) s'est produite chez 1,1% (1/89) de patients recevant du séroquette 400 mg et 4,7% (4/85) des patients recevant des séroquences 600 mg par rapport à 0% (0/98) de patients recevant un placebo. Les augmentations moyennes de la fréquence cardiaque étaient de 12,8 bpm et 13,4 bpm pour les groupes séroqueux de 400 mg et 600 mg respectivement par rapport à une diminution de 1,7 bpm dans le groupe placebo [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Dans un essai SEROQUEL XR aigu (8 semaines) chez les enfants et les adolescents (10-17 ans) atteints de dépression bipolaire dans laquelle l'efficacité n'a pas été établie, une augmentation de la fréquence cardiaque (> 110 bpm 10-12 ans et 13-17 ans) s'est produite chez 0% des patients recevant Seroquel XR et 1,2% des patients recevant un placebo. Les augmentations moyennes de la fréquence cardiaque étaient de 3,4 bpm pour Seroquel XR contre 0,3 bpm dans le groupe placebo [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Expérience de commercialisation de la poste
Les effets indésirables suivants ont été identifiés lors de l'approbation post-approbation de Seroquel. Étant donné que ces réactions sont rapportées volontairement d'une population de taille incertaine, il n'est pas toujours possible d'estimer de manière fiable leur fréquence ou d'établir une relation causale à l'exposition au médicament.
Les réactions indésirables signalées depuis l'introduction du marché qui étaient temporellement liées au traitement de la quétiapine comprennent la réaction de cardiomyopathie de réaction anaphylactique avec éosinophilie et systemic symptoms (DRESS) hypon / Atremia myocarditis nocturn / Al enuresis pancreatitis retrograde amnesia rhabdomyolysis syndrome of in / Appropriate antidiuretic hormone secretion (SIADH) Stevens-Johnson syndrome (SJS) toxic epidermal necrolysis (TEN) decreased platelet count serious liver reactions (including hepatitis liver necrosis et hepatic failure) Agranulocytisie Obstruction intestinale Ileus Colon Ischémie Rétention urinaire Apné de sommeil Généralisé aiguë Généralise exanthémateuse (AGEP) Vasculite cutanée confusion et incontinence fécale.
Interactions médicamenteuses for Seroquel
Effet d'autres médicaments sur la quétiapine
Les risques d'utilisation de Seroquel en combinaison avec d'autres médicaments n'ont pas été largement évalués dans des études systématiques. Étant donné les effets principaux du SNC de la prudence du séroquette, il faut être utilisé lorsqu'il est pris en combinaison avec d'autres médicaments à action centrale. Seroquel a potentialisé les effets cognitifs et motrices de l'alcool dans un essai clinique chez des sujets présentant des troubles psychotiques sélectionnés et des boissons alcoolisées devraient être limitées lors de la prise de la quétiapine.
L'exposition à la quétiapine est augmentée par les inhibiteurs du prototype du CYP3A4 (par exemple, le kétoconazole itraconazole indinavir ritonavir néfazodone, etc.) et diminué par le prototype des inducteurs CYP3A4 (par exemple, le carbamazépine de la phénytoïde. L'ajustement de la dose de la quétiapine sera nécessaire s'il est co-administré avec de puissants inducteurs ou inhibiteurs du CYP3A4.
Inhibiteurs du CYP3A4
La co-administration de kétoconazole Un puissant inhibiteur du cytochrome CYP3A4 a entraîné une augmentation significative de l'exposition à la quétiapine. La dose de Seroquel doit être réduite à un sixième de la dose d'origine si elle est co-administrée avec un fort inhibiteur du CYP3A4 [voir Posologie et administration et Pharmacologie clinique ].
Inducteurs CYP3A4
La co-administration de la quétiapine et de la phénytoïne A CYP3A4 a augmenté la clairance orale moyenne de la quétiapine de 5 fois. Des doses accrues de séroquel jusqu'à 5 fois peuvent être nécessaires pour maintenir le contrôle des symptômes de la schizophrénie chez les patients recevant la quétiapine et la phénytoïne ou d'autres inducteurs CYP3A4 puissants connus [voir [voir Posologie et administration et Pharmacologie clinique ]. When the CYP3A4 inducer is discontinued the dose of Séroquel should be reduced to the origin / Al level within 7-14 days [see Posologie et administration ].
Médicaments anticholinergiques
Le traitement concomitant avec la quétiapine et d'autres médicaments atteints d'activité anticholinergique peut augmenter le risque de réactions indésirables gastro-intestinales sévères liées à l'hypomotilité. Seroquel doit être utilisé avec prudence chez les patients recevant des médicaments ayant des effets anticholinergiques (antimuscariniques) [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Les effets potentiels de plusieurs médicaments concomitants sur la pharmacocinétique quétiapine ont été étudiés [voir Pharmacologie clinique ].
Effet de la quétiapine sur d'autres médicaments
En raison de son potentiel d'induction de l'hypotension, Seroquel peut améliorer les effets de certains agents antihypertenseurs.
Séroquel may antagonize the effects of levodopa et dopamine agonistes.
Il n'y a pas d'interactions pharmacocinétiques cliniquement pertinentes de Seroquel sur d'autres médicaments basés sur la voie CYP. Seroquel et ses métabolites ne sont pas inhibiteurs de CYP métabolisant majeur (1A2 2C9 2C19 2D6 et 3A4).
Abus de drogues et dépendance
Substance contrôlée
Séroquel is not a controlled substance.
Abus
Séroquel has not been systematically studied in animals or humans for its potential for abuse tolerance or physical dependence. While the clinical trials did not reveal any tendency for any drug-seeking behavior these observations were not systematic et it is not possible to predict on the basis of this limited experience the extent to which a CNS-active drug will be misused diverted et/or abused once marketed. Consequently patients should be evaluated carefully for a history of drug abuse et such patients should be observed closely for signs of misuse or abuse of Séroquel e.g. development of tolerance increases in dose drug-seeking behavior.
Avertissements pour seroquel
Inclus dans le cadre du 'PRÉCAUTIONS' Section
Précautions pour seroquel
Accrue de la mortalité chez les patients âgés atteints de psychose liée à la démence
Patients âgés atteints de démence psychose Traité avec des antipsychotiques courent un risque accru de décès. L'analyse de 17 essais contrôlés par placebo (durée modale de 10 semaines) en grande partie chez les patients prenant des antipsychotiques atypiques a révélé un risque de décès chez les patients traités par médicament entre 1,6 et 1,7 fois le risque de décès chez les patients traités par placebo. Au cours d'un essai contrôlé typique de 10 semaines, le taux de décès chez les patients traités par médicament était d'environ 4,5% contre un taux d'environ 2,6% dans le groupe placebo. Bien que les causes de la mort soient variées, la plupart des décès semblent être soit cardiovasculaires (par exemple, insuffisance cardiaque à la mort subite) ou infectieuse (par exemple pneumonie) dans la nature. Des études d'observation suggèrent que, similaire au traitement des antipsychotiques atypiques avec des antipsychotiques conventionnels, peut augmenter la mortalité. La mesure dans laquelle les résultats d'une mortalité accrue dans les études observationnelles peuvent être attribués au médicament antipsychotique par opposition à certaines caractéristiques des patients n'est pas clair. Seroquel n'est pas approuvé pour le traitement des patients atteints de psychose liée à la démence [voir Avertissement de boîte ].
Pensées et comportements suicidaires chez les adolescents et les jeunes adultes
Les patients atteints de troubles dépressifs majeurs (MDD) à la fois adultes et pédiatriques peuvent éprouver une aggravation de leur dépression et / ou de l'émergence d'idées et de comportements suicidaires (suicidalité) ou de changements inhabituels dans le comportement, qu'ils prennent ou non des médicaments antidépresseurs et ce risque peut persister jusqu'à ce que des remises significatives se produisent ou non. Le suicide est un risque connu de dépression et certains autres troubles psychiatriques et ces troubles eux-mêmes sont les prédicteurs les plus forts du suicide. Il y a eu une préoccupation de longue date que les antidépresseurs peuvent avoir un rôle dans l'induction de l'aggravation de la dépression et de l'émergence de la suicidalité chez certains patients au cours des premières phases du traitement. Des analyses regroupées des essais à court terme contrôlées par placebo de médicaments antidépresseurs (ISRS et autres) ont montré que ces médicaments augmentent le risque de pensée et de comportement suicidaires (suicidalité) chez les enfants adolescents et les jeunes adultes (âgés de 18 à 24 ans) avec un trouble dépressif majeur (MDD) et d'autres troubles psychiatriques. Des études à court terme n'ont pas montré d'augmentation du risque de suicidalité avec des antidépresseurs par rapport au placebo chez les adultes au-delà de 24 ans; Il y a eu une réduction des antidépresseurs par rapport au placebo chez les adultes de 65 ans et plus.
Les analyses regroupées des essais contrôlés par placebo chez les enfants et les adolescents atteints de TDM trouble obsessionnel compulsif (TOC) ou d'autres troubles psychiatriques comprenaient un total de 24 essais à court terme de 9 médicaments antidépresseurs chez plus de 4400 patients. Les analyses regroupées des essais contrôlées par placebo chez les adultes atteints de TDM ou d'autres troubles psychiatriques comprenaient un total de 295 essais à court terme (durée médiane de 2 mois) de 11 médicaments antidépresseurs chez plus de 77 000 patients. Il y avait une variation considérable du risque de suicidalité parmi les médicaments, mais une tendance à une augmentation des patients plus jeunes pour presque tous les médicaments étudiés. Il y avait des différences dans le risque absolu de suicidalité à travers les différentes indications avec l'incidence la plus élevée dans le TDM. Les différences de risque (médicament contre placebo) étaient cependant relativement stables dans les strates d'âge et à travers les indications. Ces différences de risque (la différence de lieu du lieu-lieu dans le nombre de cas de suicidalité pour 1000 patients traitées) sont fournis dans le tableau 2.
Tableau 2: Drug-lieu de différence dans le nombre de cas de suicidalité pour 1000 patients traités
| Tranche d'âge | Différence de drogue en place dans Nombre de cas de suicidalité pour 1000 patients traités |
| Augmentation par rapport au placebo | |
| <18 | 14 cas supplémentaires |
| 18-24 | 5 cas supplémentaires |
| Diminue par rapport au placebo | |
| 25-64 | 1 cas de moins |
| ≥65 | 6 cas moins |
Aucun suicide ne s'est produit dans aucun des essais pédiatriques. Il y avait des suicides dans les essais pour adultes, mais le nombre n'était pas suffisant pour parvenir à une conclusion sur l'effet du médicament sur le suicide.
On ne sait pas si le risque de suicidalité s'étend à une utilisation à plus long terme, c'est-à-dire au-delà de plusieurs mois. Cependant, il existe des preuves substantielles provenant d'essais d'entretien contrôlés par placebo chez les adultes souffrant de dépression que l'utilisation d'antidépresseurs peut retarder la récidive de la dépression.
Tous patients being treated with antidépresseurs for any indication should be monitored appropriately et observed closely for clinical worsening suicidality et unusual changes in behavior especially during the initial few months of a course of drug therapy or at times of dose changes either increases or decreases.
Les symptômes suivants agitation anxiété attaque l'insomnie Irritabilité Hostilité Agressivité Impulsivité Akathisie (agitation psychomotrice) Hypomanie et manie ont été signalées chez les patients adultes et pédiatriques traités avec des antidépresseurs principaux ainsi que pour d'autres indications psychiatriques et non psychiatriques. Bien qu'un lien causal entre l'émergence de ces symptômes et soit l'aggravation de la dépression et / ou l'émergence d'impulsions suicidaires ne se soient pas établies, il est à craindre que de tels symptômes représentent les précurseurs de la suicidalité émergente.
Une considération doit être accordée à la modification du régime thérapeutique, notamment en désintégrant le médicament chez les patients dont la dépression est constamment pire ou qui éprouve une suicidalité ou des symptômes émergents qui pourraient être des précurseurs pour aggraver la dépression ou la suicidalité, en particulier si ces symptômes sont graves abrupt lors de l'apparition ou ne faisaient pas partie des symptômes de présentation du patient.
Les familles et les soignants des patients traités avec des antidépresseurs pour un trouble dépressif majeur ou d'autres indications psychiatriques et non psychiatriques devraient être alertés sur la nécessité de surveiller les patients pour l'émergence de l'agitation d'irritabilité des changements inhabituels dans le comportement et les autres symptômes décrits ci-dessus ainsi que l'émergence de la suicidie et de signaler immédiatement ces symptômes aux prestataires de soins de santé. Une telle surveillance devrait inclure l'observation quotidienne par les familles et les soignants. Les prescriptions de SEROQUEL doivent être écrites pour la plus petite quantité de comprimés conformes à une bonne gestion des patients afin de réduire le risque de surdose.
Dépistage des patients pour trouble bipolaire
Un épisode dépressif majeur peut être la présentation initiale de trouble bipolaire . On pense généralement (bien que non établi dans les essais contrôlés) que le traitement d'un tel épisode avec un antidépresseur seul peut augmenter la probabilité de précipitation d'un épisode mixte / maniaque chez les patients à risque de trouble bipolaire. On ne sait pas si l'un des symptômes décrits ci-dessus représente une telle conversion. Cependant, avant de lancer un traitement avec un antidépresseur, y compris les patients SEROQUEL présentant des symptômes dépressifs, il faut être dépisté de manière adéquate pour déterminer s'ils sont à risque de trouble bipolaire; Un tel dépistage devrait inclure une histoire psychiatrique détaillée, notamment des antécédents familiaux de trouble bipolaire suicide et de dépression.
Réactions indésirables cérébrovasculaires, y compris les AVC chez les patients âgés atteints de psychose liée à la démence
Dans les essais contrôlés par placebo avec de la rispéridone aripiprazole et de l'olanzapine chez des sujets âgés atteints de démence, il y avait une incidence plus élevée d'adversaires cérébrovasculaires (accidents cérébrovasculaires et des attaques ischémiques transitoires), y compris des graisses par rapport aux sujets traités par placebo. Seroquel n'est pas approuvé pour le traitement des patients atteints de psychose liée à la démence [voir aussi Avertissement de boîte et Accrue de la mortalité chez les patients âgés atteints de psychose liée à la démence ].
Syndrome malin neuroleptique (NMS)
Un complexe de symptômes potentiellement mortel parfois appelé syndrome malin neuroleptique (NMS) a été signalé en association avec l'administration de médicaments antipsychotiques, y compris Seroquel. De rares cas de SNM ont été signalés avec Seroquel. Les manifestations cliniques des SNM sont la rigidité musculaire de l'hyperpyrexie altérée l'état mental et les preuves d'une instabilité autonome (impulsion irrégulière ou pression artérielle de la tachycardie diaphorèse et de la dysrhythmie cardiaque). Des signes supplémentaires peuvent inclure une créatinine phosphokinase myoglobinurie élevée (rhabdomyolyse) et insuffisance rénale aiguë .
L'évaluation diagnostique des patients atteints de ce syndrome est compliquée. En arrivant à un diagnostic, il est important d'exclure les cas où la présentation clinique comprend à la fois une maladie médicale grave (par exemple, une infection systémique de la pneumonie, etc.) et des signes et symptômes extrapyramidaux non traités ou mal traités. D'autres considérations importantes dans le diagnostic différentiel comprennent la toxicité centrale de la toxicité anticholique et la pathologie du système nerveux central primaire (SNC).
La gestion des SNM devrait comprendre: 1) l'arrêt immédiat des antipsychotiques et d'autres médicaments non essentiels à la thérapie simultanée; 2) traitement symptomatique intensif et surveillance médicale; et 3) le traitement de tout problème médical grave concomitant pour lequel des traitements spécifiques sont disponibles. Il n'y a aucun accord général sur des schémas de traitement pharmacologique spécifiques pour le NMS.
Si un patient a besoin d'un traitement médicamenteux antipsychotique après la récupération du SNM, la réintroduction potentielle du médicament doit être soigneusement prise en compte. Le patient doit être soigneusement surveillé car les récidives de SNM ont été signalées.
Changements métaboliques
Les antipsychotiques atypiques ont été associés à des changements métaboliques qui incluent l'hyperglycémie / diabète sucré dyslipidemia and body weight gain. While all of the drugs in the class have been shown to produce some metabolic changes each drug has its own specific risk profile. In some patients a worsening of more than one of the metabolic parameters of weight blood glucose and lipides a été observé dans les études cliniques. Les changements dans ces profils métaboliques devraient être gérés comme cliniquement appropriés.
Hyperglycémie et diabète sucré
L'hyperglycémie dans certains cas extrêmes et associée à la cétoacidose ou au coma hyperosmolaire ou à la mort a été signalée chez des patients traités par des antipsychotiques atypiques, notamment la quétiapine. L'évaluation de la relation entre l'utilisation des antipsychotiques atypiques et les anomalies du glucose est compliquée par la possibilité d'une augmentation du risque de fond de diabète sucré chez les patients atteints de schizophrénie et de l'incidence croissante du diabète sucré dans la population générale. Compte tenu de ces facteurs de confusion, la relation entre l'utilisation des antipsychotiques atypiques et les effets indésirables liés à l'hyperglycémie n'est pas complètement comprise. Cependant, les études épidémiologiques suggèrent un risque accru de réactions indésirables liées à l'hyperglycémie chez les patients traités avec les antipsychotiques atypiques. Des estimations précises des risques pour les effets indésirables liées à l'hyperglycémie chez les patients traitées par des antipsychotiques atypiques ne sont pas disponibles.
Les patients avec un diagnostic établi de diabète sucré qui sont lancé sur des antipsychotiques atypiques doivent être surveillés régulièrement pour l'aggravation du contrôle du glucose. Les patients présentant des facteurs de risque de diabète sucré (par exemple. obésité Les antécédents familiaux de diabète) qui commencent un traitement avec des antipsychotiques atypiques devraient subir des tests de glycémie à jeun au début du traitement et périodiquement pendant le traitement. Tout patient traité avec des antipsychotiques atypiques doit être surveillé pour les symptômes de l'hyperglycémie, y compris la polydipsie polyurie polyphagie et la faiblesse. Les patients qui développent des symptômes d'hyperglycémie pendant le traitement avec des antipsychotiques atypiques doivent subir des tests de glycémie à jeun. Dans certains cas, l'hyperglycémie s'est résolue lorsque l'antipsychotique atypique a été interrompu; Cependant, certains patients ont nécessité une poursuite du traitement antidiabétique malgré l'arrêt du médicament suspect.
Adultes
Tableau 3: Glucose à jeun - proportion de patients passant à ≥126 mg / dL dans des études contrôlées par placebo à court terme (≤12 semaines)1
| Analyte de laboratoire | Changement de catégorie (Au moins une fois) de la ligne de base | Bras de traitement | N | Patients n (%) |
| Jeûne Glucose | Normal à élevé (<100 mg/dL to ≥126 mg/dL) | Quétiapine | 2907 | 71 (2,4%) |
| Placebo | 1346 | 19 (1,4%) | ||
| Limite à haute (≥ 100 mg / dl et <126 mg/dL to ≥126 mg/dL) | Quétiapine | 572 | 67 (11,7%) | |
| Placebo | 279 | 33 (11,8%) | ||
| 1. Comprend les données Seroquel et Seroquel XR. |
Dans un essai de 24 semaines (115 patients contrôlés par actif traités par SEROQUEL) conçus pour évaluer le statut glycémique avec des tests de tolérance au glucose par voie orale de tous les patients à la semaine 24, l'incidence d'un défi de glucose de défi post-glucose ≥200 mg / dL était de 1,7% et l'incidence d'un niveau de glucose sanguin à jeun ≥126 mg / dL était de 2,6%. Le changement moyen du glucose à jeun par rapport à la ligne de base était de 3,2 mg / dL et le changement moyen du glucose 2 heures par rapport à la ligne de base était de -1,8 mg / dL pour la quétiapine.
Dans 2 essais cliniques de sevrage randomisés contrôlés par placebo à long terme pour l'exposition moyenne à l'entretien des troubles bipolaires de 213 jours pour le sérocoul (646 patients) et 152 jours pour le placebo (680 patients), le changement moyen du glucose de la ligne de base était de 5,0 mg / DL pour Seroquel et –0,05 mg / dL pour le placebo. Le taux ajusté en fonction de l'exposition de tout taux d'augmentation de la glycémie (≥126 mg / dL) pour les patients plus de 8 heures depuis un repas (mais certains patients peuvent ne pas avoir été exclus de l'apport calorique des liquides pendant la période de jeûne) était de 18,0 pour 100 années de patient pour le sérobène (10,7% des patients; n = 556) et 9,5 pour PlaceBO par 100 ans (4,6% des patients;
Enfants et adolescents
Dans une étude de monothérapie séroquetée contrôlée par placebo des patients adolescents (13-17 ans) avec une schizophrénie (6 semaines), le changement moyen des niveaux de glucose à jeun pour le sérocoul (n = 138) par rapport au placebo (n = 67) était de - 0,75 mg / dL contre –1,70 mg / dL. Dans une étude de monothérapie séroquetée contrôlée par placebo des enfants et des patients adolescents (10-17 ans) avec une manie bipolaire (durée de 3 semaines), le changement moyen du niveau de glucose à jeun pour le séroquel (n = 170) par rapport au placebo (n = 81) était de 3,62 mg / dL versus –1,17 mg / dL. Aucun patient dans l'une ou l'autre étude avec un niveau de glucose à jeun normal de base (<100 mg/dL) or a baseline borderline fasting glucose level (≥100 mg/dL et <126 mg/dL) had a blood glucose level of ≥126 mg/dL.
Effets secondaires du contrôle des naissances yaz
Dans une étude de monothérapie SEROQUEL XR contrôlée par placebo (durée de 8 semaines) des enfants et des adolescents (1017 ans) avec une dépression bipolaire dans laquelle l'efficacité n'a pas été établie, le changement moyen des niveaux de glucose à jeun pour le séroquette XR (n = 60) par rapport au placebo (n = 62) était de 1,8 mg / dL contre 1,6 mg / DL. Dans cette étude, il n'y avait pas de patients dans les groupes SEROQUEL XR ou traités par placebo avec un niveau de glucose à jeun normal de base (<100 mg/dL) that had an increase in blood glucose level>126 mg / dl. Il y avait un patient dans le groupe Seroquel XR avec un niveau de glucose à jeun limite de base (> 100 mg / dL et <126 mg/dL) who had an increase in blood glucose level of>126 mg / dL par rapport aux patients zéro dans le groupe placebo.
Dyslipidémie
Adultes
Le tableau 4 montre le pourcentage de patients adultes avec des changements dans les triglycérides totaux de cholestérol LDL-cholestérol et le HDL-cholestérol par rapport à l'indication dans les essais cliniques avec Seroquel.
Tableau 4: Pourcentage de patients adultes avec des quarts de travail dans le total des triglycérides LDL-cholestérol et le HDL-cholestérol de la ligne de base à des niveaux cliniquement significatifs par indication
| Laboratoire Analyte | Indication | Bras de traitement | N | Patients n (%) |
| Cholestérol total ≥ 240 mg / dl | Schizophrénie1 | Séroquel | 137 | 24 (18%) |
| Placebo | 92 | 6 (7%) | ||
| Bipolaire Dépression2 | Séroquel | 463 | 41 (9%) | |
| Placebo | 250 | 15 (6%) | ||
| Triglycérides ≥200 mg / dl | Schizophrénie1 | Séroquel | 120 | 26 (22%) |
| Placebo | 70 | 11 (16%) | ||
| Bipolaire Dépression2 | Séroquel | 436 | 59 (14%) | |
| Placebo | 232 | 20 (9%) | ||
| LDL Cholestérol ≥160 mg / dl | Schizophrénie1 | Séroquel | NA3 | NA3 |
| Placebo | NA3 | NA3 | ||
| Bipolaire Dépression2 | Séroquel | 465 | 29 (6%) | |
| Placebo | 256 | 12 (5%) | ||
| HDL Cholestérol ≤40 mg / dl | Schizophrénie1 | Séroquel | n / A3 | n / A3 |
| Placebo | n / A3 | n / A3 | ||
| Bipolaire Dépression2 | Séroquel | 393 | 56 (14%) | |
| Placebo | 214 | 29 (14%) | ||
| 1. Durée de 6 semaines 2. Durée de 8 semaines 3. Paramètres non mesurés dans les études d'enregistrement Seroquel pour la schizophrénie. |
Enfants et adolescents
Le tableau 5 montre le pourcentage d'enfants et d'adolescents ayant des changements dans les triglycérides totaux de cholestérol LDL-cholestérol et le HDL-cholestérol de la ligne de base dans les essais cliniques avec Seroquel.
Tableau 5: Pourcentage d'enfants et d'adolescents avec des changements dans le total des triglycérides de cholestérol ldlcholesterol et HDL-cholestérol de la ligne de base à des niveaux cliniquement significatifs
| Laboratoire Analyte | Indication | Bras de traitement | N | Patients n (%) |
| Cholestérol total ≥200 mg / dl | Schizophrénie1 | Séroquel | 107 | 13 (12%) |
| Placebo | 56 | 1 (2%) | ||
| Bipolaire Manie2 | Séroquel | 159 | 16 (10%) | |
| Placebo | 66 | 2 (3%) | ||
| Triglycérides ≥150 mg/dL | Schizophrénie1 | Séroquel | 103 | 17 (17%) |
| Placebo | 51 | 4 (8%) | ||
| Bipolaire Manie2 | Séroquel | 149 | 32 (22%) | |
| Placebo | 60 | 8 (13%) | ||
| LDL-Cholestérol ≥130 mg/dL | Schizophrénie1 | Séroquel | 112 | 4 (4%) |
| Placebo | 60 | 1 (2%) | ||
| Bipolaire Manie2 | Séroquel | 169 | 13 (8%) | |
| Placebo | 74 | 4 (5%) | ||
| HDL-Cholestérol ≤40 mg / dl | Schizophrénie1 | Séroquel | 104 | 16 (15%) |
| Placebo | 54 | 10 (19%) | ||
| Bipolaire Manie2 | Séroquel | 154 | 16 (10%) | |
| Placebo | 61 | 4 (7%) | ||
| 1. 13-17 ans 6 semaines Durée 2. 10-17 ans 3 semaines Durée |
In a placebo-controlled SEROQUEL XR monotherapy study (8 weeks duration) of children and adolescent patients (10 to 17 years of age) with bipolar depression in which efficacy was not established the percentage of children and adolescents with shifts in total cholesterol (≥200 mg/dL) triglycerides (≥150 mg/dL) LDL-cholesterol (≥ 130 mg/dL) et le cholestérol HDL (≤40 mg / dL) de la ligne de base aux niveaux cliniquement significatifs étaient: le cholestérol total 8% (7/83) pour Seroquel XR vs 6% (5/84) pour le placebo; triglycérides 28% (22/80) pour Seroquel XR contre 9% (7/82) pour le placebo; LDL-cholestérol 2% (2/86) pour Seroquel XR vs 4% (3/85) pour le placebo et le cholestérol HDL 20% (13/65) pour Seroquel XR contre 15% (11/74) pour le placebo.
Prise de poids
Des augmentations de poids ont été observées dans les essais cliniques. Les patients recevant la quétiapine devraient recevoir une surveillance régulière du poids.
Adultes
Dans les essais cliniques avec Seroquel, les augmentations de poids suivantes ont été signalées. 12
Tableau 6: Proportion de patients avec une prise de poids ≥ 7% du poids corporel (adultes)
| Vital Signe | Indication | Bras de traitement | N | Patients n (%) |
| Prise de poids ≥7% of Body Weight | Schizophrénie1 | Séroquel | 391 | 89 (23%) |
| Placebo | 206 | 11 (6%) | ||
| Bipolaire Manie (monotherapy)2 | Séroquel | 209 | 44 (21%) | |
| Placebo | 198 | 13 (7%) | ||
| Bipolaire Manie (thérapie auxiliaire)3 | Séroquel | 196 | 25 (13%) | |
| Placebo | 203 | 8 (4%) | ||
| Bipolaire Dépression4 | Séroquel | 554 | 47 (8%) | |
| Placebo | 295 | 7 (2%) | ||
| 1. jusqu'à 6 semaines de durée 2. jusqu'à 12 semaines de durée 3 jusqu'à 3 semaines de durée 4. jusqu'à 8 semaines de durée |
Enfants et adolescents
Dans deux essais cliniques avec Seroquel One dans la manie bipolaire et un dans la schizophrénie signalés par des augmentations de poids sont inclus dans le tableau 7.
Tableau 7: Proportion de patients ayant une prise de poids ≥ 7% du poids corporel (enfants et adolescents)
| Vital Signe | Indication | Bras de traitement | N | Patients n (%) |
| Prise de poids ≥7% of Body Weight | Schizophrénie1 | Séroquel | 111 | 23 (21%) |
| Placebo | 44 | 3 (7%) | ||
| Bipolaire Manie2 | Séroquel | 157 | 18 (12%) | |
| Placebo | 68 | 0 (0%) | ||
| 1. Durée de 6 semaines 2. Durée de 3 semaines |
Le changement moyen du poids corporel dans l'essai de schizophrénie était de 2,0 kg dans le groupe Seroquel et de -0,4 kg dans le groupe placebo et dans l'essai bipolaire de Mania, il était de 1,7 kg dans le groupe Seroquel et 0,4 kg dans le groupe placebo.
Dans une étude ouverte qui a recruté des patients des deux essais pédiatriques ci-dessus, 63% des patients (241/380) ont terminé 26 semaines de traitement avec Seroquel. Après 26 semaines de traitement, l'augmentation moyenne du poids corporel était de 4,4 kg. Quarante-cinq pour cent des patients ont gagné ≥ 7% de leur poids corporel non ajusté pour une croissance normale. Afin de s'adapter à une croissance normale sur 26 semaines, une augmentation d'au moins 0,5 écart-type par rapport à la base de base dans l'IMC a été utilisée comme mesure d'un changement cliniquement significatif; 18,3% des patients de Seroquel répondaient à ce critère après 26 semaines de traitement.
Dans un essai clinique pour Seroquel XR chez les enfants et les adolescents (10-17 ans) avec une dépression bipolaire dans laquelle l'efficacité n'a pas été établie, le pourcentage de patients avec une prise de poids ≥ 7% du poids corporel à tout moment était de 15% (14/92) pour le séroquette XR contre 10% (10/100) pour le placebo. Le changement moyen du poids corporel était de 1,4 kg dans le groupe Seroquel XR contre 0,6 kg dans le groupe placebo.
Lors du traitement des patients pédiatriques atteints de SéRoQue pour toute indication, la prise de poids doit être évaluée par rapport à celle attendue pour la croissance normale.
Dyskinésie tardive
Un syndrome de mouvements dyskinétiques involontaires potentiellement irréversibles peut se développer chez les patients traités par des antipsychotiques, notamment la quétiapine. Bien que la prévalence du syndrome semble être la plus élevée chez les personnes âgées, en particulier les femmes âgées, il est impossible de s'appuyer sur les estimations de prévalence pour prédire au début du traitement antipsychotique que les patients sont susceptibles de développer le syndrome. On ne sait pas si les produits anti-médicaments antipsychotiques diffèrent dans leur potentiel à provoquer une dyskinésie tardive.
Le risque de développer une dyskinésie tardive et la probabilité qu'elle devienne irréversible augmente à mesure que la durée du traitement et la dose cumulative totale des antipsychotiques administrés à l'augmentation du patient. Cependant, le syndrome peut se développer, bien que beaucoup moins couramment après des périodes de traitement relativement brèves à de faibles doses ou peut même survenir après l'arrêt du traitement.
La dyskinésie tardive peut se remettre partiellement ou complètement si le traitement antipsychotique est retiré. Le traitement antipsychotique lui-même peut cependant supprimer (ou supprimer partiellement) les signes et symptômes du syndrome et peut donc éventuellement masquer le processus sous-jacent. L'effet que la suppression symptomatique a sur l'évolution à long terme du syndrome est inconnu.
Compte tenu de ces considérations, Seroquel doit être prescrite d'une manière la plus susceptible de minimiser la survenue de dyskinésie tardive. Le traitement antipsychotique chronique doit généralement être réservé aux patients qui semblent souffrir d'une maladie chronique qui (1) est connu pour répondre aux médicaments antipsychotiques et (2) pour lesquels des traitements alternatifs tout aussi efficaces mais potentiellement moins nocifs ne sont pas disponibles ou appropriés. Chez les patients qui nécessitent un traitement chronique, la plus petite dose et la plus courte durée du traitement produisant une réponse clinique satisfaisante doivent être recherchées. La nécessité d'un traitement continu devrait être réévaluée périodiquement.
Si des signes et des symptômes de dyskinésie tardive apparaissent chez un patient sur l'arrêt du médicament séroqueux doit être pris en compte. Cependant, certains patients peuvent avoir besoin d'un traitement avec Seroquel malgré la présence du syndrome.
Hypotension
Quétiapine may induce orthostatic hypotension associated with vertiges tachycardia et in some patients syncope especially during the initial dose-titration period probably reflecting its α1- Propriétés antagonistes adrénergiques. La syncope a été signalée dans 1% (28/3265) des patients traités par Seroquel, contre 0,2% (2/954) sur le placebo et environ 0,4% (2/527) sur des médicaments témoins actifs. Les étourdissements et la syncope de l'hypotension orthostatique peuvent entraîner des chutes.
Séroquel should be used with particular caution in patients with known cardiovascular disease (history of myocardial infarction or ischemic heart disease heart failure or conduction abnormalities) cerebrovascular disease or conditions which would predispose patients to hypotension (dehydration hypovolemia et treatment with antihypertensive medications). Le risk of orthostatic hypotension et syncope may be minimized by limiting the initial dose to 25 mg twice daily [see Posologie et administration ]. If hypotension occurs during titration to the target dose a return to the previous dose in the titration schedule is appropriate.
Chute
Les antipsychotiques atypiques, y compris le sérocoul, peuvent provoquer une somnolence hypotension posturale Instabilité motrice et sensorielle qui peut entraîner des chutes et par conséquent des fractures ou d'autres blessures. Pour les patients atteints de maladies ou des médicaments qui pourraient exacerber ces effets, les évaluations des risques de chute complètes lors de la création d'un traitement antipsychotique et de manière récurrente pour les patients sous traitement antipsychotique à long terme.
Augmentation de la pression artérielle (enfants et adolescents)
Dans les essais contrôlés par placebo chez les enfants et les adolescents atteints de schizophrénie (durée de 6 semaines) ou de manie bipolaire (durée de 3 semaines), l'incidence des augmentations à tout moment dans la pression artérielle systolique (≥20 mmHg) était de 15,2% (51/335) pour SeroQuel et 5,5% (9/163) pour PlaceBo; L'incidence des augmentations à tout moment de la pression artérielle diastolique (≥10 mmHg) était de 40,6% (136/335) pour Seroquel et 24,5% (40/163) pour le placebo. Au cours de l'essai clinique ouvert de 26 semaines, un enfant ayant des antécédents d'hypertension a connu une crise hypertensive. La pression artérielle chez les enfants et les adolescents doit être mesurée au début et périodiquement pendant le traitement.
Dans un essai clinique Seroquel XR contrôlé par placebo (durée de 8 semaines) chez les enfants et les adolescents (10-17 ans) avec une dépression bipolaire dans laquelle l'efficacité n'a pas été établie, l'incidence des augmentations à tout moment dans la pression artérielle systolique (≥20 mmHg) était de 6,5% (6/92) pour le SEROCHEL et 6,0% (6/100) pour le placebo; L'incidence des augmentations à tout moment de la pression artérielle diastolique (≥10 mmHg) était de 46,7% (43/92) pour Seroquel XR et 36,0% (36/100) pour le placebo.
Leukopénia neutropénie et l'agranulocytose
Dans les essais cliniques et l'expérience post-commercialisation des événements de leukopénie / neutropénie ont été signalés temporellement liés aux agents antipsychotiques atypiques, dont Seroquel. Une agranulocytose a été signalée.
Agranulocytose (définie comme Nombre de neutrophiles absolus <500/mm3) a été signalé avec la quétiapine, y compris les cas mortels et les cas chez les patients sans facteurs de risque préexistants. La neutropénie doit être prise en compte chez les patients présentant une infection, en particulier en l'absence de facteurs prédisposants évidents ou chez les patients atteints de fièvre inexpliquée et doit être géré comme cliniquement approprié.
Les facteurs de risque possibles de leucopénie / neutropénie comprennent le faible nombre de cellules blanches préexistantes (WBC) et les antécédents de leucopénie / neutropénie induite par le médicament. Les patients avec une faible WBC préexistante ou des antécédents de leucopénie / neutropénie induite par un médicament devraient avoir leur Nombre de sang complet ( CBC ) surveillé fréquemment au cours des premiers mois de thérapie et devrait interrompre Seroquel au premier signe d'une baisse de WBC en l'absence d'autres facteurs causaux.
Patients with neutropénie should be carefully monitored for fièvre or other symptoms or signs of infection et treated promptly if such symptoms or signs occur. Patients with severe neutropénie (Nombre de neutrophiles absolus <1000/mm3) devrait interrompre Seroquel et faire suivre leur WBC jusqu'à la récupération.
Cataracte
Le développement de cataractes a été observé en association avec le traitement quétiapine dans les études chroniques de chiens [voir Toxicologie non clinique ]. Lens changes have also been observed in adults children et adolescents during longterm Séroquel treatment but a causal relationship to Séroquel use has not been established. Nevertheless the possibility of lenticular changes cannot be excluded at this time. Lerefore examin / Ation of the lens by methods adequate to detect cataract formation such as slit lamp exam or other appropriately sensitive methods is recommended at initiation of treatment or shortly thereafter et at 6-month intervals during chronic treatment.
Prolongation QT
Dans les essais cliniques, la quétiapine n'était pas associée à une augmentation persistante des intervalles de QT. Cependant, l'effet QT n'a pas été systématiquement évalué dans une étude QT approfondie. Dans une expérience post-marketing, il y avait des cas rapportés de l'allongement du QT chez les patients qui ont surédosé sur la quétiapine [voir Surdosage ] chez les patients atteints d'une maladie concomitante et chez les patients prenant des médicaments connus pour provoquer un déséquilibre électrolytique ou augmenter l'intervalle de QT [voir Interactions médicamenteuses ].
The use of quetiapine should be avoided in combination with other drugs that are known to prolong QTc including Class 1A antiarrythmics (e.g. quinidine procainamide) or Class III antiarrythmics (e.g. amiodarone sotalol) antipsychotic medications (e.g. ziprasidone chlorpromazine thioridazine) antibiotics (e.g. gatifloxacin moxifloxacin) or any other class of medications known to prolong the QTc interval (e.g. pentamidine levomethadyl acetate methadone).
Quétiapine should also be avoided in circumstances that may increase the risk of occurrence of torsade de pointes et/or sudden la mort including (1) a history of cardiac arrhythmias such as bradycardia; (2) hypokalemia or hypomagnesemia; (3) concomitant use of other drugs that prolong the QTc interval; et (4) presence of congenital prolongation of the QT interval.
La prudence doit également être exercée lorsque la quétiapine est prescrite chez les patients présentant un risque accru de prolongation QT (par exemple, les antécédents familiaux de la maladie cardiovasculaire de l'allongement des QT les personnes âgées insuffisance cardiaque congestive et heart hypertrophy).
Crises
Au cours des essais cliniques, des convulsions se sont produites dans 0,5% (20/3490) des patients traités par Seroquel contre 0,2% (2/954) sur le placebo et 0,7% (4/527) sur des médicaments témoins actifs. Comme pour les autres antipsychotiques, le sérocoul doit être utilisé
prudemment chez les patients ayant des antécédents de crises ou avec des conditions qui potentiellement abaisser le seuil de crise, par ex. Démence d'Alzheimer. Les conditions qui réduisent le seuil de crise peuvent être plus répandues dans une population de 65 ans ou plus.
Hypothyroïdie
Adultes: Clinical trials with quétiapine demonstrated dose-related decreases in thyroid hormone levels. Le reduction in total et free thyroxine (T4) d'environ 20% à l'extrémité supérieure de la plage de dose thérapeutique était maximale au cours des six premières semaines de traitement et maintenues sans adaptation ni progression pendant une thérapie plus chronique. Dans presque tous les cas4 Quelle que soit la durée du traitement. Le mécanisme par lequel la quétiapine affecte l'axe thyroïdien n'est pas claire. S'il y a un effet sur la mesure de l'axe hypothalamique-hypophysaire de la TSH seul peut ne pas refléter avec précision le statut thyroïdien d'un patient. Par conséquent, TSH et T Free4 En plus de l'évaluation clinique doit être mesurée au départ et au suivi.
Dans les études complémentaires de Mania où Seroquel a été ajouté au lithium ou au divalproex 12% (24/196) des patients traités par Seroquel, contre 7% (15/203) des patients traités par placebo avaient des niveaux élevés de TSH. Des patients traités par Seroquel avec des niveaux élevés de TSH 3 avaient simultanément faible4 Niveaux (T4<0.8 LLN).
Environ 0,7% (26/3489) des patients SEROQUEL ont connu des augmentations de TSH dans les études de monothérapie. Certains patients atteints d'augmentation de la TSH ont besoin d'un traitement thyroïdien de remplacement.
Dans tous les essais de quétiapine, l'incidence des changements dans les hormones thyroïdiennes et la TSH étaient 1: diminution du T libre4 (<0.8 LLN) 2.0% (357/17513); decrease in Total T4 (<0.8LLN) 4.0% (75/1861); decrease in gratuit t3 (<0.8 LLN) 0.4% (53/13766); decrease in Total T3 (<0.8LLN) 2.0% (26/1312) and increase in TSH (>5MIU / L) 4,9% (956/19412). Chez huit patients où le TBG a été mesuré des niveaux de TBG inchangés.
Le tableau 8 montre l'incidence de ces changements dans les essais cliniques contrôlés par placebo à court terme.
Tableau 8: Incidence des changements dans les niveaux d'hormones thyroïdiens et TSH dans les essais cliniques contrôlés par placebo à court terme12
| Total T4 | Gratuit t4 | Total T3 | Gratuit t3 | TSH | |||||
| Quétiapine | Placebo | Quétiapine | Placebo | Quétiapine | Placebo | Quétiapine | Placebo | Quétiapine | Placebo |
| 3,4% | 0,6% | 0,7% | 0,1% | 0,5% | 0,0% | 0,2% | 0,0% | 3,2% | 2,7% |
| (37/1097) | (4/651) | (52/7218) | (4/3668) | (2/369) | (0/113) | (11/5673) | (1/2679) | (240/7587) | (105/3912) |
| 1. Basé sur des changements de la ligne de base normale à une valeur potentiellement cliniquement importante à tout moment après la base. Change dans le total t4 gratuit t4 Total T3 et gratuit t3 sont définis comme <0.8 x LLN (pmol/L) and shift in TSH is>5 MLU / L à tout moment. 2. Comprend les données séroqueuses et séroqueuses XR |
Dans les essais de monothérapie contrôlés par placebo à court terme, l'incidence des changements réciproques en t3 et TSH was 0.0 % for both quétiapine (1/4800) et placebo (0/2190) et for T4 et TSH the shifts were 0,1% (7/6154) for quétiapine versus 0,0% (1/3007) for placebo.
Enfants et adolescents
Dans les essais aigus contrôlés par un placebo chez les enfants et les patients adolescents atteints de schizophrénie (durée de 6 semaines) ou de manie bipolaire (durée de 3 semaines), l'incidence des changements pour les valeurs de fonction thyroïdienne à tout moment pour les patients traités par Séroque 2,8% (8/289) contre 0% (0/145) respectivement. Des patients traités par Seroquel avec des niveaux élevés de TSH 1 avait simultanément faible4 Niveau à la fin du traitement.
Hyperprolactinémie
Adultes
Au cours des essais cliniques avec la quétiapine, l'incidence des changements dans les niveaux de prolactine à une valeur cliniquement significative s'est produite dans 3,6% (158/4416) des patients traités par quétiapine par rapport à 2,6% (51/1968) sur le placebo.
Enfants et adolescents
Dans les essais aigus contrôlés par un placebo chez les enfants et les patients adolescents atteints de manie bipolaire (durée de 3 semaines) ou de schizophrénie (durée de 6 semaines) L'incidence des changements dans les niveaux de prolactine à une valeur (> 20 μg / L des hommes; 8,7% (9/104) pour Seroquel contre 0% (0/39) pour le placebo chez les femmes.
Comme d'autres médicaments qui antagonisent la dopamine D2 Les récepteurs seroquel augmentent les niveaux de prolactine chez certains patients et l'élévation peut persister pendant l'administration chronique. L'hyperprolactinémie quelle que soit l'étiologie peut supprimer la GnRH hypothalamique entraînant une sécrétion de gonadotrophine hypophysaire réduite. Ceci peut à son tour inhiber la fonction reproductive en altérant la stéroïdogenèse gonadique chez les patients femmes et masculins. La galactorrhée amenorrhée gynécomastie et l'impuissance ont été rapportées chez les patients recevant des composés évelant de la prolactine. Une hyperprolactinémie de longue date lorsqu'elle est associée à l'hypogonadisme peut entraîner une diminution de la densité osseuse chez les sujets féminins et masculins.
Des expériences de culture tissulaire indiquent qu'environ un tiers des cancers du sein humain sont dépendants de la prolactine in vitro Un facteur d'importance potentielle si la prescription de ces médicaments est considérée chez un patient atteint d'un cancer du sein précédemment détecté. Comme cela est courant avec les composés qui augmentent la libération de la prolactine de la glande mammaire et la néoplasie des cellules pancréatiques (adénocarcinomes mammaires, adénomes pituitaires et pancréatiques) ont été observés dans des études de carcinogénicité menées chez la souris et les rats [voir Toxicologie non clinique] . Des études épidémiologiques publiées ont montré des résultats incohérents lors de l'exploration de l'association potentielle entre l'hyperprolactinémie et le cancer du sein.
Potentiel de déficience cognitive et motrice
Somnolence was a commonly reported adverse event reported in patients treated with Séroquel especially during the 3-5 day period of initial dose-titration. In schizophrenia trials somnolence was reported in 18% (89/510) of patients on Séroquel compared to 11% (22/206) of placebo patients. In acute bipolar mania trials using Séroquel as monotherapy somnolence was reported in 16% (34/209) of patients on Séroquel compared to 4% of placebo patients. In acute bipolar mania trials using Séroquel as adjunct therapy somnolence was reported in 34% (66/196) of patients on Séroquel compared to 9% (19/203) of placebo patients. In bipolar depression trials somnolence was reported in 57% (398/698) of patients on Séroquel compared to 15% (51/347) of placebo patients. Since Séroquel has the potential to impair judgment thinking or motor skills patients should be cautioned about performing activities requiring mental alertness such as operating a motor vehicle (including automobiles) or operating hazardous machinery until they are reason / Ably certain that Séroquel therapy does not affect them adversely. Somnolence may lead to chute.
Régulation de la température corporelle
Bien que non signalé avec la perturbation de Seroquel de la capacité du corps à réduire la température corporelle du noyau a été attribué aux agents antipsychotiques. Des soins appropriés sont conseillés lors de la prescription de Seroquel pour les patients qui éprouveront des conditions qui peuvent contribuer à une élévation de la température corporelle centrale, par ex. exercer une exposition vigoureuse à une chaleur extrême recevant des médicaments concomitants avec une activité anticholinergique ou étant soumis à une déshydratation.
Dysphagie
La dysmotilité et l'aspiration œsophagiennes ont été associées à la consommation de médicaments antipsychotiques. La pneumonie de l'aspiration est une cause fréquente de morbidité et de mortalité chez les patients âgés en particulier ceux atteints de démence avancée d'Alzheimer. La séroquel et d'autres médicaments antipsychotiques doivent être utilisés avec prudence chez les patients à risque de pneumonie d'aspiration.
Syndrome d'arrêt
Des symptômes de sevrage aigutes tels que l'insomnie nausée et vomissements ont été décrits après l'arrêt brutal des antipsychotiques atypiques, y compris la séroquette. Dans les essais cliniques de monothérapie à court terme contrôlé par placebo avec Seroquel XR qui comprenait une phase d'arrêt qui a évalué les symptômes d'arrêt de l'incidence agrégée des patients présentant un ou plusieurs symptômes d'arrêt après une cessation abrupte de 12,1% (241/1993) pour le SEROQUEL XR et 6,7% (71/1065) pour le placebo. L'incidence des effets indésirables individuels (c'est-à-dire l'insomnie nausée des nausées diarrhée vomissant les étourdissements et l'irritabilité) n'a dépassé 5,3% dans aucun groupe de traitement et généralement résolu après 1 semaine après le discontination. Un retrait progressif est conseillé. [voir Utiliser dans des populations spécifiques ].
Effets anticholinergiques (antimuscariniques)
Norquetiapine Un métabolite actif de la quétiapine a une affinité modérée à forte pour plusieurs sous-types de récepteurs muscariniques. Cela contribue aux effets indésirables anticholinergiques lorsque le sérocoul est utilisé à des doses thérapeutiques prises en concomitance avec d'autres médicaments anticholinergiques ou pris de surdosage. Seroquel doit être utilisé avec prudence chez les patients recevant des médicaments ayant des effets anticholinergiques (antimuscariniques) [voir Interactions médicamenteuses Surdosage et Pharmacologie clinique ].
Constipation was a commonly reported adverse event in patients treated with quétiapine et represents a risk factor for intestin / Al obstruction. Intestin / Al obstruction has been reported with quétiapine including fatal reports in patients who were receiving multiple concomitant medications that decrease intestin / Al motility.
Séroquel should be used with caution in patients with a current diagnosis or prior history of urin / Ary retention clinically significant prostatic hypertrophy or constipation.
Informations de conseil des patients
Conseiller au patient de lire l'étiquetage des patients approuvé par la FDA ( Informations sur les patients ).
Patients should be advised of the folfaibleing issues et asked to alert their prescriber if these occur while taking Séroquel.
Accrue de la mortalité chez les patients âgés atteints de psychose liée à la démence
Patients et caregivers should be advised that elderly patients with démence-related psychose treated with atypical antipsychotic drugs are at increased risk of la mort compared with placebo. Quétiapine is not approved for elderly patients with démence-related psychose [see AVERTISSEMENTS AND PRÉCAUTIONS ].
Pensées et comportements suicidaires
Patients their families et their caregivers should be encouraged to be alert to the emergence of anxiety agitation crises de panique insomnia irritability hostility aggressiveness impulsivity akathisia (psychomotor restlessness) hypomania mania other unusual changes in behavior worsening of depression et suicidal ideation especially early during antidépresseur treatment et when the dose is adjusted up or down. Families et caregivers of patients should be advised to look for the emergence of such symptoms on a day-to-day basis since changes may be abrupt. Such symptoms should be reported to the patient's prescriber or health profession / Al especially if they are severe abrupt in onset or were not part of the patient's presenting symptoms. Symptoms such as these may be associated with an increased risk for suicidal thinking et behavior et indicate a need for very close monitoring et possibly changes in the medication [see AVERTISSEMENTS AND PRÉCAUTIONS ].
Syndrome malin neuroleptique (NMS)
Patients should be advised to report to their physician any signs or symptoms that may be related to NMS. Lese may include muscle stiffness et forte fièvre [see AVERTISSEMENTS AND PRÉCAUTIONS ].
Hyperglycémie et diabète sucré
Patients should be aware of the symptoms of hyperglycemia (glycémie) et diabète sucré. Patients who are diagnosed with diabetes those with risk factors for diabète ou those that develop these symptoms during treatment should have their blood glucose monitored at the beginning of et periodically during treatment [see AVERTISSEMENTS AND PRÉCAUTIONS ].
Hyperlipidémie
Patients should be advised that elevations in total cholesterol LDL-cholesterol et triglycérides et decreases in HDL-cholesterol may occur. Patients should have their lipid profile monitored at the beginning of et periodically during treatment [see AVERTISSEMENTS AND PRÉCAUTIONS ].
Prise de poids
Patients should be advised that they may experience prise de poids. Patients should have their weight monitored regularly [see AVERTISSEMENTS AND PRÉCAUTIONS ].
Hypotension orthostatique
Patients should be advised of the risk of orthostatic hypotension (symptoms include feeling dizzy or lightheaded upon steting which may lead to chute) especially during the period of initial dose titration et also at times of re-initiating treatment or increases in dose [see AVERTISSEMENTS AND PRÉCAUTIONS ].
Augmentation de la tension artérielle chez les enfants et les adolescents
Les enfants et les patients adolescents devraient avoir leur tension artérielle mesurée au début et périodiquement pendant le traitement [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Leucopénie / neutropénie
Patients with a pre-existing faible WBC or a history of drug induced leukopenia/neutropénie should be advised that they should have their CBC monitored while taking Séroquel. Patients should be advised to talk to their doctor as soon as possible if they have a fièvre flu-like symptoms mal de gorge or any other infection as this could be a result of a very faible WBC which may require Séroquel to be stopped et/or treatment to be given [see AVERTISSEMENTS AND PRÉCAUTIONS ].
Interférence avec les performances cognitives et moteurs
Patients should be advised of the risk of somnolence or sedation (which may lead to chute) especially during the period of initial dose titration. Patients should be cautioned about performing any activity requiring mental alertness such as operating a motor vehicle (including automobiles) or operating machinery until they are reason / Ably certain quétiapine therapy does not affect them adversely [see AVERTISSEMENTS AND PRÉCAUTIONS ].
Exposition à la chaleur et déshydratation
Patients should be advised regarding appropriate care in avoiding overheating et dehydration [see AVERTISSEMENTS AND PRÉCAUTIONS ].
Médicaments concomitants
Comme pour les autres médicaments, les patients doivent être invités à informer leurs médecins s'ils prennent ou prévoient de prendre des médicaments sur ordonnance ou en vente libre [Voir Interactions médicamenteuses ].
Grossesse
Conseillez des femmes enceintes d'informer leur professionnel de la santé si elles tombent enceintes ou ont l'intention de devenir enceintes pendant le traitement par Seroquel. Conseillez les patients que Seroquel peut provoquer des symptômes extrapyramidaux et / ou de sevrage (Agitation Hypertonia hypotonia Tremor Somnolence Respiratory Distre and Aliteding Trouble) chez un nouveau-né. Conseiller les patients qu'il existe un registre de grossesse qui surveille les résultats de la grossesse chez les femmes exposées à Seroquel pendant la grossesse [voir Utiliser dans des populations spécifiques ].
Infertilité
Conseiller les femmes de potentiel reproducteur selon lesquelles Seroquel peut altérer la fertilité en raison d'une augmentation des taux sériques de prolactine. Les effets sur la fertilité sont réversibles [voir Utiliser dans des populations spécifiques ].
Besoin d'un programme de traitement complet
Séroquel is indicated as an integral part of a total treatment program for adolescents with schizophrenia et pediatric trouble bipolaire that may include other measures (psychological education / Al et social). Effectiveness et safety of Séroquel have not been established in pediatric patients less than 13 years of age for schizophrenia or less than 10 years of age for bipolar mania. Appropriate education / Al placement is essential et psychosocial intervention is often helpful. Le decision to prescribe atypical antipsychotic medication will depend upon the physician’s assessment of the chronicity et severity of the patient’s symptoms [see Indications ].
Que ne pas prendre avec Humira
Toxicologie non clinique
Carcinogenèse Mutagenèse A trouble de la fertilité
Cancérogenèse
Des études de cancérogénicité ont été menées chez des souris C57BL et des rats Wistar. La quétiapine a été administrée dans le régime alimentaire à des souris à des doses de 20 75 250 et 750 mg / kg et à des rats par gavage à des doses de 25 75 et 250 mg / kg pendant deux ans. Ces doses sont équivalentes à 0,1 0,5 1,5 et 4,5 fois le MRHD de 800 mg / jour sur la base de mg / m2 Surface corporelle (souris) ou 0,3 1 et 3 fois le MRHD à base de mg / m2 Surface corporelle (rats). Il y a eu des augmentations statistiquement significatives des adénomes folliculaires de la glande thyroïde chez les souris mâles à des doses de 1,5 et 4,5 fois le MRHD sur la base de Mg / M2 Surface corporelle et chez des rats mâles à une dose de 3 fois le MRHD sur Mg / M2 Surface corporelle. Les adénocarcinomes de la glande mammaire ont été statistiquement significativement augmentés chez les rats femelles à toutes les doses testées (0,3 1 et 3 fois le MRHD sur la base de Mg / M2 surface corporelle).
Les adénomes de cellules folliculaires thyroïdiens peuvent avoir résulté de la stimulation chronique de la glande thyroïde par l'hormone stimulante thyroïdienne (TSH) résultant d'un métabolisme accru et de la clairance de la thyroxine par le foie des rongeurs. Des changements dans la TSH thyroxine et la clairance de la thyroxine compatibles avec ce mécanisme ont été observés dans les études de toxicité sous-chronique chez le rat et la souris et dans une étude de toxicité à 1 an chez le rat; Cependant, les résultats de ces études n'étaient pas définitifs. La pertinence de l'augmentation des adénomes des cellules folliculaires thyroïdiennes au risque humain à travers le mécanisme est inconnu.
Il a été démontré que les médicaments antipsychotiques augmentent chroniquement les niveaux de prolactine chez les rongeurs. Les mesures sériques dans une étude de toxicité à 1 an ont montré que la quétiapine augmentait les niveaux de prolactine sérique médiane un maximum de 32 et 13 fois chez les rats mâles et femelles respectivement. Des augmentations des néoplasmes mammaires ont été trouvées chez les rongeurs après administration chronique d'autres médicaments antipsychotiques et sont considérés comme médiés par la prolactine. La pertinence de cette incidence accrue des tumeurs de la glande mammaire médiée par la prolactine chez le rat au risque humain est inconnue [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Mutagenèse
Quétiapine was not mutagenic or clastogenic in stetard genotoxicity tests. Le mutagenic potential of quétiapine was tested in the in vitro Test de mutation des gènes bactériens et dans le in vitro Dosage de mutation du gène des mammifères dans les cellules ovaires du hamster chinois. Le potentiel clastogène de la quétiapine a été testé dans le in vitro test d'aberration chromosomique dans les lymphocytes humains cultivés et dans le en vain Dosage de micronucléus de moelle osseuse chez le rat jusqu'à 500 mg / kg, soit 6 fois la MRHD sur la base de Mg / M2 Surface corporelle.
Altération de la fertilité
Quétiapine decreased mating et fertility in male Sprague-Dawley rats at oral doses of 50 et 150 mg/kg or approximately 1 et 3 times the MRHD of 800 mg / jour based on mg/m2 Surface corporelle. Drug-related effects included increases in interval to mate et in the number of matings required for successful impregn / Ation. Lese effects continued to be observed at 3 times the MRHD even after a two-week period without treatment. Le no-effect dose for impaired mating et fertility in male rats was 25 mg/kg or 0.3 times the MRHD based on mg/m2 Surface corporelle. Quétiapine adversely affected mating et fertility in female Sprague-Dawley rats at an oral dose approximately 1 times the MRHD of 800 mg / jour based on mg/m2 Surface corporelle. Drug-related effects included decreases in matings et in matings resulting in pregn / Ancy et an increase in the interval to mate. An increase in irregular estrus cycles was observed at doses of 10 et 50 mg/kg or approximately 0.1 et 1 times the MRHD of 800 mg / jour based on mg/m2 Surface corporelle. Le no-effect dose in female rats was 1 mg/kg or 0.01 times the MRHD of 800 mg / jour based on mg/m2 Surface corporelle.
Utiliser dans des populations spécifiques
Grossesse
Grossesse Exposure Registry
Il existe un registre d'exposition à la grossesse qui surveille les résultats de la grossesse chez les femmes exposées aux antipsychotiques atypiques, y compris le séroquette pendant la grossesse. Les prestataires de soins de santé sont encouragés à enregistrer des patients en contactant le National Grossancy Registry pour les antipsychotiques atypiques au 1-866-961-2388 ou en ligne à https://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/
Résumé des risques
Les nouveau-nés exposés aux antipsychotiques (y compris le séroquel) au cours du troisième trimestre sont à risque de symptômes extrapyramidaux et / ou de sevrage après l'accouchement (voir Considérations cliniques ). Overall available data from published epidemiologic studies of pregn / Ant women exposed to quétiapine have not established a drug-associated risk of major birth defects miscarriage or adverse matern / Al or fetal outcomes (see Données ). Lere are risks to the mother associated with untreated schizophrenia bipolar I or major depressive disorder et with exposure to antipsychotics including Séroquel during pregn / Ancy (see Considérations cliniques ).
Dans les études animales, la toxicité embryon-foetal s'est produite, notamment des retards dans l'ossification squelettique à environ 1 et 2 fois la dose humaine maximale recommandée (MRHD) de 800 mg / jour chez les rats et les lapins et une incidence accrue de flexion carpale / tarsal (tissu molle mineur anomaly) dans les fetuses de lapin à approximativement 2 fois le MRHD. De plus, les poids fœtaux ont diminué chez les deux espèces. La toxicité maternelle (observée comme une diminution du poids corporel et / ou de la mort) s'est produite à 2 fois le MRHD chez le rat et environ 1 à 2 fois le MRHD chez les lapins.
Le risque de fond estimé des principaux malformations congénitales et une fausse couche pour les populations indiquées est inconnue. Toutes les grossesses présentent un risque de fond de perte de maltraitance natale ou d'autres résultats indésirables. Dans la population générale américaine, le risque de fond estimé de malformations congénitales majeures et de fausse couche dans les grossesses cliniquement reconnues est respectivement de 2 à 4% et 15 à 20%.
Considérations cliniques
Risque maternel et / ou fœtal associé à la maladie
Il y a un risque pour la mère de la schizophrénie non traitée ou du trouble bipolaire I, y compris un risque accru d'hospitalisation et de suicide. La schizophrénie et les troubles bipolaires I sont associés à une augmentation des résultats périnataux défavorables, y compris une naissance prématurée. On ne sait pas s'il s'agit d'un résultat direct de la maladie ou d'autres facteurs comorbides.
Une étude longitudinale prospective a suivi 201 femmes enceintes ayant des antécédents de troubles dépressifs majeurs qui étaient euthymiques et prenaient des antidépresseurs au début de la grossesse. Les femmes qui ont interrompu les antidépresseurs pendant la grossesse étaient plus susceptibles de subir une rechute de dépression majeure que les femmes qui ont continué les antidépresseurs. Considérez le risque de dépression non traitée lors de l'arrêt ou de la modification du traitement avec des médicaments antidépresseurs pendant la grossesse et le post-partum.
Réactions indésirables fœtales / néonatales
Symptômes extrapyramidaux et / ou de sevrage, y compris l'agitation Hypertonia hypotonia Tremor Somnolence Respiratory Distre and Aliteding Trouble a été signalé chez les nouveau-nés qui ont été exposés à des médicaments antipsychotiques, y compris la séroQuel au cours du troisième trimestre de la grossesse. Ces symptômes variaient en gravité. Surveiller les nouveau-nés pour les symptômes extrapyramidaux et / ou de sevrage et gérer les symptômes de manière appropriée. Certains nouveau-nés se sont rétablis en quelques heures ou sans traitement spécifique; D'autres ont nécessité une hospitalisation prolongée.
Données
Données humaines
Les données publiées des études d'observation des registres de naissance et des rapports de cas sur l'utilisation des antipsychotiques atypiques pendant la grossesse ne signalent pas une association claire avec les antipsychotiques et les principaux malformations congénitales. Une étude de cohorte rétrospective d'une base de données Medicaid de 9258 femmes exposées aux antipsychotiques pendant la grossesse n'a pas indiqué un risque global accru de malformations congénitales majeures.
Données sur les animaux
Lorsque des rats et des lapins enceintes ont été exposés à la quétiapine pendant l'organogenèse, il n'y avait aucun effet tératogène chez les fœtus. Les doses étaient de 25 50 et 200 mg / kg chez le rat et 25 50 et 100 mg / kg chez les lapins qui sont d'environ 0,3 0,6 et 2 fois (rats) et 0,6 1 et 2 fois (lapins) le MRHD pour la schizophrénie de 800 mg / jour sur la base de Mg / M).2 Surface corporelle. However there was evidence of embryo-fetal toxicity including delays in skeletal ossification at approximately 1 et 2 times the MRHD of 800 mg / jour in both rats et rabbits et an increased incidence of carpal/tarsal flexure (minor soft tissue anomaly) in rabbit fetuses at approximately 2 times the MRHD. In addition fetal weights were decreased in both species. Matern / Al toxicity (observed as decreased body weights et/or la mort) occurred at 2 times the MRHD in rats et approximately 1-2 times the MRHD (all doses tested) in rabbits.
Dans une étude reproductive péri / postnatale chez le rat, aucun effet lié au médicament n'a été observé lorsque les barrages enceintes ont été traités par quétiapine à des doses de 0,01 0,1 et 0,2 fois le MRHD de 800 mg / jour sur la base de Mg / M2 Surface corporelle. However in a prelimin / Ary peri/postn / Atal study there were increases in fetal et pup la mort et decreases in mean litter weight at 3 times the MRHD.
Lactation
Résumé des risques
Données limitées de la littérature publiée rapportent la présence de quétiapine dans le lait maternel humain à la dose relative de nourrisson de <1% of the matern / Al weight-adjusted dosage. Lere are no consistent adverse events that have been reported in infants exposed to quétiapine through breast milk. Lere is no information on the effects of quétiapine on milk production. Le developmental et health benefits of breastfeeding should be considered along with the mother’s clinical need for Séroquel et any potential adverse effects on the breastfed child from Séroquel or from the mother’s underlying condition.
Femmes et mâles de potentiel reproducteur
Infertilité
Femelles
Basé sur l'action pharmacologique de la quétiapine (D2 antagonisme) Le traitement par sérocoul peut entraîner une augmentation des taux sériques de prolactine qui peuvent entraîner une réduction réversible de la fertilité chez les femmes de potentiel reproducteur [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Usage pédiatrique
En général, les effets indésirables observés chez les enfants et les adolescents au cours des essais cliniques étaient similaires à ceux de la population adulte à quelques exceptions près. Une augmentation de la pression artérielle systolique et diastolique s'est produite chez les enfants et les adolescents et n'a pas eu lieu chez l'adulte. L'hypotension orthostatique s'est produite plus fréquemment chez les adultes (4-7%) par rapport aux enfants et aux adolescents (<1%) [see AVERTISSEMENTS AND PRÉCAUTIONS et Effets indésirables ].
Schizophrénie
L'efficacité et l'innocuité de Seroquel dans le traitement de la schizophrénie chez les adolescents âgés de 13 à 17 ans ont été démontrées dans un essai contrôlé par un placebo en double aveugle de 6 semaines [voir Indications Posologie et administration Effets indésirables et Études cliniques ].
Innocuité et efficacité de Seroquel chez les patients pédiatriques de moins de 13 ans avec la schizophrénie n'a pas été établi.
Entretien
La sécurité et l'efficacité de Seroquel dans le traitement d'entretien du trouble bipolaire n'ont pas été établies chez les patients pédiatriques de moins de 18 ans. La sécurité et l'efficacité de Seroquel dans le traitement d'entretien de la schizophrénie n'ont été établies dans aucune population de patients, y compris les patients pédiatriques.
Bipolaire Manie
L'efficacité et l'innocuité de Seroquel dans le traitement de la manie chez les enfants et les adolescents âgés de 10 à 17 ans avec un trouble bipolaire I ont été démontrés dans un essai multicentrique contrôlé par placebo en double aveugle de 3 semaines [voir [voir Indications Posologie et administration Effets indésirables et Études cliniques ]. Safety et effectiveness of Séroquel in pediatric patients less than 10 years of age with bipolar mania have not been established.
Bipolaire Dépression
Innocuité et efficacité de Seroquel chez les patients pédiatriques de moins de 18 ans avec dépression bipolaire n'a pas été établi. Un essai clinique avec Seroquel XR a été mené chez les enfants et les adolescents (10-17 ans) avec une efficacité de dépression bipolaire n'a pas été établi.
Certaines différences dans la pharmacocinétique de la quétiapine ont été notées entre les enfants / adolescents (10-17 ans) et les adultes. Lorsqu'il est ajusté pour le poids, l'ASC et le CMAX de la quétiapine étaient respectivement de 41% et 39% chez les enfants et les adolescents par rapport aux adultes. La pharmacocinétique du métabolite actif norquetiapine était similaire entre les enfants / adolescents et les adultes après avoir ajusté le poids [voir Pharmacologie clinique ].
Utilisation gériatrique
Sur les environ 3700 patients en études cliniques avec Seroquel 7% (232) étaient âgés de 65 ans ou plus. En général, il n'y avait aucune indication d'une tolérabilité différente de Seroquel chez les personnes âgées par rapport aux jeunes adultes. Néanmoins, la présence de facteurs qui pourraient diminuer la clairance pharmacocinétique augmentent la réponse pharmacodynamique à Seroquel ou provoquer une tolérance ou une orthostase plus faible devrait conduire à une considération d'une dose de départ plus faible et à une surveillance minutieuse pendant la période de dosage initiale chez les personnes âgées. La clairance du plasma moyen de Seroquel a été réduite de 30% à 50% chez les patients âgés par rapport aux patients plus jeunes [voir Pharmacologie clinique et Posologie et administration ].
Trouble rénal
L'expérience clinique avec Seroquel chez les patients souffrant de troubles rénaux est limité [voir Pharmacologie clinique ].
Trouble hépatique
Étant donné que la quétiapine est largement métabolisée par le foie, des taux plasmatiques plus élevés sont attendus chez les patients souffrant de troubles hépatiques. Dans cette population, une faible dose de départ de 25 mg / jour est recommandée et la dose peut être augmentée par incréments de 25 mg / jour-50 mg / jour [voir Posologie et administration et Pharmacologie clinique ].
Informations sur la surdose pour Seroquel
Expérience humaine
Dans les essais cliniques, une survie a été signalée dans des surdoses aiguës allant jusqu'à 30 grammes de quétiapine. La plupart des patients qui ont surdosé n'ont connu aucune réaction indésirable ou se sont complètement rétablis des réactions signalées. Le décès a été signalé dans un essai clinique à la suite d'une surdose de 13,6 grammes de quétiapine seul. En général, les signes et les symptômes signalés étaient ceux résultant d'une exagération des effets pharmacologiques connus du médicament, à savoir la tachycardie de sédation de somnolence et la toxicité anticholinergique, y compris le coma et le délire. Les patients atteints d'une maladie cardiovasculaire sévère préexistante peuvent être à un risque accru des effets de la surdose [voir AVERTISSEMENTS AND PRÉCAUTIONS ]. One case involving an estimated overdose of 9600 mg was associated with hypokalemia et first-degree heart block. In post-marketing experience there were cases reported of QT prolongation with overdose.
Gestion de la surdosage
Établir et maintenir une voie aérienne et assurer une oxygénation et une ventilation adéquates. La surveillance cardiovasculaire devrait commencer immédiatement et doit inclure une surveillance électrocardiographique continue pour détecter les arythmies possibles.
Les mesures de soutien appropriées sont le pilier de la gestion. Pour les informations les plus à jour sur la gestion de Seroquel Overdosage, contactez un centre de contrôle régional de poison certifié (1-800-222-1222).
Contre-indications pour Seroquel
Hypersensibilité à la quétiapine ou à tout excipie dans la formulation de Seroquel. Des réactions anaphylactiques ont été rapportées chez les patients traités par Seroquel.
Pharmacologie clinique for Seroquel
Mécanisme d'action
Le mécanisme d'action de la quétiapine dans les indications énumérées n'est pas claire. Cependant, l'efficacité de la quétiapine dans ces indications pourrait être médiée par une combinaison de dopamine de type 2 (D2) et l'antagonisme de la sérotonine de type 2 (5HT2). Le métabolite actif n-desalkyl quetiapine (norquetiapine) a une activité similaire à d2 mais une plus grande activité à 5ht2A récepteurs que le médicament parent (quétiapine).
Pharmacodynamique
Quétiapine et its metabolite norquétiapine have affinity for multiple neurotransmitter receptors with norquétiapine binding with higher affinity than quétiapine in general. Le Ki values for quétiapine et norquétiapine at the dopamine D1 sont 428 / 99,8 nm à d2 626 / 489nm à la sérotonine 5ht1A 1040/191 nm à 5ht2A 38 / 2,9 nm à l'histamine H1 4.4 / 1,1 nm à la muscarinique M1 1086 / 38,3 nm et à l'adrénergique α1b 14,6 / 46,4 nm et à α2 Récepteurs 617/1290 nm respectivement. La quétiapine et la norquetiapine manquent d'une affinité appréciable avec les récepteurs de la benzodiazépine.
Effet sur l'intervalle QT
Dans les essais cliniques, la quétiapine n'était pas associée à une augmentation persistante des intervalles de QT. Cependant, l'effet QT n'a pas été systématiquement évalué dans une étude QT approfondie. Dans une expérience post-marketing, il y avait des cas rapportés de l'allongement du QT chez les patients qui ont surédosé sur la quétiapine [voir Surdosage ] chez les patients atteints d'une maladie concomitante et chez les patients prenant des médicaments connus pour provoquer un déséquilibre électrolytique ou augmenter l'intervalle de QT.
Pharmacocinétique
Adultes
Quétiapine activity is primarily due to the parent drug. Le multiple-dose pharmacokinetics of quétiapine are dose-proportion / Al within the proposed clinical dose range et quétiapine accumulation is predictable upon multiple dosing. Elimin / Ation of quétiapine is mainly via hepatic metabolism with a mean termin / Al half-life of about 6 hours within the proposed clinical dose range. Steady-state concentrations are expected to be achieved within two days of dosing. Quétiapine is unlikely to interfere with the metabolism of drugs metabolized by cytochrome P450 enzymes.
Enfants et adolescents
À l'état d'équilibre, la pharmacocinétique du composé parent chez les enfants et les adolescents (10-17 ans) était similaire aux adultes. Cependant, lorsqu'ils sont ajustés pour la dose et le poids, l'AUC et le CMAX du composé parent étaient respectivement de 41% et 39% chez les enfants et les adolescents que chez les adultes. Pour le métabolite actif, la norquetiapine AUC et CMAX étaient respectivement de 45% et 31% plus élevées chez les enfants et les adolescents que chez les adultes. Lorsqu'il est ajusté pour la dose et le poids, la pharmacocinétique du métabolite norquetiapine était similaire entre les enfants et les adolescents et les adultes [voir Utiliser dans des populations spécifiques ].
Absorption
Quétiapine is rapidly absorbed after oral administration reaching peak plasma concentrations in 1.5 hours. Le tablet formulation is 100% bioavailable relative to solution. Le bioavailability of quétiapine is margin / Ally affected by administration with food with Cmax et AUC values increased by 25% et 15% respectively.
Distribution
Quétiapine is widely distributed throughout the body with an apparent volume of distribution of 10±4 L/kg. It is 83% bound to plasma proteins at therapeutic concentrations. In vitro La quétiapine n'a pas affecté la liaison de la warfarine ou du diazépam à l'albumine sérique humaine. À son tour, ni la warfarine ni le diazépam n'ont modifié la liaison de la quétiapine.
Métabolisme et élimination
Après une seule dose orale de 14La c-quetiapine inférieure à 1% de la dose administrée a été excrétée en tant que médicament inchangé indiquant que la quétiapine est fortement métabolisée. Environ 73% et 20% de la dose ont été récupérés respectivement dans l'urine et les excréments.
Quétiapine is extensively metabolized by the liver. Le major metabolic pathways are sulfoxidation to the sulfoxide metabolite et oxidation to the parent acid metabolite; both metabolites are pharmacologically in / Active. In vitro Des études utilisant des microsomes hépatiques humains ont révélé que l'isoenzyme du cytochrome P450 3A4 est impliquée dans le métabolisme de la quétiapine à son métabolite de sulfoxyde majeur mais inactif et dans le métabolisme de son métabolite actif N-desalkyl quetiapine.
Âge
La clairance orale de la quétiapine a été réduite de 40% chez les patients âgés (≥ 65 ans n = 9) par rapport aux jeunes patients (n = 12) et un ajustement de dosage peut être nécessaire [voir Posologie et administration ].
Genre
Il n'y a aucun effet de genre sur la pharmacocinétique de la quétiapine.
Course
Il n'y a aucun effet racial sur la pharmacocinétique de la quétiapine.
Fumeur
Fumeur has no effect on the oral clearance of quétiapine.
Insuffisance rénale
Patients with severe ren / Al impairment (Clcr=10-30 mL/min/1.73 m2 n = 8) avait une clairance orale moyenne de 25% plus faible que les sujets normaux (CLCR> 80 ml / min / 1,73 m2 n = 8) Mais les concentrations plasmatiques de quétiapine chez les sujets présentant une insuffisance rénale se situaient dans la plage de concentrations observées chez les sujets normaux recevant la même dose. L'ajustement posologique n'est donc pas nécessaire chez ces patients [voir Utiliser dans des populations spécifiques ].
Insuffisance hépatique
Les patients atteints de troubles hépatique (n = 8) avaient une clairance orale moyenne de 30% de la quétiapine que les sujets normaux. Chez deux des 8 patients atteints de souffrance hépatique, l'AUC et le CMAX étaient 3 fois plus élevés que ceux observés généralement chez des sujets sains. Étant donné que la quétiapine est largement métabolisée par le foie, des taux plasmatiques plus élevés sont attendus dans la population altérée hépatique et un ajustement posologique peut être nécessaire [voir Posologie et administration et Utiliser dans des populations spécifiques ].
Études d'interaction médicament-médicament
Le en vain Les évaluations de l'effet d'autres médicaments sur la pharmacocinétique de la quétiapine sont résumées dans le tableau 17 [voir Posologie et administration et Interactions médicamenteuses ].
Tableau 17: L'effet d'autres médicaments sur la pharmacocinétique de la quétiapine
| Drogue à co-administration | Horaires de dose | Effet sur la pharmacocinétique quétiapine | |
| Drogue à co-administration | Quétiapine | ||
| Lable | 100 mg three times daily | 250 mg trois fois par jour | Augmentation de 5 fois de la clairance orale |
| Divalproex | 500 mg deux fois par jour | 150 mg deux fois par jour | 17% increase mean max plasma concentration at steady state. Aucun effet sur l'absorption ou la clairance orale moyenne |
| Thioridazine | 200 mg twice daily | 300 mg twice daily | Augmentation de 65% de la clairance orale |
| Cimétidine | 400 mg three times daily for 4 days | 150 mg trois fois par jour | 20% decrease in mean oral clearance |
| Kétoconazole (inhibiteur puissant du CYP 3A4) | 200 mg once daily for 4 days | 25 mg single dose | Une diminution de 84% de la clairance orale entraînant une augmentation de 6,2 fois de l'ASUC de quétiapine |
| Fluoxétine | 60 mg une fois par jour | 300 mg twice daily | Aucun changement dans l'état d'équilibre PK |
| Imipramine | 75 mg deux fois par jour | 300 mg twice daily | Aucun changement dans l'état d'équilibre PK |
| Halopéridol | 7,5 mg deux fois par jour | 300 mg twice daily | Aucun changement dans l'état d'équilibre PK |
| Rispéridone | 3 mg deux fois par jour | 300 mg twice daily | Aucun changement dans l'état d'équilibre PK |
In vitro Les données d'inhibition des enzymes suggèrent que la quétiapine et 9 de ses métabolites auraient peu d'effet inhibiteur sur en vain Métabolisme médié par les cytochromes CYP 1A2 2C9 2C19 2D6 et 3A4. La quétiapine à des doses de 750 mg / jour n'a pas affecté la pharmacocinétique à dose unique du lithium antipyrine ou du lorazépam (tableau 18) [voir Interactions médicamenteuses ].
Tableau 18: L'effet de la quétiapine sur la pharmacocinétique d'autres médicaments
| Drogue à co-administration | Horaires de dose | Effet sur d'autres médicaments pharmacocinétique | |
| Drogue à co-administration | Quétiapine | ||
| Lorazépam | 2 mg de dose unique | 250 mg trois fois par jour | La clairance orale de lalorazépam réduite de 20% |
| Divalproex | 500 mg deux fois par jour | 150 mg deux fois par jour | Le CMAX et l'AUC de l'acide valproïque libre à l'état d'équilibre ont été diminués de 10 à 12% |
| Lithium | Jusqu'à 2400 mg / jour donné en doses deux fois par jour | 250 mg trois fois par jour | Aucun effet sur la pharmacocinétique en régime permanent du lithium |
| Antipyrine | 1 g une seule dose | 250 mg trois fois par jour | Aucun effet sur la clairance de l'antipyrine ou de la récupération urinaire de ses métabolites |
Toxicologie et / ou pharmacologie animale
Quétiapine caused a dose-related increase in pigment deposition in glande thyroïde Dans les études de toxicité des rats qui étaient de 4 semaines ou plus et dans une étude de cancérogénicité de 2 ans de souris. Les doses étaient de 10 25 50 75 150 et 250 mg / kg dans des études de rat qui sont d'environ 0,1 0,3 0,6 1 2 et 3 fois le MRHD de 800 mg / jour sur la base de mg / m2 Surface corporelle respectivement. Les doses dans l'étude de la cancérogénicité de la souris étaient de 20 75 250 et 750 mg / kg qui sont d'environ 0,1 0,5 1,5 et 4,5 fois le MRHD de 800 mg / jour sur la base de Mg / m2 Surface corporelle. Pigment deposition was shown to be irreversible in rats. Le identity of the pigment could not be determined but was found to be co-localized with quétiapine in glande thyroïde follicular epithelial cells. Le function / Al effects et the relevance of this finding to human risk are unknown.
Chez les chiens recevant la quétiapine pendant 6 ou 12 mois, mais pas pour des cataractes triangulaires focales d'un mois, il s'est produit à la jonction des sutures postérieures dans le cortex externe de la lentille à une dose de 100 mg / kg ou 4 fois le MRHD de 800 mg / jour sur la base de mg / m / m2 Surface corporelle. This finding may be due to inhibition of cholesterol biosynthesis by quétiapine. Quétiapine caused a dose-related reduction in plasma cholesterol levels in repeat-dose dog et monkey studies; however there was no correlation between plasma cholesterol et the presence of cataracte in individual dogs. Le appearance of delta-8cholestanol in plasma is consistent with inhibition of a late stage in cholesterol biosynthesis in these species. Lere also was a 25% reduction in cholesterol content of the outer cortex of the lens observed in a special study in quétiapine treated female dogs. Drug-related cataracte have not been seen in any other species; however in a 1-year study in monkeys a striated appearance of the anterior lens surface was detected in 2/7 females at a dose of 225 mg/kg or 5.5 times the MRHD of 800 mg / jour based on mg/m2 Surface corporelle.
Études cliniques
Schizophrénie
Essais à court terme-adultes
Le efficacy of Séroquel in the treatment of schizophrenia was established in 3 short-term (6-week) controlled trials of inpatients with schizophrenia who met DSM III-R criteria for schizophrenia. Although a single fixed dose haloperidol arm was included as a comparative treatment in one of the three trials this single haloperidol dose group was in / Adequate to provide a reliable et valid comparison of Séroquel et haloperidol.
Plusieurs instruments ont été utilisés pour évaluer les signes et symptômes psychiatriques dans ces études parmi lesquels l'échelle de notation psychiatrique (BPRS) Un inventaire multi-éléments de la psychopathologie générale utilisée traditionnellement pour évaluer les effets du traitement médicamenteux dans la schizophrénie. Le cluster de psychose BPRS (désorganisation conceptuelle la suspicion des comportements hallucinatoires et le contenu de la pensée inhabituel) est considéré comme un sous-ensemble particulièrement utile pour évaluer les patients schizophrènes activement psychotiques. Une deuxième évaluation traditionnelle L'impression mondiale clinique (CGI) reflète l'impression d'un observateur qualifié pleinement familier avec les manifestations de la schizophrénie sur l'état clinique global du patient.
Le results of the trials folfaible:
- Dans un essai contrôlé par un placebo de 6 semaines (n = 361) (étude 1) impliquant 5 doses fixes de séroquette (75 mg / jour 150 mg / jour 300 mg / jour 600 mg / jour et 750 mg / jour donné en doses divisées trois fois par jour) Les 4 doses les plus élevées de Seroquel étaient généralement supérieures au score Place sur le score BPRS BPR Effet maximal observé à 300 mg / jour et les effets des doses de 150 mg / jour à 750 mg / jour étaient généralement indiscernables.
- Dans un essai contrôlé par un placebo de 6 semaines (n = 286) (étude 2) impliquant la titrage de Seroquel en haute (jusqu'à 750 mg / jour donné en doses divisées trois fois par jour) uniquement les doses de dose élevée (dose à forte dose (dose moyenne de 500 mg) a été superbe Cluster et le score de gravité CGI.
- Dans un essai de comparaison de dose et de dose de 6 semaines (n = 618) (étude 3) impliquant deux doses fixes de séroquel (450 mg / jour données en doses divisées deux fois par jour et trois fois par jour et 50 mg / jour donné en doses divisées deux fois par jour) seulement les 450 mg / jour (225 mg donnés par jour) Le groupe de dose sur le score total BPRS Le cluster de psychose BPRS et le score de gravité CGI.
Le primary efficacy results of these three studies in the treatment of schizophrenia in adults is presented in Table 19.
L'examen des sous-ensembles de population (sexe et âge de race) n'a révélé aucune réactivité différentielle sur la base de la race ou du sexe avec un effet apparemment plus important chez les patients de moins de 40 ans par rapport à ceux de plus de 40 ans. La signification clinique de cette constatation est inconnue.
Adolescents (13-17 ans)
Le efficacy of Séroquel in the treatment of schizophrenia in adolescents (13-17 years of age) was demonstrated in a 6-week double-blind placebo-controlled trial (Étude 4). Patients who met DSM-IV diagnostic criteria for schizophrenia were retomized into one of three treatment groups: Séroquel 400 mg/day (n = 73) Séroquel 800 mg / jour (n = 74) or placebo (n = 75). Étude medication was initiated at 50 mg/day et on day 2 increased to 100 mg/per day (divided et given two or three times per day). Subsequently the dose was titrated to the target dose of 400 mg/day or 800 mg / jour using increments of 100 mg/day divided et given two or three times daily. Le primary efficacy variable was the mean change from baseline in total Positive et Negative Syndrome Scale (PANSS).
Séroquel at 400 mg/day et 800 mg / jour was superior to placebo in the reduction of PANSS total score. Le primary efficacy results of this study in the treatment of schizophrenia in adolescents is presented in Table 19.
Tableau 19: essais à court terme de la schizophrénie
| Numéro d'étude | Groupe de traitement | Point de terminaison de l'efficacité principale: BPRS total | ||
| Score de base moyen (SD) | LS MANGE CHANGE de la ligne de base (SE) | Placebo-subtracted Différence1 (95% là-bas) | ||
| Étude 1 | Séroquel (75 mg / jour) | 45,7 (10,9) | -2.2 (2.0) | -4.0 (-11.2 3.3) |
| Séroquel (150 mg / jour)2 | 47.2 (10.1) | -8,7 (2.1) | -10.4 (-17.8 -3.0) | |
| Séroquel (300 mg / jour)2 | 45.3 (10.9) | -8,6 (2.1) | -10.3 (-17.6 -3.0) | |
| Séroquel (600 mg / jour)2 | 43,5 (11,3) | -7,7 (2.1) | -9.4 (-16.7 -2.1) | |
| Séroquel (750 mg / jour)2 | 45,7 (11.0) | -6.3 (2.0) | -8.0 (-15.2 -0.8) | |
| Placebo | 45.3 (9.2) | 1.7 (2.1) | - | |
| Étude 2 | Séroquel (250 mg/day) | 38.9 (9.8) | -4.2 (1.6) | -3.2 (-7,6 1.2) |
| Séroquel (750 mg / jour)2 | 41.0 (9.6) | -8,7 (1.6) | -7.8 (-12.2 -3.4) | |
| Placebo | 38.4 (9.7) | -1.0 (1.6) | - | |
| Étude 3 | Séroquel (450 mg/day BID) | 42.1 (10.7) | -10.0 (1.3) | -4.6 (-7.8 -1.4) |
| Séroquel (450 mg/day TID)3 | 42.7 (10.4) | -8,6 (1.3) | -3,2 (-6,4 0,0) | |
| Séroquel (50 mg BID) | 41.7 (10.0) | -5,4 (1.3) | - | |
| Point de terminaison de l'efficacité primaire: PANSS Total | ||||
| Score de base moyen (SD) | LS MANGE CHANGE de la ligne de base (SE) | Placebo-subtracted Différence1(95% là-bas) | ||
| Étude 4 | Séroquel (400 mg/day)2 | 96.2 (17.7) | -27.3 (2.6) | -8.2 (-16.1 -0.3) |
| Séroquel (800 mg / jour)2 | 96.9 (15.3) | -28.4 (1.8) | -9.3 (-16.2 -2.4) | |
| Placebo | 96.2 (17.7) | -19.2 (3.0) | - | |
| SD: écart-type; SE: erreur standard; LS signifie: les moindres carrés moyens; IC: Intervalle de confiance non ajusté. 1. Différence (médicament moins placebo) dans le changement des moindres carrés par rapport à la ligne de base. 2. Doses statistiquement significatives supérieures au placebo. 3. Doses qui sont statistiquement significatives supérieures à Seroquel 50 mg Bid. |
Trouble bipolaire
Bipolaire I Disorder Manic Or Mixed Episodes
Adultes
Le efficacy of Séroquel in the acute treatment of manic episodes was established in 3 placebo-controlled trials in patients who met DSM-IV criteria for bipolar I disorder with manic episodes. Lese trials included patients with or without psychotic features et excluded patients with rapid cycling et mixed episodes. Of these trials 2 were monotherapy (12 weeks) et 1 was adjunct therapy (3 weeks) to either lithium or divalproex. Key outcomes in these trials were change from baseline in the Young Manie Rating Scale (YMRS) score at 3 et 12 weeks for monotherapy et at 3 weeks for adjunct therapy. Adjunct therapy is defined as the simultaneous initiation or subsequent administration of Séroquel with lithium or divalproex.
Le primary rating instrument used for assessing manic symptoms in these trials was YMRS an 11-item clinician-rated scale tradition / Ally used to assess the degree of manic symptomatology (irritability disruptive/aggressive behavior sleep elevated mood speech increased activity sexual interest language/thought disorder thought content appearance et insight) in a range from 0 (no manic features) to 60 (maximum score).
Le results of the trials folfaible:
Monothérapie
Le efficacy of Séroquel in the acute treatment of bipolar mania was established in 2 placebo-controlled trials. In two 12-week trials (n=300 n=299) comparing Séroquel to placebo Séroquel was superior to placebo in the reduction of the YMRS total score at weeks 3 et 12. Le majority of patients in these trials taking Séroquel were dosed in a range between 400 mg/day et 800 mg per day (studies 1 et 2 in Table 20).
Thérapie auxiliaire
Dans cet essai contrôlé par un placebo de 3 semaines, 170 patients atteints de manie bipolaire (YMR ≥20) ont été randomisés pour recevoir Seroquel ou placebo comme traitement complémentaire au lithium ou au divalproex. Les patients peuvent ou non avoir reçu un traitement adéquat de lithium ou de divalproex avant la randomisation. Seroquel était supérieur au placebo lorsqu'il était ajouté au lithium ou au divalproex seul dans la réduction du score total des YMR (étude 3 dans le tableau 20).
Le majority of patients in this trial taking Séroquel were dosed in a range between 400 mg/day et 800 mg per day. In a similarly designed trial (n=200) Séroquel was associated with an improvement in YMRS scores but did not demonstrate superiority to placebo possibly due to a higher placebo effect.
Le primary efficacy results of these studies in the treatment of mania in adults is presented in Table 20.
Enfants et adolescents (ages 10-17)
Le efficacy of Séroquel in the acute treatment of manic episodes associated with bipolar I disorder in children et adolescents (10-17 years of age) was demonstrated in a 3-week double-blind placebo-controlled multicenter trial (Étude 4 in Table 20). Patients who met DSM-IV diagnostic criteria for a manic episode were retomized into one of three treatment groups: Séroquel 400 mg/day (n = 95) Séroquel 600 mg / jour (n = 98) or placebo (n=91). Étude medication was initiated at 50 mg/day et on day 2 increased to 100 mg/day (divided doses given two or three times daily). Subsequently the dose was titrated to a target dose of 400 mg/day or 600 mg / jour using increments of 100 mg/day given in divided doses two or three times daily. Le primary efficacy variable was the mean change from baseline in total YMRS score.
Séroquel 400 mg/day et 600 mg / jour were superior to placebo in the reduction of YMRS total score (Table 20).
Tableau 20: essais de manie
| Étude Nombre | Groupe de traitement | Mesure d'efficacité primaire: YMRS total | ||
| Baseline moyenne Score (SD)4 | Ls signifie changement de la ligne de base (SE) | Placebo-subtracted Différence2 (95% là-bas) | ||
| Étude 1 | Séroquel (200-800 mg / jour)1 3 | 34.0 (6.1) | -12.3 (1.3) | -4.0 (-7.0 -1.0) |
| Halopéridol1 3 | 32.3 (6.0) | -15.7 (1.3) | -7.4 (-10.4 -4.4) | |
| Placebo | 33.1 (6.6) | -8,3 (1.3) | - | |
| Étude 2 | Séroquel (200-800 mg / jour)1 | 32.7 (6.5) | -14.6 (1.5) | -7,9 (-10.9 -5.0) |
| Lithium1 3 | 33.3 (7.1) | -15.2 (1.6) | -8,5 (-11,5 -5,5) | |
| Placebo | 34.0 (6.9) | -6,7 (1.6) | - | |
| Étude 3 | Séroquel (200-800 mg / jour)1 stabilisateur d'humeur | 31,5 (5.8) | -13.8 (1.6) | -3.8 (-7.1 -0.6) |
| Placebo stabilisateur d'humeur | 31.1 (5.5) | -10 (1.5) | - | |
| Étude 4 | Séroquel (400 mg/day)1 | 29.4 (5.9) | -14,3 (0,96) | -5.2 (-8.1 -2.3) |
| Séroquel (600 mg / jour1 | 29.6 (6.4) | -15,6 (0,97) | -6.6 (-9.5 -3.7) | |
| Placebo | 30.7 (5.9) | -9.0 (1.1) | - | |
| Stabilisateur d'humeur: lithium ou divalproex; SD: écart-type; SE: erreur standard; LS signifie: les moindres carrés moyens; IC: Intervalle de confiance non ajusté. 1. Doses statistiquement significativement supérieures au placebo. 2. Différence (médicament moins placebo) dans le changement des moindres carrés par rapport à la ligne de base. 3. Inclus dans l'essai en tant que comparateur actif. 4. Le score de référence moyen des données adultes est basé sur les patients inclus dans l'analyse primaire; Le score de référence moyen pédiatrique est basé sur tous les patients de la population ITT. |
Trouble bipolaire Depressive Episodes
Adultes
Le efficacy of Séroquel for the acute treatment of épisodes dépressifs associés au trouble bipolaire was established in 2 identically designed 8-week retomized double-blind placebo-controlled studies (N=1045) (studies 5 et 6 in Table 21). Lese studies included patients with either bipolar I or II disorder et those with or without a rapid cycling course. Patients retomized to Séroquel were administered fixed doses of either 300 mg or 600 mg once daily.
Le primary rating instrument used to assess depressive symptoms in these studies was the Montgomery-Asberg Dépression Rating Scale (MADRS) a 10-item clinician-rated scale with scores ranging from 0 to 60. Le primary endpoint in both studies was the change from baseline in MADRS score at week 8. In both studies Séroquel was superior to placebo in reduction of MADRS score. Improvement in symptoms as measured by change in MADRS score relative to placebo was seen in both studies at Day 8 (week 1) et onwards. In these studies no addition / Al benefit was seen with the 600 mg dose. For the 300 mg dose group statistically significant improvements over placebo were seen in overall quality of life et satisfaction related to various areas of functioning as measured using the Q-LES-Q(SF).
Le primary efficacy results of these studies in the acute treatment of épisodes dépressifs associés au trouble bipolaire in adults is presented in Table 21.
Tableau 21: Épisodes dépressifs associés au trouble bipolaire
| Numéro d'étude | Groupe de traitement | Mesure d'efficacité primaire: madrs total | ||
| Baseline moyenne Score (SD) | Ls signifie changement de la ligne de base (SE) | Placebo-subtracted Différence2(95% là-bas) | ||
| Séroquel (300 mg / jour)1 | 30.3 (5.0) | -16,4 (0,9) | -6.1 (-8.3 -3.9) | |
| Étude 5 | Séroquel (600 mg / jour)1 | 30.3 (5.3) | -16,7 (0,9) | -6,5 (-8,7 -4.3) |
| Placebo | 30,6 (5.3) | -10,3 (0,9) | - | |
| Séroquel (300 mg / jour)1 | 31.1 (5.7) | -16.9 (1.0) | -5.0 (-7.3 -2.7) | |
| Étude 6 | Séroquel (600 mg / jour)1 | 29.9 (5.6) | -16.0 (1.0) | -4.1 (-6.4 -1.8) |
| Placebo | 29.6 (5.4) | -11.9 (1.0) | - | |
| SD: écart-type; SE: erreur standard; LS signifie: les moindres carrés moyens; IC: Intervalle de confiance non ajusté. 1. Doses statistiquement significativement supérieures au placebo. 2. Différence (médicament moins placebo) dans le changement des moindres carrés par rapport à la ligne de base. |
Traitement d'entretien As An Adjunct To Lithium Or Divalproex
Le efficacy of Séroquel in the mainten / Ance treatment of bipolar I disorder was established in 2 placebo-controlled trials in patients (n=1326) who met DSM-IV criteria for bipolar I disorder (studies 7 et 8 in Figures 1 et 2). Le trials included patients whose most recent episode was manic depressed or mixed with or without psychotic features. In the open-label phase patients were required to be stable on Séroquel plus lithium or divalproex for at least 12 weeks in order to be retomized. On average patients were stabilized for 15 weeks. In the retomization phase patients continued treatment with lithium or divalproex et were retomized to receive either Séroquel (administered twice daily totaling 400 mg/day to 800 mg / jour) or placebo. Approximately 50% of the patients had discontinued from the Séroquel group by day 280 et 50% of the placebo group had discontinued by day 117 of double-blind treatment. Le primary endpoint in these studies was time to recurrence of a mood event (manic mixed or depressed episode). A mood event was defined as medication initiation or hospitalization for a mood episode; YMRS score≥20 or MADRS score≥20 at 2 consecutive assessments; or study discontinuation due to a mood event (Figure 1 et Figure 2).
Dans les deux études, Seroquel était supérieur au placebo pour augmenter le temps de récidive de tout événement d'humeur. L'effet de traitement était présent pour l'augmentation du temps de récidive des épisodes maniaques et déprimés. L'effet de SeroQuel était indépendant de tout sous-groupe spécifique (Assigned Humeur Stabilizer Sex Age Race Episode Bipolar Episode ou Rapid Cycling Course).
Figure 1: Courbes de Kaplan-Meier du temps pour réciter un événement d'humeur (étude 7)
Figure 2: Courbes de Kaplan-Meier de la récidive d'un événement d'humeur (étude 8)
Informations sur le patient pour Seroquel
Séroquel
(Ser-oh-kwell)
(Quétiapine) comprimés
Lisez ce guide de médicaments avant de commencer à prendre Seroquel et chaque fois que vous obtenez une recharge. Il peut y avoir de nouvelles informations. Ces informations ne prennent pas la place de parler à votre fournisseur de soins de santé de votre état de santé ou de votre traitement.
Quelles sont les informations les plus importantes que je devrais connaître sur Seroquel?
Séroquel may cause serious side effects including:
- Risque de décès chez les personnes âgées atteintes de démence. Des médicaments comme Seroquel peuvent augmenter le risque de décès chez les personnes âgées qui ont une perte de mémoire (démence). Seroquel ne concerne pas le traitement de la psychose chez les personnes âgées atteintes de démence.
- Risque de pensées ou d'actions suicidaires (dépression antidépresseurs et autres maladies mentales graves et pensées ou actions suicidaires).
- Parlez à votre fournisseur de soins de santé de votre famille ou de votre famille:
- Tous les risques et avantages du traitement avec des antidépresseurs.
- Tous les choix de traitement pour la dépression ou toute autre maladie mentale grave
- Les médicaments antidépresseurs peuvent augmenter les pensées ou les actions suicidaires chez certains enfants adolescents et jeunes adultes au cours des premiers mois de traitement.
- Dépression et other serious mental illnesses are the most important causes of suicidal thoughts et actions. Some people may have a particularly high risk of having suicidal thoughts or actions. Lese include people who have (or have a family history of) depression bipolar illness (also called manic-depressive illness) or suicidal thoughts or actions.
- Comment puis-je surveiller et essayer d'empêcher les pensées et les actions suicidaires en moi-même ou un membre de la famille?
- Portez une attention particulière à tout changement, en particulier les changements soudains dans les pensées ou les sentiments des comportements de l'humeur. Ceci est très important lorsqu'un médicament antidépresseur est démarré ou lorsque la dose est modifiée.
- Appelez immédiatement le fournisseur de soins de santé pour signaler des changements nouveaux ou soudains dans les pensées ou les sentiments du comportement de l'humeur.
- Gardez toutes les visites de suivi avec le fournisseur de soins de santé comme prévu. Appelez le fournisseur de soins de santé entre les visites au besoin, surtout si vous avez des inquiétudes concernant les symptômes.
- Réflexions sur le suicide ou la mort
- tente de se suicider
- Dépression nouvelle ou pire
- Anxiété nouvelle ou pire
- Se sentir très agité ou agité
- crises de panique
- Diffusion de sommeil (insomnie)
- irritabilité nouvelle ou pire
- Agir agressif étant en colère ou violent
- Agissant sur des impulsions dangereuses 49
- Une augmentation extrême de l'activité et de la parole (manie) • Autres changements inhabituels dans le comportement ou l'humeur
- N'arrêtez jamais un médicament antidépresseur sans d'abord parler à votre fournisseur de soins de santé. L'arrêt d'un médicament antidépresseur peut soudainement provoquer d'autres symptômes.
- Les antidépresseurs sont des médicaments utilisés pour traiter la dépression et d'autres maladies. Il est important de discuter de tous les risques de traitement de la dépression et des risques de ne pas le traiter. Les patients et leurs familles ou autres soignants devraient discuter de tous les choix de traitement avec le fournisseur de soins de santé et pas seulement l'utilisation d'antidépresseurs.
- Les médicaments antidépresseurs ont d'autres effets secondaires. Parlez au fournisseur de soins de santé des effets secondaires du médicament prescrit à vous ou à un membre de votre famille.
- Les médicaments antidépresseurs peuvent interagir avec d'autres médicaments. Connaissez tous les médicaments que vous ou le membre de votre famille prenez. Gardez une liste de tous les médicaments pour montrer le fournisseur de soins de santé. Ne démarrez pas de nouveaux médicaments sans d'abord vérifier avec votre fournisseur de soins de santé.
- Tous les médicaments antidépresseurs prescrits aux enfants ne sont pas approuvés par la FDA pour une utilisation chez les enfants. Parlez au fournisseur de soins de santé de votre enfant pour plus d'informations.
- Schizophrénie chez les personnes âgées de 13 ans ou plus
- trouble bipolaire in adults including:
- épisodes dépressifs associés au trouble bipolaire
- épisodes maniaques associés au trouble bipolaire I seul ou au lithium ou au divalproex
- Traitement à long terme du trouble bipolaire I avec lithium ou divalproex
- Épisodes maniaques associés au trouble bipolaire I chez les enfants de 10 à 17 ans
On ne sait pas si Seroquel est sûr et efficace chez les enfants de moins de 10 ans.
Que dois-je dire à mon fournisseur de soins de santé avant de prendre Seroquel?
Avant de prendre Seroquel, dites à votre fournisseur de soins de santé si vous avez ou avez eu:
- diabète ou glycémie en vous ou à votre famille. Votre fournisseur de soins de santé doit vérifier votre glycémie avant de commencer Seroquel et aussi pendant la thérapie
- niveaux élevés de cholestérol total triglycérides ou LDL-cholestérol ou faibles niveaux de HDL-cholestérol
- Hypertension artérielle basse ou élevée
- faible Nombre de globules blancs
- cataracte
- crises
- tests de thyroïde anormaux
- Niveaux de prolactine élevés
- problèmes cardiaques
- problèmes de foie
- Toute autre condition médicale
- grossesse ou prévoit de devenir enceinte. On ne sait pas si Seroquel va nuire à votre bébé à naître.
- Si vous tombez enceinte en recevant Seroquel, parlez-en à votre fournisseur de soins de santé de vous inscrire auprès du National Pregnancy Registry pour les antipsychotiques atypiques. Vous pouvez vous inscrire en appelant le 1-866-961-2388 ou accéder à https://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/
- allaitement ou prévoit d'allaiter. Seroquel peut passer dans votre lait maternel. Parlez à votre fournisseur de soins de santé de la meilleure façon de nourrir votre bébé si vous recevez Seroquel.
- Si vous avez ou avez eu une condition où vous ne pouvez pas vider complètement votre vessie (rétention urinaire) avez une prostate ou une constipation agrandie ou une pression accrue à l'intérieur de vos yeux.
Parlez au fournisseur de soins de santé de tous les médicaments que vous prenez ou que vous avez récemment pris, y compris les médicaments sur ordonnance Suppléments à base de plantes en vente libre et vitamines.
Séroquel et other medicines may affect each other causing serious side effects. Séroquel may affect the way other medicines work et other medicines may affect how Séroquel works.
50 mg de prednisone pendant 3 jours
Dites à votre fournisseur de soins de santé si vous avez un écran de médicament urinaire, car Seroquel peut affecter les résultats de vos tests. Dites à ceux qui donnent le test que vous prenez Seroquel.
Comment devrais-je prendre Seroquel?
- Prenez Seroquel exactement comme votre fournisseur de soins de santé vous dit de le prendre. Ne changez pas la dose vous-même.
- Prenez Seroquel par la bouche avec ou sans nourriture.
- Si vous sentez que vous devez arrêter Seroquel parler d'abord avec votre fournisseur de soins de santé. Si vous cessez soudainement de prendre Seroquel, vous pouvez avoir des effets secondaires tels que des problèmes de sommeil ou du mal à rester endormis (insomnie) des nausées et des vomissements.
- Si vous manquez une dose de Seroquel, prenez-le dès que vous vous en souvenez. Si vous êtes proche de votre prochaine dose, sautez la dose manquée. Prenez simplement la prochaine dose à votre heure régulière. Ne prenez pas 2 doses en même temps à moins que votre professionnel de la santé ne vous le dise. Si vous n'êtes pas sûr de votre dosage, appelez votre fournisseur de soins de santé.
- Ne conduisez pas à faire fonctionner des machines ou ne faites pas d'autres activités dangereuses tant que vous ne savez pas comment Seroquel vous affecte. Seroquel peut vous rendre somnolent.
- Évitez de se faire surchauffer ou de déshydrater.
- Ne pas exercer.
- Par temps chaud, restez à l'intérieur dans un endroit frais si possible.
- Restez en dehors du soleil. Ne portez pas trop de vêtements ou lourds.
- Boire beaucoup d'eau.
- Ne buvez pas d'alcool en prenant Seroquel. Cela peut aggraver certains effets secondaires de Seroquel.
Quels sont les effets secondaires possibles de Seroquel?
Séroquel can cause serious side effects including:
- Vous voyez quelles sont les informations les plus importantes que je devrais connaître sur Seroquel?
- Un AVC qui peut entraîner la mort peut se produire chez les personnes âgées atteintes de démence qui prennent des médicaments comme Seroquel
- Syndrome malin neuroleptique (NMS). Le NMS est une condition rare mais très grave qui peut se produire chez les personnes qui prennent des antipsychotiques, y compris la séroquette. Les NM peuvent provoquer la mort et doivent être traités dans un hôpital. Appelez votre fournisseur de soins de santé immédiatement si vous devenez gravement malade et que vous avez tout ou partie de ces symptômes:
- forte fièvre
- transpiration excessive
- muscles rigides
- confusion
- Changements dans votre rythme cardiaque respiratoire et votre tension artérielle
- chute peut se produire chez certaines personnes qui prennent Seroquel. Ces chutes peuvent causer de graves blessures.
- glycémie (hyperglycemia) . Une glycémie élevée peut se produire si vous souffrez déjà du diabète ou si vous n'avez jamais eu de diabète. La glycémie élevée pourrait conduire à:
- accumulation d'acide dans votre sang en raison de cétones (cétoacidose)
- coma
- la mort
- Une augmentation de la glycémie peut se produire chez certaines personnes qui prennent Seroquel. La glycémie extrêmement élevée peut conduire au coma ou à la mort. Si vous souffrez de diabète ou de facteurs de risque de diabète (comme être en surpoids ou des antécédents familiaux de diabète), votre fournisseur de soins de santé devrait vérifier votre glycémie avant de commencer Seroquel et pendant la thérapie. Appelez votre fournisseur de soins de santé si vous présentez l'un de ces symptômes de glycémie élevée (hyperglycémie) tout en prenant Seroquel:
- avoir très soif
- besoin d'uriner plus que d'habitude
- se sentir très faim
- se sentir faible ou fatigué
- se sentir malade à votre estomac
- Sentez-vous confus ou votre souffle sent fruité
- Des niveaux élevés de graisses dans votre sang (augmentation du cholestérol et des triglycérides). Des niveaux élevés de graisses peuvent se produire chez les personnes traitées avec Seroquel. Vous n'avez peut-être pas de symptômes afin que votre fournisseur de soins de santé puisse décider de vérifier votre cholestérol et vos triglycérides pendant votre traitement avec Seroquel.
- augmentation du poids (gain de poids). La prise de poids est courante chez les personnes qui prennent Seroquel, vous et votre fournisseur de soins de santé devriez donc vérifier régulièrement votre poids. Parlez à votre fournisseur de soins de santé des moyens de contrôler la prise de poids tels que manger une alimentation saine et équilibrée et faire de l'exercice.
- Mouvements que vous ne pouvez pas contrôler dans la langue de votre visage ou d'autres parties du corps (dyskinésie tardive). Lese may be signs of a serious condition. Tardive dyskinesia may not go away even if you stop taking Séroquel. Tardive dyskinesia may also start after you stop taking Séroquel.
- diminution de la pression artérielle (hypotension orthostatique) y compris les étourdissements ou évanouissement causée par un changement soudain de la fréquence cardiaque et de la pression artérielle lors de la hausse trop rapidement d'une position assise ou couchée.
- Augmentation de la pression artérielle chez les enfants et les adolescents. Votre fournisseur de soins de santé doit vérifier la pression artérielle chez les enfants et les adolescents avant de commencer la séroquette et pendant la thérapie.
- faible Nombre de globules blancs. Dites à votre fournisseur de soins de santé dès que possible si vous avez des symptômes pseudo-grippaux ou toute autre infection, car cela pourrait être le résultat d'un nombre de globules blancs très faible. Votre fournisseur de soins de santé peut vérifier votre niveau de globules blancs pour déterminer si un traitement ou une autre action supplémentaire est nécessaire.
- cataracte
- crises
- tests de thyroïde anormaux. Votre professionnel de la santé peut faire des tests sanguins pour vérifier votre niveau hormonal thyroïdien.
- augmentation des niveaux de prolactine
- Diette de la somnolence Sentiment fatigué de la difficulté à penser et à faire des activités normales
- augmentation de la température corporelle
- difficulté à avaler
- Des problèmes de sommeil ou du mal à rester endormis (insomnie) nausées ou vomissements si vous arrêtez soudainement de Seroquel. Lese symptoms usually get better 1 week after you start having them.
Le most common side effects of Séroquel include:
Chez les adultes:
- somnolence
- une chute soudaine de la tension artérielle en se tenant
- prise de poids
- lenteur
- tests hépatiques anormaux
- estomac renversé
- bouche sèche
- vertiges
- faiblesse
- douleurs abdominales
- constipation
- mal de gorge
- somnolence
- vertiges
- fatigue
- n / Ausea
- bouche sèche
- prise de poids
- appétit accru
- vomissement
- rythme cardiaque rapide
Lese are not all the possible side effects of Séroquel. For more information ask your healthcare provider or pharmacist.
Appelez votre médecin pour des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
Comment dois-je stocker Seroquel?
- Stockez séroquecteur à température ambiante entre 68 ° F à 77 ° F (20 ° C à 25 ° C).
- Gardez Seroquel et tous les médicaments hors de portée des enfants.
Informations générales sur l'utilisation sûre et efficace de Seroquel Les médicaments sont parfois prescrits à des fins autres que celles énumérées dans un guide de médicaments. N'utilisez pas Seroquel pour une condition pour laquelle il n'a pas été prescrit. Ne donnez pas Seroquel à d'autres personnes même si elles présentent les mêmes symptômes que vous. Cela peut leur faire du mal.
Ce guide de médicaments résume les informations les plus importantes sur Seroquel. Si vous souhaitez plus d'informations, parlez avec votre fournisseur de soins de santé. Vous pouvez demander à votre pharmacien ou fournisseur de soins de santé pour des informations sur Seroquel qui sont écrits pour les professionnels de la santé.
Pour plus d'informations, rendez-vous sur www.seroquet.com ou appelez le 1-800-236-9933.
Quels sont les ingrédients de Seroquel?
Ingrédient actif: quétiapine
Ingrédients inactifs : Povidone Dibasic Dicalcium phosphate dihydrate microcristallin cellulose Sodium Glycolate Glycolate lactose monohydrate de magnésium stéarate hypromellose polyéthylène glycol et dioxyde de titane. Les comprimés de 25 mg contiennent de l'oxyde ferrique rouge et jaune. Les comprimés de 100 mg et 400 mg ne contiennent que de l'oxyde ferrique jaune.