Isovue
Les Informations Présentées Sur Ce Site Ne Constituent Pas Un Avis Médical. Nous Ne Vendons Rien. L'Exactitude De La Traduction N'Est Pas Garantie. Clause De Non-Responsabilité
Résumé
Qu'est-ce que Isovue-M?
L'injection d'isovue-M (iopamidol) est un support de contraste utilisé pour l'administration intrathécale en neuroradiologie, y compris la myélographie (colonne du col de l'utérus thoracique lombaire) et pour l'amélioration du contraste de la cisternographie tomographique calculée (CECT) et de la ventriculographie.
Quels sont les effets secondaires de l'isovue-M?
Isovue
- urticaire
- difficulté à respirer
- gonflement de ton visage lèvres langue ou gorge
- étourdissements sévères
- étourdissement
- gonflement
- gain de poids rapide
- peu ou pas d'uriner
- respiration sifflante
- crise d'épilepsie
- gonflement in your neck ou throat (enlarged thyroid )
- fatigue extrême
- peau sec
- Douleur ou raideur articulaire
- douleur musculaire
- faiblesse
- enrouement
- prise de poids
- Sensibilité accrue aux températures froides
- douleur à la poitrine ou pression
- Douleur se propageant à votre mâchoire ou à votre épaule
- nausée
- transpiration
- toux soudaine
- essoufflement
- cracher du sang
- Engourdissement soudain ou faiblesse (surtout d'un côté du corps)
- Maux de tête soudains graves
- discours lié et
- Problèmes de vision ou d'équilibre
Obtenez de l'aide médicale immédiatement si vous présentez l'un des symptômes énumérés ci-dessus.
Les effets secondaires courants de l'isovue-M comprennent:
- mal de tête
- nausée
- vomissement
- Douleur musculo-squelettique (pattes du cou arrière)
- pression artérielle basse ( hypotension )
- douleur et sensation de brûlure
- se sentir chaud et
- bouffées de chaleur .
Cherchez des soins médicaux ou appelez le 911 à la fois si vous avez les effets secondaires graves suivants:
- Des symptômes oculaires graves tels que la perte de vision soudaine floue du tunnel de vision de la vision de la vision des yeux ou de l'enflure ou de voir des halos autour des lumières;
- Symptômes cardiaques graves tels que les battements cardiaques rapides ou battants; flotter dans votre poitrine; essoufflement; et des étourdissements soudains étourdisseurs ou s'évanouissant;
- Maux de tête sévères Confusion Slurred Speech Bras ou Ligne Proulitude Trouble de la merde Perte de coordination Sentiment des muscles très rigides très rigides Fièvre élevée Propice ou des tremblements.
Ce document ne contient pas tous les effets secondaires possibles et d'autres peuvent survenir. Vérifiez auprès de votre médecin des informations supplémentaires sur les effets secondaires.
Dosage pour isovue-m
La plage de dose pour adultes habituelle pour l'isovue-M est de 2000 à 3000 mg d'iode.
Quelles substances ou suppléments de médicaments interagissent avec Isovue-M?
Aucun autre produit pharmaceutique ou corticostéroïde ne doit être utilisé avec Isovue-M. La prudence doit être prise si vous avez augmenté la pression intracrânienne ou la suspicion de tumeur intracrânienne abcès ou hématome avoir des antécédents de trouble convulsif sévère maladie cardiovasculaire chronique alcoolisme sclérose en plaques ou sont âgés.
Isovue-M pendant la grossesse ou l'allaitement
Isovue-M ne doit être utilisé que pendant la grossesse s'il est clairement nécessaire. La prudence doit être utilisée si vous allaitez.
Informations Complémentaires
Notre Isovue-M (iopamidol) Effets Drug Center Drug offre une vue complète des informations sur les médicaments disponibles sur les effets secondaires potentiels lors de la prise de ce médicament.
Informations sur les médicaments de la FDA
- Description de la drogue
- Indications
- Dosage
- Effets secondaires
- Avertissements
- Précautions
- Surdosage
- Pharmacologie clinique
- Guide des médicaments
Description de l'isovue-m
Les formulations d'isovue (injection de lopamidol) sont des solutions aqueuses stériles et non pyrogéniques stables pour l'administration intravasculaire.
Chaque ML d'Isovue-200 (injection de lopamidol 41%) fournit 408 mg d'iopamidol avec 1 mg de trométhamine et 0,26 mg de disodium en calcium en éétté. La solution contient environ 0,029 mg (0,001 meq) de sodium et 200 mg d'iode lié de manière organique par ml.
Chaque ML d'Isovue-250 (injection de lopamidol 51%) fournit 510 mg d'iopamidol avec 1 mg de trométhamine et 0. 33 mg de disodium en calcium en ététate. La solution contient environ 0,036 mg (0,002 mEq) de sodium et 250 mg d'iode lié de manière organique par ml.
Chaque ML d'Isovue-300 (injection de lopamidol 61%) fournit 612 mg d'iopamidol avec 1 mg de trométhamine et 0,39 mg de disodium en calcium en éétate. La solution contient environ 0,043 mg (0,002 mEq) de sodium et 300 mg d'iode lié de manière organique par ml.
Chaque ML d'Isovue-370 (injection de lopamidol 76%) fournit 755 mg d'iopamidol avec 1 mg de trométhamine et 0,48 mg de disodium de calcium en éétate. La solution contient environ 0,053 mg (0,002 mEq) de sodium et 370 mg d'iode lié de manière organique par ml.
Le pH des milieux de contraste d'isovue a été ajusté à 6,5-7,5 avec de l'acide chlorhydrique et / ou de l'hydroxyde de sodium. Des données physicochimiques pertinentes sont notées ci-dessous. L'isovue (injection de lopamidol) est hypertonique par rapport au plasma et au liquide céphalorachidien (environ 285 et 301 mosm / kg d'eau respectivement).
| Iopamidol | ||||
| Paramètre | 41% | 51% | 61% | 76% |
| Concentration (mgl / ml) | 200 | 250 | 300 | 370 |
| Osmolalité à 37 ° C (MOSM / kg d'eau) | 413 | 524 | 616 | 796 |
| Viscosité (CP) à 37 ° C | 2.0 | 3.0 | 4.7 | 9.4 |
| @ 20 ° C | 3.3 | 5.1 | 8.8 | 20.9 |
| Gravité spécifique à 37 ° C | 1.227 | 1.281 | 1.339 | 1.405 |
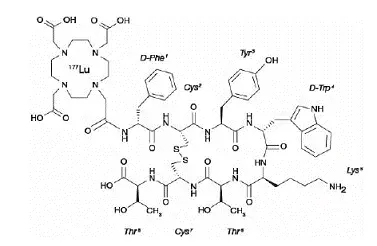
Le lopamidol est désigné chimiquement comme (S) -NN'-BIS [2-hydroxy-1- (hydroxyméthyl) -éthyl] 246-triiodo-5-lactamidoisophthalamide. Formule structurelle:
 |
Utilisations pour Isovue-M
L'isovue (injection d'iopamidol) est indiquée pour l'angiographie dans tout le système cardiovasculaire chez les adultes, notamment l'artériographie coronaire et la ventriculographie cérébrale et périphérique et la veine périphérique (phlébographie) et les patients pédiatriques pour les patients pédiatriques pour l'angiocardiographie; ou pour une utilisation intraveineuse chez l'adulte et pédiatrique pour l'imagerie tomographique (CT) de la tête et du corps (voir ci-dessous).
Imagerie de tête CT
Isovue peut être utilisée pour affiner la précision diagnostique dans les zones du cerveau qui n'auraient pas été autrement visualisées de manière satisfaisante.
Tumeur
L'isovue peut être utile pour étudier la présence et l'étendue de certaines tumeurs malignes telles que: des gliomes, notamment des gliomes malins glioblastomes astrocytomes oligodendrogliomes et gangliomes épendymomas médulloblastomes méningiomes neuromas neuromas picitomes pitutatics craniopharyngiomasgiomas. L'utilité de l'amélioration du contraste pour l'étude de l'espace rétrobulbaire et en cas de gliome de bas grade ou infiltrant n'a pas été démontrée.
Dans les lésions calcifiées, il y a moins de probabilité d'amélioration. Après la thérapie, les tumeurs peuvent montrer une amélioration diminuée ou aucune amélioration.
L'opacification du vermis inférieur suivant l'administration de médias de contraste a entraîné un diagnostic faussement positif dans un certain nombre d'études autrement normales.
Conditions non néoplasiques
L'isovue peut être bénéfique dans l'amélioration de l'image des lésions non néoplasiques. Les infarctus cérébraux de début récent peuvent être mieux visualisés avec l'amélioration du contraste tandis que certains infarctus sont obscurcis si des milieux de contraste sont utilisés. L'utilisation de milieux de contraste iodé entraîne une amélioration du contraste dans environ 60% des infarctus cérébraux étudiés de une à quatre semaines à compter de l'apparition des symptômes.
Les sites d'infection active peuvent également être améliorés à la suite de l'administration de médias de contraste. Les malformations et anévrismes artérioveineux montreront une amélioration du contraste. Pour ces lésions vasculaires, l'amélioration dépend probablement de la teneur en iode de la piscine sanguine en circulation.
Les hématomes et les saignements intraparenchymateux démontrent rarement toute amélioration du contraste. Cependant, dans les cas de caillot intraparenchymateux pour lequel il n'y a pas d'explication clinique évidente, l'administration de médias de contraste peut être utile pour exclure la possibilité d'une malformation artérioveineuse associée.
Imagerie corporelle CT
L'isovue (injection d'iopamidol) peut être utilisée pour l'amélioration de l'isovue tomographique calculée (injection d'iopamidol) peut être utilisée pour l'amélioration des images tomographiques calculées pour la détection et l'évaluation des lésions dans le pelvis de cavité abdominale de la foie dans l'espace rétro-enrénitonéal.
L'amélioration de la tomodensitométrie avec Isovue peut être avantageuse à établir des diagnostics de certaines lésions dans ces sites avec une plus grande assurance que possible avec CT seul et à fournir des caractéristiques supplémentaires des lésions (par exemple, la délimitation de l'abcès hépatique avant le drainage percutané). Dans d'autres cas, l'agent de contraste peut permettre la visualisation des lésions non observées avec CT seule (par exemple l'extension tumorale) ou peut aider à définir des lésions suspectes observées avec une TDM non améliorée (par exemple le kyste pancréatique).
L'amélioration du contraste semble être la plus grande dans les 60 à 90 secondes après l'administration du bolus d'agent de contraste. Par conséquent, l'utilisation d'une technique de balayage continu (tomodensitométrie dynamique) peut améliorer l'amélioration et l'évaluation diagnostique de la tumeur et d'autres lésions telles qu'un abcès révélant parfois une maladie insoupçonnée ou plus étendue. Par exemple, un kyste peut être distingué d'une lésion solide vascularisée lorsque des scans pré-contrastes et améliorés sont comparés; La masse non perfusée montre une absorption des rayons X inchangée (numéro CT). Une lésion vascularisée est caractérisée par une augmentation du nombre de TDM dans les quelques minutes après un bolus d'agent de contraste intravasculaire; Il peut être malin bénin ou tissu normal, mais ne serait probablement pas un hématome kyste ou une autre lésion non vasculaire.
Étant donné que le balayage non amélioré peut fournir des informations diagnostiques adéquates chez le patient individuel, la décision d'employer une amélioration du contraste qui peut être associée au risque et à une exposition accrue aux radiations devrait être basée sur une évaluation minutieuse des autres résultats cliniques radiologiques et non améliorés.
Dosage pour isovue-m
Général
Les médicaments parentéraux doivent être inspectés visuellement pour les particules et la décoloration avant l'administration chaque fois que la solution et le permis de conteneur. Les solutions d'iopamidol ne doivent être utilisées que si elles sont claires et dans la gamme normale incolore à jaune pâle. Jeter tout produit qui montre des signes de cristallisation ou de dommages au système de clôture de récipient qui comprend le bouchon et / ou le serrage du récipient en verre.
Il est souhaitable que les solutions d'agents diagnostiques radiopaques à usage intravasculaire soient à température corporelle lorsqu'ils sont injectés. Les techniques stériles doivent être utilisées avec toute injection intravasculaire.
Le transfert d'Isovue à partir du conteneur de package en vrac Isovue Imaging doit être effectué en utilisant la technique aseptique. La fermeture du package en vrac d'imagerie ne peut être pénétrée qu'une seule fois avec un composant stérile approprié du système de gestion de contraste du système de contraste de contraste automatisé ou de l'ensemble de transfert de support de contraste approuvé ou effacé pour être utilisé avec ce package en vrac d'imagerie.
Les patients doivent être bien hydratés avant et suivre l'administration d'isovue (injection d'iopamidol).
Comme pour tous les agents de contraste radiopaque, seuls la dose la plus faible d'isovue nécessaire pour obtenir une visualisation adéquate doit être utilisée. Une dose plus faible réduit la possibilité d'une réaction indésirable. La plupart des procédures ne nécessitent pas d'utilisation d'une dose maximale ni de la concentration d'isovue la plus élevée disponible; La combinaison de la dose et de la concentration d'isovue à utiliser doit être soigneusement individualisée et des facteurs tels que la taille du corps de l'âge du navire et son débit sanguin de la pathologie et le degré et l'étendue de l'opacification Structure requis ou de la zone à examiner les processus pathologiques affectant le patient et l'équipement et la technique à utiliser doivent être considérés.
Artériographie cérébrale
L'isovue-300 (injection d'iopamidol 300 mg d'iode / ml) doit être utilisé. L'injection individuelle habituelle par ponction carotidienne ou cathétérisme transfémoral est de 8 à 12 ml avec des doses multiples totales jusqu'à 90 ml.
Artériographie périphérique
Isovue-300 offre généralement une visualisation adéquate. Pour l'injection dans l'artère fémorale ou l'artère sous-clavière, 5 à 40 ml peuvent être utilisées; Pour l'injection dans l'aorte pour un ruissellement distal, 25 à 50 ml peuvent être utilisés. Des doses jusqu'à un total de 250 ml d'Isovue-300 ont été administrées pendant l'artériographie périphérique.
Venographie périphérique (phlébographie)
Isovue-300 doit être utilisé. La dose habituelle est de 15 ml à 100 ml par membre inférieur.
Qu'est-ce que Meloxicam a dedans
La dose totale combinée pour les injections multiples ne doit pas dépasser 230 ml.
Artériographie et aortographie viscérale sélective
L'isovue-370 (injection d'iopamidol 370 mg d'iode / ml) doit être utilisé. Des doses allant jusqu'à 50 ml peuvent être nécessaires pour l'injection dans les plus grands vaisseaux tels que l'aorte ou l'artère cœliaque; Des doses allant jusqu'à 10 ml peuvent être nécessaires pour l'injection dans les artères rénales. Les doses plus faibles seront souvent suffisantes. La dose totale combinée pour les injections multiples n'a pas dépassé 225 ml.
Angiocardiographie pédiatrique
Isovue-370 doit être utilisé. L'angiocardiographie pédiatrique peut être effectuée par injection dans une grande veine périphérique ou être une caractérisation directe du cœur. La plage de dose habituelle pour les injections uniques est fournie dans le tableau suivant:
| Injection unique | Gamme de dose habituelle |
| Âge | ml |
| <2 years | 10-15 |
| 2 à 9 ans | 15-30 |
| 10 à 18 ans | 20-50 |
La dose recommandée habituelle pour les injections cumulatives est fournie dans le tableau suivant.
| Injection cumulée | Dose recommandée habituelle |
| Âge | ml |
| <2 years | 40 |
| 2 à 4 ans | 50 |
| 5 à 9 ans | 100 |
| 10 à 18 ans | 125 |
Artériographie coronaire et ventriculographie
Isovue-370 doit être utilisé. La dose habituelle pour les injections sélectives de l'artère coronaire est de 2 à 10 ml. La dose habituelle pour la ventriculographie ou pour l'opacification non sélective de plusieurs artères coronaires après l'injection à la racine aortique est de 25 à 50 ml. La dose totale pour les procédures combinées n'a pas dépassé 200 ml. La surveillance EKG est essentielle.
Tomodensitométrie
CT de la tête
La dose suggérée pour l'isovue-300 est de 100 à 200 ml par administration intraveineuse. L'imagerie peut être effectuée immédiatement après la fin de l'administration.
CT du corps
La plage de dose adulte habituelle pour l'isovue-300 est de 100 à 200 ml administrée par une perfusion intraveineuse rapide ou une injection de bolus.
Des doses équivalentes d'Isovue-370 basées sur une teneur en iode liée organiquement peuvent également être utilisées.
La dose totale pour l'une ou l'autre procédure CT ne doit pas dépasser 60 grammes d'iode.
Tomodensitométrie pédiatrique
La posologie recommandée pour une utilisation chez les enfants pour une tomodensitométrie améliorée de contraste est de 1,0 ml / kg à 3,0 ml / kg pour l'isovue-300. Il ne devrait pas être nécessaire de dépasser une dose totale de 30 grammes d'iode.
Incompatibilités de médicament
De nombreux agents de contraste radiopaque sont incompatibles in vitro avec quelques antihistaminiques et de nombreux autres médicaments; Par conséquent, aucun autre pharmaceutique ne devrait être admis avec des agents de contraste.
Manipulation de drogues
Les médicaments parentéraux doivent être inspectés visuellement pour les particules et la décoloration avant l'administration chaque fois que la solution et le permis de conteneur. Les solutions d'iopamidol ne doivent être utilisées que si elles sont claires et dans la gamme normale incolore à jaune pâle. Jeter tout produit qui montre des signes de cristallisation ou de dommages au système de clôture de récipient qui comprend le bouchon et / ou le serrage du récipient en verre.
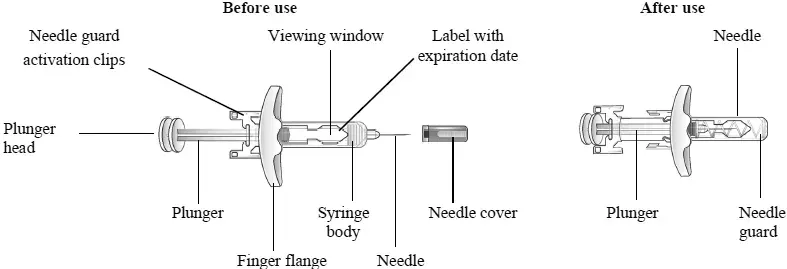
Itinéraire pour une utilisation appropriée du package en vrac d'imagerie Isovue
Le package en vrac d'imagerie Isovue est utilisé pour dispenser plusieurs doses uniques d'injection d'iopamidol pour plusieurs patients utilisant un système de gestion de contraste de contraste de contraste de contraste automatisé ou un ensemble de transfert de supports de contraste approuvé ou effacé pour être utilisé avec cet agent de contraste dans ce package en vrac d'imagerie. Les préparations de l'injection de chlorure de sodium à 0,9% USP avec un port stérile pour un ensemble d'administration intraveineuse doivent être utilisées avec le paquet en vrac d'imagerie isovue et les systèmes d'injection de contraste automatisés ou les systèmes de gestion de contraste approuvés pour une utilisation avec le package en vrac d'imagerie isovue. Veuillez consulter l'étiquetage des médicaments et des appareils pour plus d'informations sur les appareils indiqués pour une utilisation avec ce package en vrac d'imagerie et les techniques pour assurer une utilisation sûre.
- Le package en vrac d'imagerie Isovue ne doit être utilisé que dans une pièce désignée pour les procédures radiologiques qui impliquent l'administration intravasculaire d'un agent de contraste.
- Le transfert d'Isovue à partir du package en vrac d'imagerie doit être effectué en utilisant la technique aseptique. Avant de pénétrer la fermeture de conteneurs, la surface du bouchon du conteneur avec 70% d'alcool isopropylique. La fermeture du conteneur ne peut être pénétrée qu'une seule fois avec un composant stérile approprié du système de gestion de contraste de contraste de contraste de contraste de contraste automatisé ou de l'ensemble de transfert de support de contraste approuvé ou effacé pour être utilisé avec ce package en vrac d'imagerie.
- Une fois que le paquet en vrac d'imagerie est perforé, il ne doit pas être retiré de la zone de travail pendant toute la période d'utilisation et la bouteille doit être maintenue en position inversée de telle sorte que le contenu des conteneurs soit en contact continu avec l'ensemble de distribution.
- Un temps d'utilisation maximal de 10 heures à compter de l'entrée de fermeture initiale est autorisé à effectuer un transfert de fluide. Toute injection d'isovue inutilisée doit être jetée 10 heures après la ponction initiale du package en vrac d'imagerie.
- Une fois la fermeture de conteneurs perforée si l'intégrité du package en vrac d'imagerie et que le système de livraison ne peut pas être assuré, mais une supervision continue directe le package en vrac d'imagerie et toutes les jetables associées pour le système de gestion de contraste du système d'injection de contraste automatisé ou l'ensemble de transfert de supports de contraste doivent être rejetés.
- La température de stockage du récipient en vrac d'imagerie isovue après la fermeture de la fermeture ne doit pas dépasser 25 ° C (77 ° F); Cependant, il est souhaitable que le contenu soit réchauffé à la température corporelle avant l'injection.
- Si l'injection de chlorure de sodium à 0,9% est utilisée, préparez le port intraveineux conformément à la section posologique et administration des informations de prescription approuvées du produit.
- Utilisation à dose multiple de 0,9% d'injection de chlorure de sodium USP:
- L'USP à 0,9% de chlorure de sodium ne doit être utilisé que pour fournir des doses multiples à plusieurs patients lorsqu'ils sont utilisés avec un système automatisé d'injection de contraste ou un système de gestion de contraste approuvé ou effacé pour une utilisation à dose multiple d'une injection de chlorure de sodium à 0,9%.
- Le port d'administration intraveineux du récipient de chlorure de sodium ne peut être pénétré qu'une seule fois avec un composant stérile approprié du système de gestion de contraste approuvé pour une utilisation avec le package en vrac d'imagerie isovue en utilisant la technique aseptique. Un temps d'utilisation maximal de 10 heures à compter de l'entrée de fermeture initiale est autorisé à terminer le transfert de fluide. Tout chlorure de sodium inutilisé doit être jeté 10 heures après la ponction initiale du récipient USP à injection de chlorure de sodium à 0,9%. Le conteneur de l'injection de chlorure de sodium à 0,9% doit être utilisé uniquement dans une zone désignée pour les procédures radiologiques qui impliquent l'administration intravasculaire de contraste. Toutes les instructions ci-dessus en c. à travers e. Pour l'imagerie Isovue, un ensemble en vrac doit être suivi pour le conteneur USP d'injection de chlorure de sodium à 0,9%. Broupez l'étiquette saline fournie avec le paquet en vrac d'imagerie isovue sur le récipient USP à injection de chlorure de sodium à 0,9%.
- Utilisation à dose unique de 0,9% d'injection de chlorure de sodium USP: utilisation conformément aux fabricants de prescription d'informations.
Comment fourni
Stockage et manipulation
Isovue-300 (injection d'iopamidol 61%)
Dix packages en vrac d'imagerie de 200 ml ( NDC 0270-1315-45)
Packages en vrac d'imagerie de six 500 ml ( NDC 0270-1315-95)
Isovue-370 (injection d'iopamidol 76%)
Dix packages en vrac d'imagerie de 200 ml ( NDC 0270-1316-45)
Packages en vrac d'imagerie de six 500 ml ( NDC 0270-1316-95)
Stockage
Stocker à 20-25 ° C (68-77 ° F). [Voir USP]. Protéger de la lumière.
Isovue est une marque déposée de Bracco Diagnostics Inc.
Fabriqué par: Bipso GmbH 78224 Singen (Allemagne). Révisé: avril 2023
Combien de temps dure Ambien Cr
Effets secondaires pour Isovue-M
Les effets indésirables suivant l'utilisation de l'iopamidol sont généralement légers à modérés sellimités et transitoires.
En angiocardiographie (597 patients), les effets indésirables avec une incidence estimée de 1 pour cent ou plus sont: bouffées de chaleur 3,4%; Angina pectoralis 3,0%; Flushing 1,8%; Bradycardie 1,3%; hypotension 1,0%; ruches 1,0%.
Dans un essai clinique avec 76 patients pédiatriques subissant une angiocardiographie, 2 effets indésirables (2,6%) tous deux à distance attribués aux milieux de contraste ont été signalés. Les deux patients avaient moins de 2 ans, les deux avaient des maladies cardiaques cyanotiques avec des anomalies ventriculaires droites sous-jacentes et une circulation pulmonaire anormale. Chez un patient, la cyanose préexistante a été transitoirement intensifiée à la suite de l'administration de médias de contraste. Chez le deuxième patient, une diminution de la perfusion périphérique a été intensifiée pendant 24 heures après l'examen. (Voir PRÉCAUTIONS Section pour des informations sur la nature à haut risque de ces patients.)
L'injection intravasculaire de milieux de contraste est fréquemment associée à la sensation de chaleur et de douleur, en particulier dans l'artériographie périphérique et la venographie; La douleur et la chaleur sont moins fréquentes et moins sévères avec l'isovue (injection d'iopamidol) qu'avec l'injection de diatrizoate de méglumine et de diatrizoate de sodium.
Le tableau suivant de l'incidence des réactions est basé sur des études cliniques avec Isovue chez environ 2246 patients.
| Effets indésirables | ||
| Système | > 1% | Incidence globale estimée ≤ 1% |
| Cardiovasculaire | aucun | tachycardie hypotension hypertension ischémie myocardique effondrement circulatoire Dépression du segment S-T bigémines extrasystoles fibrillation ventriculaire Coffre d'angine bradycardie Attaque ischémique transitoire thrombophlebitis |
| Nerveux | Douleur (2,8%) Sensation de brûlure (1,4%) | réaction vasovagale picotements dans les bras grimace malaise |
| Digestif | nausée (1.2%) | vomissement anouexia |
| Respiratoire | aucun | constriction de la gorge Dyspnée œdème pulmonaire |
| Peau et appendices | aucun | éruption cutanée urticaire prurit bouffée |
| Le corps dans son ensemble | bouffées de chaleur (1.5%) | mal de tête fièvre frissons transpiration excessive spasme arrière |
| Sens spéciaux | chaleur (1,1%) | altération de goût congestion nasale troubles visuels |
| Urogénital | aucun | rétention urinaire |
Quel que soit le contraste que l'agent a utilisé l'incidence globale estimée des effets indésirables graves est plus élevé avec artériographie coronaire qu'avec d'autres procédures. Décompensation cardiaque arythmies graves ou ischémie ou infarctus du myocarde ont été signalés avec isovue et peuvent se produire pendant artériographie coronaireet left ventriculography .
Après les injections coronariennes et ventriculaires, certains changements électrocardiographiques (augmentation de la QTC a augmenté l'amplitude des ondes R-R) et certains changements hémodynamiques (diminution de la pression systolique) se sont produits moins fréquemment avec l'isovue (injection d'iopamidol) qu'avec l'injection de diatrizoate de méglumine et de diatrizoate de sodium; Une augmentation du LVEDP s'est produite moins fréquemment après les injections ventriculaires d'iopamidol.
Dans aortographie the risks of procedures also include injury to the aorta and neighboring organs pleural puncture renal damage including infarction and acute tabular necrosis with oliguria and anuria accidental selective filling of the right renal artery during the translumbar procedure in the presence of pre-existing renal disease retroperitoneal hemorrhage from the translumbar approach and spinal cord injury and pathology associated with the syndrome of transverse myélite.
Les effets indésirables suivants ont été signalés pour l'iopamidol:
Cardiovasculaire: arythmie spasmes artériels rinçage de vasodilatation de la poitrine
Nerveux Système: Confusion Paresthésie Dizzucies Temporary Cortical Belness Temporary Amnésie Convulsions Paralysie Coma;
Respiratoire: Augmentation de la toux éternuement de l'asthme de l'asthme de l'œdème laryngé rhinite de résistance à la poitrine;
Peau et appendices: Douleur du site d'injection généralement dû à l'extravasation et / ou à une pâleur de gonflement érythémateuse œdème périorbital œdème facial;
Urogénital: Hématurie de la douleur;
Sens spéciaux: conjonctivite de déviation des yeux démangeaisons aqueux;
Musculo-squelette: Spasme musculaire Mouvement des jambes involontaires;
Corps dans son ensemble: Tremors malaise réaction anaphylactoïde (caractérisé par des symptômes respiratoires et cutanés cardiovasculaires)
Digestif: Retching sévère et étouffement des crampes abdominales. Certains d'entre eux peuvent survenir en conséquence de la procédure. D'autres réactions peuvent également se produire avec l'utilisation de tout agent de contraste en raison du danger procédural;
Il s'agit notamment de l'hémorragie ou des pseudo-anévrismes au site de ponction par la paralysie du plexus brachial après l'injection d'artère axillaire infarctus du myocarde de la douleur thoracique et les changements transitoires dans les tests de chimie hépatorrénale. Déplacement de la thrombose artérielle des plaques artérielles Dissection de thrombose veineuse des vaisseaux coronaires et de l'arrêt des sinus transitoires sont de rares complications.
Général Effets indésirables To Contrast Media
Les réactions connues pour se produire avec l'administration parentérale d'agents de contraste ionique iodé (voir la liste ci-dessous) sont possibles avec tout agent non ionique. Environ 95% des effets indésirables accompagnant l'utilisation d'autres agents de contraste administrés par voie intravasculaire sont légers à modérés en degré. Cependant, les réactions et les décès potentiellement mortels d'origine cardiovasculaire se sont produits. Les incidences de décès rapportées par l'administration d'autres milieux de contraste iodés vont de 6,6 pour 1 million (0,00066%) à 1 sur 10000 patients (0,01%). La plupart des décès surviennent pendant l'injection ou 5 à 10 minutes plus tard, la principale caractéristique étant un arrêt cardiaque avec une maladie cardiovasculaire comme principal facteur aggravant. Des rapports isolés d'effondrement hypotensif et choc se trouvent dans la littérature. L'incidence du choc est estimée à 1 des patients sur 20000 (0,005%).
Les réactions indésirables au milieu de contraste injectable se répartissent en deux catégories: les réactions chimiotoxiques et les réactions idiosyncratiques. Les réactions chimiotoxiques résultent des propriétés physicochimiques du milieu de contraste la dose et la vitesse d'injection. Toutes les perturbations hémodynamiques et les blessures aux organes ou aux navires perfusés par le milieu de contraste sont inclus dans cette catégorie. Les réactions idiosyncratiques comprennent toutes les autres réactions. Ils surviennent plus fréquemment chez les patients âgés de 20 à 40 ans. Les réactions idiosyncratiques peuvent ou non dépendre de la quantité de médicament injecté à la vitesse d'injection du mode d'injection et de la procédure radiographique. Les réactions idiosyncratiques sont subdivisées en intermédiaire mineur et sévère. Les réactions mineures sont auto-limitées et de courte durée; Les réactions graves sont mortelles et le traitement est urgent et obligatoire.
L'incidence signalée des effets indésirables aux milieux de contraste chez les patients ayant des antécédents allergie est deux fois cela pour la population générale. Les patients ayant des antécédents de réactions précédentes à un milieu de contraste sont trois fois plus sensibles que les autres patients. Cependant, la sensibilité aux milieux de contraste ne semble pas augmenter avec des examens répétés. La plupart des effets indésirables aux agents de contraste intravasculaire apparaissent dans un à trois minutes après le début de l'injection, mais des réactions retardées peuvent se produire. Les réactions retardées impliquant généralement la peau peuvent se produire inhabituellement dans les 2 à 3 jours (intervalle 1 à 7 jours) après l'administration du contraste (voir PRÉCAUTIONS - Général ).
Les réactions allergiques retardées sont plus fréquentes chez les patients traités par des immunostimulants tels que l'interleukine-2.
Dans addition to the adverse drug reactions repouted fou iopamidol the following additional adverse reactions have been repouted with the use of other intravascular contrast agents et are possible with the use of any water-soluble iodinated contrast agent:
Cardiovasculaire: hématomes cérébraux Petechiae ;
Hématologique: neutropénie ;
Urogénital: néphrose osmotique des cellules tubulaires proximales insuffisance rénale;
Sens spéciaux: chimiose conjonctivale avec infection.
Endocrine: hypothyroïdie de l'hyperthyroïdie;
Troubles de la peau et des tissus sous-cutanés: Nécrose cutanée; Les réactions vont de légères (par exemple, érythème érythème uticaria et décoloration cutanée) à sévère: [par ex. Syndrome de Stevens-Johnson et nécrolyse épidermique toxique (SJS / Ten) mignonnes de pustulose exanthémateuse généralisée (AGEP) et réaction médicamenteuse avec éosinophilie et symptômes systémiques (robe)].
Interactions médicamenteuses pour l'isovue-M
Une toxicité rénale a été signalée chez quelques patients atteints de dysfonctionnement hépatique qui ont reçu des agents cholécystographiques oraux suivis d'agents de contraste intravasculaire. L'administration d'agents intravasculaires doit donc être reportée chez tout patient atteint d'un trouble hépatique ou biliaire connu ou suspecté qui a récemment reçu un agent de contraste cholécystographique.
D'autres drogues ne doivent pas être mélangées avec de l'iopamidol.
Avertissements fou Isovue-M
Événements indésirables sévères LNADADVERTENT ADMINORTION INTRATHÉQUE DES EFFACTES SÉCURITÉS ont été signalés en raison de l'administration intrathécale par inadvertance de milieux de contraste iodés qui ne sont pas indiqués pour une utilisation intrathécale.
Ces effets indésirables graves comprennent: les convulsions de la mort hémorragie cérébrale paralysie du coma arachnoïdite d'insuffisance rénale aiguë des crises d'arrêt cardiaque de rhabdomyolyse hyperthermie et œdème cérébral. Une attention particulière doit être accordée pour s'assurer que ce produit médicamenteux n'est pas administré par inadvertance intrathécalement.
Général
Les milieux de contraste iodés non ioniques inhibent la coagulation sanguine in vitro Moins de contrastes ioniques. La coagulation a été signalée lorsque le sang reste en contact avec des seringues contenant des milieux de contraste non ionique.
Des événements thromboemboliques rarement mortels provoquant un infarctus du myocarde et un AVC ont été signalés lors de procédures angiographiques avec des milieux de contraste ionique et non ionique. Par conséquent, une technique d'administration intravasculaire méticuleuse est nécessaire en particulier pendant les procédures angiographiques pour minimiser les événements thromboemboliques. De nombreux facteurs, notamment la durée du cathéter de procédure et le matériel de seringue sous-jacent, l'état pathologique et les médicaments concomitants peuvent contribuer au développement d'événements thromboemboliques. Pour ces raisons, des techniques angiographiques méticuleuses sont recommandées, notamment une attention particulière à l'utilisation de la manipulation du fil de guidage et du cathéter des systèmes de collecteur et / ou des buts à trois voies de cathéter fréquents avec des solutions salines héparinites et une minimisation de la durée de la procédure. Il a été rapporté que l'utilisation de seringues en plastique à la place des seringues en verre diminue mais n'éliminerait pas la probabilité de in vitro coagulation.
La prudence doit être exercée chez les patients atteints de fonction rénale gravement altérée, celles atteintes d'une maladie rénale et hépatique combinée ou de l'anurie, en particulier lorsque des doses plus importantes sont administrées.
Les agents de contraste diagnostique radiopaque sont potentiellement dangereux chez les patients atteints de myélome multiple ou autre paraprotéinémie, en particulier chez les personnes atteintes d'anurie thérapeutiquement résistante. Le myélome se produit le plus souvent chez les personnes de plus de 40 ans. Bien que ni l'agent de contraste ni la déshydratation ne se soient révélés séparément comme la cause de l'anurie chez les patients myélomateux, il a été supposé que la combinaison des deux peut être causale. Le risque chez les patients myélomateux n'est pas une contre-indication; Cependant, des précautions particulières sont nécessaires.
Les milieux de contraste peuvent favoriser la faucille chez les personnes homozygotes pour la drépanocytose lorsqu'ils sont injectés par voie intraveineuse ou par voie intra-artérielle.
L'administration de matériaux radiopaque à des patients connus ou suspectés d'avoir du phéochromocytome doit être effectué avec une extrême prudence. Si, de l'avis du médecin, les avantages possibles de ces procédures l'emportent sur les risques considérés, les procédures peuvent être effectuées; Cependant, la quantité de milieu radiopaque injecté doit être maintenue au minimum absolu. La pression artérielle doit être évaluée tout au long de la procédure et les mesures de traitement d'une crise hypertensive doivent être disponibles. Ces patients doivent être surveillés de très près pendant les procédures améliorées de contraste.
Les rapports de tempête thyroïdienne après l'utilisation d'agents diagnostiques radiopaques iodés chez les patients atteints d'hyperthyroïdie ou avec un nodule thyroïdien fonctionnant de manière autonome suggèrent que ce risque supplémentaire soit évalué chez ces patients avant l'utilisation de tout milieu de contraste.
Dysfonctionnement thyroïdien chez les patients pédiatriques de 0 à 3 ans
Une dysfonction thyroïdienne caractérisée par une hypothyroïdie ou une suppression thyroïdienne transitoire a été signalée après une exposition unique et des expositions multiples aux milieux de contraste iodé chez les patients pédiatriques de 0 à 3 ans.
Âge plus jeune, très faible poids de naissance prématurité sous-jacente aux conditions médicales affectant l'admission à la fonction thyroïdienne aux unités de soins intensifs néonatals ou pédiatriques et aux conditions cardiaques congénitales est associée à un risque accru d'hypothyroïdie après l'exposition à l'ICM. Les patients pédiatriques atteints de conditions cardiaques congénitales peuvent être les plus à risque étant donné qu'ils ont souvent besoin de doses élevées de contraste pendant les procédures cardiaques invasives.
Une thyroïde sous-active au début de la vie peut être nocive pour le développement cognitif et neurologique et peut nécessiter une hormonothérapie de remplacement des hormones thyroïdiennes. Après exposition à l'ICM, individualiser la surveillance de la fonction thyroïdienne en fonction des facteurs de risque sous-jacents, en particulier dans les nouveau-nés à terme et prématurés.
Réactions indésirables cutanées sévères
Les effets indésirables cutanés sévères (cicatriciel) peuvent se développer de 1 heure à plusieurs semaines après l'administration d'agent de contraste intravasculaire. Ces réactions incluent le syndrome de Stevens-Johnson et la nécrolyse épidermique toxique (SJS / dix) de la pustulose exanthémateuse généralisée aiguë (AGEP) et la réaction médicamenteuse avec l'éosinophilie et les symptômes systémiques (robe). La gravité de la réaction peut augmenter et le temps à l'apparition peut diminuer avec l'administration répétée de l'agent de contraste; Les médicaments prophylactiques ne peuvent pas empêcher ou atténuer les effets indésirables cutanés graves. Évitez d'administrer l'isovue aux patients ayant des antécédents d'une réaction indésirable cutanée sévère à l'isovue.
Précautions fou Isovue-M
Général
Les procédures de diagnostic qui impliquent l'utilisation de tout agent radiopaque doivent être effectuées sous la direction du personnel avec la formation préalable et avec une connaissance approfondie de la procédure particulière à effectuer. Des installations appropriées devraient être disponibles pour faire face à toute complication de la procédure ainsi que pour le traitement d'urgence de la réaction sévère à l'agent de contraste lui-même. Après l'administration parentérale d'un agent radiopaque, le personnel compétent et les installations d'urgence devraient être disponibles pendant au moins 30 à 60 minutes, car de graves réactions retardées peuvent se produire. Il faut pratiquer une prudence chez les patients hydratants souffrant de conditions sous-jacentes qui peuvent être aggravées par une surcharge fluide telle que insuffisance cardiaque congestive .
La déshydratation préparatoire est dangereuse et peut contribuer à insuffisance rénale aiguë Chez les patients atteints de maladies vasculaires avancées, les patients diabétiques et chez les patients non diabétiques sensibles (souvent des personnes âgées atteintes d'une maladie rénale préexistante). Les patients doivent être bien hydratés avant et suivre l'administration d'iopamidol.
La possibilité d'une réaction comprenant des réactions à l'anaphylactoïde mortel ou cardiovasculaires mortelles potentiellement mortelles doit toujours être envisagée (voir Effets indésirables ).
Les patients à risque accru comprennent ceux ayant des antécédents d'une réaction précédente à un milieu de contraste de patients avec une sensibilité connue à l'iode en soi et aux patients présentant une hypersensibilité clinique connue (ingénierie bronchique et allergies alimentaires). La survenue de réactions idiosyncratiques sévères a provoqué l'utilisation de plusieurs méthodes de prétest. Cependant, le prétest ne peut être invoqué pour prédire les réactions graves et peut elle-même être dangereuse pour le patient. Il est suggéré qu'un antécédent médical approfondi en mettant l'accent sur l'allergie et l'hypersensibilité avant l'injection de tout milieu de contraste peut être plus précis que le prétest dans la prédiction des effets indésirables potentiels. Une histoire positive d'allergies ou d'hypersensibilité ne contrecarne pas arbitrairement l'utilisation d'un agent de contraste lorsqu'une procédure de diagnostic est considérée comme essentielle, mais la prudence doit être exercée. La prémédication avec des antihistaminiques ou des corticostéroïdes pour éviter ou minimiser les réactions allergiques possibles chez ces patients doit être envisagée. Des rapports récents indiquent qu'un tel prétraitement n'empêche pas de graves réactions mortelles mais peut réduire à la fois leur incidence et leur gravité.
Des conditions préexistantes telles que les stimulateurs cardiaques ou les médicaments cardiaques spécifiquement des betablockers peuvent masquer ou modifier les signes ou symptômes d'une réaction d'anaphylactoïde ainsi que le masquage ou la modification de la réponse à des médicaments particuliers utilisés pour le traitement. Par exemple, les bêta-bloquants inhibent une réponse tachycardienne et peuvent entraîner un diagnostic incorrect d'une réaction vasovagale plutôt que d'une réaction d'anaphylactoïde. Une attention particulière à cette possibilité est particulièrement essentielle chez les patients souffrant de réactions gravement mortelles.
Général anesthesia may be indicated in the perfoumance of some procedures in selected patients; however a higher incidence of adverse reactions has been repouted with radiopaque media in anesthetized patients which may be attributable to the inability of the patient to identify untoward symptoms ou to the hypotensive effect of anesthesia which can reduce cardiac output et increase the duration of exposure to the contrast agent.
Même si l'osmolalité de l'iopamidol est faible par rapport aux agents ioniques à base de diatrizoate ou d'iothalamate de concentration d'iode comparable, l'augmentation transitoire potentielle de la charge osmotique circulatoire chez les patients atteints de congestif insuffisance cardiaque nécessite une prudence pendant l'injection. Ces patients doivent être observés pendant plusieurs heures après la procédure pour détecter les perturbations hémodynamiques retardées. Une douleur et un gonflement du site d'injection peuvent se produire. Dans la majorité des cas, cela est dû à l'extravasation du milieu de contraste. Les réactions sont généralement transitoires et se rétablissent sans séquelles. Cependant, l'inflammation et même la nécrose cutanée ont été observées à très rares occasions.
Dans angiographic procedures the possibility of dislodging plaques ou damaging ou perfouating the vessel wall ou inducing vasospasm et ou subsequent ischemic events should be boune in mind during catheter manipulations et contrast medium injection. Test injections to ensure proper catheter placement are suggested.
Artériographie coronaire sélective ne doit être effectué que chez des patients sélectionnés et ceux chez qui les avantages attendus l'emportent sur le risque de procédure. Les risques inhérents à angiocardiographie Chez les patients présentant un emphysème pulmonaire chronique, il faut peser avec la nécessité d'effectuer cette procédure. L'angiographie doit être évitée chaque fois que possible chez les patients atteints d'homocystinurie en raison du risque d'induction de la thrombose et de l'embolie. Voir aussi Usage pédiatrique .
Dans addition to the general precautions previously described special care is required when venography is perfoumed in patients with suspected thrombosis phlebitis severe ischemic disease local infection ou a totally obstructed venous system.
Une extrême prudence lors de l'injection de milieux de contraste est nécessaire pour éviter l'extravasation et la fluoroscopie est recommandée. Ceci est particulièrement important chez les patients atteints d'une maladie artérielle ou veineuse sévère.
Interactions de test de médicament / de laboratoire
Les résultats de PBI et d'études d'absorption d'iode radioactif qui dépendent des estimations d'iode ne refléteront pas avec précision la fonction thyroïdienne jusqu'à 16 jours suivant l'administration de milieux de contraste iodé. Cependant, les tests de fonction thyroïdienne ne dépendent pas des estimations d'iode, par ex. Les tests d'absorption de résine T3 et les tests totaux ou libres de thyroxine (T4) ne sont pas affectés.
Tout test qui pourrait être affecté par des milieux de contraste doit être effectué avant l'administration du support de contraste.
Résultats des tests de laboratoire
Dans vitro Des études avec du sang animal ont montré que de nombreux agents de contraste radio-opaque, notamment l'iopamidol, produisaient une légère dépression de facteurs de coagulation plasmatique, notamment le temps de la thromboplastine partielle et le fibrinogène, ainsi qu'une légère tendance à provoquer des plaquettes et / ou une agrégation de globules rouges (voir (voir l'agrégation des globules rouges ( PRÉCAUTIONS Général ).
Des changements transitoires peuvent se produire dans les cellules rouges et les leucocytes à comptes sériques sériques sériques de la créatinine glutamique oxaloacétique transaminase (SGOT) et de l'acide urique dans l'urine; L'albuminurie transitoire peut se produire.
Ces résultats n'ont pas été associés à des manifestations cliniques.
Carcinogenèse Mutagenèse A trouble de la fertilité
Des études à long terme chez les animaux n'ont pas été réalisées pour évaluer le potentiel cancérigène. Aucune preuve de toxicité génétique n'a été obtenue en in vitro Tests.
Grossesse
Effets tératogènes
Des études de reproduction ont été réalisées chez le rat et les lapins à des doses allant jusqu'à 2,7 et 1,4 fois la dose humaine maximale recommandée (1,48 gi / kg chez un individu de 50 kg) respectivement et n'ont révélé aucune preuve de fertilité ou de préjudice altéré au fœtus due à l'iopamidol. Il n'y a cependant pas d'études adéquates et bien contrôlées chez les femmes enceintes. Étant donné que les études de reproduction animale ne sont pas toujours prédictives de la réponse humaine, ce médicament ne doit être utilisé pendant la grossesse que s'il est clairement nécessaire.
Mères qui allaitent
On ne sait pas si ce médicament est excrété dans le lait maternel. Parce que de nombreux médicaments sont excrétés dans la prudence du lait maternel doivent être exercés lorsque l'iopamidol est administré à une femme allaitée.
Usage pédiatrique
La sécurité et l'efficacité chez les enfants ont été établies dans l'angiocardiographie pédiatrique et la tomodensitométrie (tête et corps). Les patients pédiatriques à risque plus élevé de subir des événements indésirables pendant l'administration du milieu de contraste peuvent inclure ceux qui souffrent d'asthme une sensibilité aux médicaments et / ou aux allergènes cardiaques cyanotiques insuffisance cardiaque congestive une créatinine sérique supérieure à 1,5 mg / dL ou les moins de 12 mois.
Les tests de fonction thyroïdienne indiquant une dysfonction thyroïdienne caractérisée par l'hypothyroïdie ou la suppression transitoire thyroïdienne ont été inhabituellement rapportés après l'administration de médias de contraste iodé chez les patients pédiatriques, y compris les nouveau-nés à terme et prématurés; Certains patients ont été traités pour l'hypothyroïdie. Après exposition à des médias de contraste iodés, individualiser la surveillance de la fonction thyroïdienne chez les patients pédiatriques de 0 à 3 ans en fonction des facteurs de risque sous-jacents, en particulier dans les nouveau-nés à terme et prématurés (voir Avertissements et Effets indésirables ).
Effets secondaires de l'amlodipine de Norvas
Informations sur la surdose pour Isovue-M
Le traitement d'une surdose d'un milieu de contraste radiopaque injectable est dirigé vers le soutien de toutes les fonctions vitales et une institution rapide de thérapie symptomatique.
Contre-indications pour Isovue-M
Aucun.
Pharmacologie clinique fou Isovue-M
Danstravascular injection of a radiopaque diagnostic agent opacifies those vessels in the path of flow of the contrast medium permitting radiographic visualization of the internal structures of the human body until significant hemodilution occurs.
Après l'injection intravasculaire, les agents diagnostiques radiopaques sont immédiatement dilués dans le plasma circulant. Les calculs du volume apparent de distribution à l'état d'équilibre indiquent que l'iopamidol est distribué entre le volume sanguin en circulation et d'autres liquides extracellulaires; Il ne semble pas y avoir de dépôt significatif d'iopamidol dans les tissus. La distribution uniforme de l'iopamidol dans le liquide extracellulaire se reflète par son utilité démontrée dans l'imagerie tomographique calculée de la tête et du corps après l'administration intraveineuse.
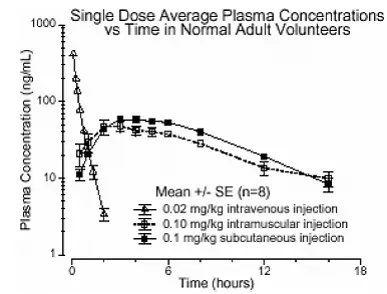
La pharmacocinétique de l'iopamidol administré par voie intraveineuse chez les sujets normaux est conforme à un modèle à deux compartiments ouverts avec élimination du premier ordre (une phase alpha rapide pour la distribution de médicaments et une phase bêta lente pour l'élimination du médicament). La demi-vie du sérum ou du plasma d'élimination est d'environ deux heures; La demi-vie ne dépend pas de la dose. Aucune déiodination ou biotransformation significative du métabolisme ne se produit.
Iopamidol is excreted mainly through the kidneys following intravascular administration. Dans patients with impaired renal function the elimination half-life is prolonged dependent upon the degree of impairment. Dans the absence of renal dysfunction the cumulative urinary excretion fou iopamidol expressed as a percentage of administered intravenous dose is approximately 35 to 40 percent at 60 minutes 80 to 90 percent at 8 hours et 90 percent ou moue in the 72- to 96-hour period after administration. Dans noumal subjects approximately one percent ou less of the administered dose appears in cumulative 72- to 96-hour fecal specimens.
L'isovue peut être visualisée dans le parenchyme rénal dans les 30 à 60 secondes après l'administration intraveineuse rapide. L'opacification des calices et des peaux chez les patients présentant une fonction rénale normale devient apparente en 1 à 3 minutes avec un contraste optimal se produisant entre 5 et 15 minutes. Chez les patients atteints de contraste de troubles rénaux, la visualisation peut être retardée.
Iopamidol displays little tendency to bind to serum ou plasma proteins. No evidence of en vain L'activation du complément a été trouvée chez les sujets normaux. Les études animales indiquent que l'iopamidol ne traverse pas la barrière hémato-encéphalique dans une mesure significative après l'administration intravasculaire.
L'isovue (injection d'iopamidol) améliore l'imagerie du cerveau tomographique calculée par augmentation de l'efficacité radiographique. Le degré d'amélioration de la visualisation de la densité tissulaire est directement lié à la teneur en iode dans une dose administrée; Des taux sanguins d'iode maximaux se produisent immédiatement après une injection rapide de la dose. Ces niveaux tombent rapidement en cinq à dix minutes. Cela peut être pris en compte par la dilution dans les compartiments de liquide vasculaire et extracellulaire qui provoque une baisse active initiale de la concentration plasmatique. L'équilibration avec les compartiments extracellulaires est atteinte dans environ dix minutes par la suite, la chute devient exponentielle. L'amélioration maximale du contraste se produit fréquemment après la maximum des taux d'iode sanguin. Le retard dans l'amélioration du contraste maximal peut varier de cinq à quarante minutes en fonction des niveaux de pic d'iode atteints et du type cellulaire de la lésion. Ce décalage suggère que l'amélioration du contraste radiographique dépend au moins en partie de l'accumulation d'iode dans la lésion et à l'extérieur du pool sanguin bien que le mécanisme par lequel cela se produit ne soit pas clair. L'amélioration radiographique des lésions non contraignantes telles que les malformations artérioveineuses et les anévrismes dépend probablement de la teneur en iode du pool sanguin circulant.
Dans CT head imaging ISOVUE (Iopamidol Dansjection) does not accumulate in noumal brain tissue due to the presence of the blood-brain barrier. The increase in x-ray absouption in noumal brain is due to the presence of contrast agent within the blood pool. A break in the blood-brain barrier such as occurs in malignant tumous of the brain allows the accumulation of the contrast medium within the interstitial tissue of the tumou. Adjacent noumal brain tissue does not contain the contrast medium.
Dans nonneural tissues (during computed tomography of the body) iopamidol diffuses rapidly from the vascular into the extravascular space. Danscrease in x-ray absouption is related to blood flow concentration of the contrast medium et extraction of the contrast medium by interstitial tissue of tumous since no barrier exists. Contrast enhancement is thus due to the relative differences in extravascular diffusion between noumal et abnoumal tissue quite different from that in the brain.
La pharmacocinétique de l'iopamidol dans le tissu normal et anormal s'est avérée variable. L'amélioration du contraste semble être la plus grande peu de temps après l'administration du milieu de contraste et après l'administration intra-artérielle plutôt que intraveineuse. Ainsi, la plus grande amélioration peut être détectée par une série de numérisations consécutives de deux à trois secondes réalisées juste après l'injection (dans les 30 à 90 secondes), c'est-à-dire l'imagerie tomographique calculée dynamique.
Informations sur les patients pour Isovue-M
Les patients recevant des agents diagnostiques radiopaques injectables doivent être invités à:
- Dansfoum your physician if you are pregnant.
- Dansfoum your physician if you are diabetic ou if you have multiple myeloma pheochromocytoma homozygous sickle cell disease ou known thyroid disouder (see Avertissements ).
- Dansfoum your physician if you are allergic to any drugs food ou if you had any reactions to previous injections of substances used fou x-ray procedures (see PRÉCAUTIONS - Général ).
- Dansfoum your physician about any other medications you are currently taking including nonprescription drugs befoue you have this procedure.
- Conseiller aux patients d'informer leur médecin s'ils développent une éruption cutanée après avoir reçu une isovue.
- Conseiller les parents / soignants sur le risque de développer un dysfonctionnement thyroïdien après l'administration d'Isovue. Conseiller les parents / soignants sur le moment de consulter des soins médicaux pour leur enfant pour surveiller la fonction thyroïdienne (voir Avertissements ).