Wellbutrin SR
Les Informations Présentées Sur Ce Site Ne Constituent Pas Un Avis Médical. Nous Ne Vendons Rien. L'Exactitude De La Traduction N'Est Pas Garantie. Clause De Non-Responsabilité
Résumé
Qu'est-ce que Wellbutrin SR?
Welbutrin SR (chlorhydrate de bupropion) est un antidépresseur utilisé pour traiter les troubles dépressifs majeurs et le trouble affectif saisonnière. Au moins une marque de bupropion (Zyban) est utilisée pour aider les gens à arrêter de fumer en réduisant les envies et autres effets de sevrage. Wellbutrin SR est disponible en générique formulaire.
Quels sont les effets secondaires de Wellbutrin SR?
Les effets secondaires courants de Wellbutrin SR comprennent:
- bouche sèche
- mal de gorge
- nausée
- vomissement
- Douleurs d'estomac / abdominal
- bouffée
- mal de tête
- Modifications de l'appétit
- perte de poids ou gain
- constipation
- Difficulté à dormir
- Augmentation de la transpiration
- Augmentation de la miction
- Taste étrange dans la bouche
- douleur musculaire
- douleurs conjointes
- vertiges
- démangeaison
- éruption cutanée
- sonner dans vos oreilles
- Perte d'intérêt pour le sexe
- tremblant (tremblement) ou
- Vision floue.
Welbutrin SR may cause serious side effects including:
- Changements d'humeur ou de comportement
- anxiété
- dépression
- crises de panique
- Difficulté à dormir
- sentiments d'être impulsif irritable agité hostile agressif agressif hyperactif ou plus déprimé
- Pensées de suicide
- Convulsions (convulsions)
- confusion
- changements inhabituels d'humeur ou de comportement
- vision floue
- vision du tunnel
- Douleurs oculaires ou gonflement
- voir des halos autour des lumières
- Roigments cardiaques rapides ou irréguliers
- pensées de course
- comportement téméraire
- Se sentir extrêmement heureux ou irritable
- parler plus que d'habitude
- Problèmes graves de sommeil
Obtenez de l'aide médicale immédiatement si vous présentez l'un des symptômes énumérés ci-dessus.
Cherchez des soins médicaux ou appelez le 911 à la fois si vous avez les effets secondaires graves suivants:
- Des symptômes oculaires graves tels que la perte de vision soudaine floue du tunnel de vision de la vision de la vision des yeux ou de l'enflure ou de voir des halos autour des lumières;
- Symptômes cardiaques graves tels que les battements cardiaques rapides ou battants; flotter dans votre poitrine; essoufflement; Et des étourdissements soudains étourdissement ou s'évanouir;
- Maux de tête sévères Confusion Slurred Speech Bras ou Ligne Proulitude Trouble de la merde Perte de coordination Sentiment des muscles très rigides très rigides Fièvre élevée Propice ou des tremblements.
Ce document ne contient pas tous les effets secondaires possibles et d'autres peuvent survenir. Vérifiez auprès de votre médecin des informations supplémentaires sur les effets secondaires.
Dosage pour Wellbutrin SR
La dose habituelle des adultes pour Wellbutrin SR est de 300 mg / jour donnée à 150 mg deux fois par jour. L'effet antidépresseur complet peut ne pas être évident avant 4 semaines de traitement ou plus.
Quelles substances ou suppléments de médicaments interagissent avec Wellbutrin SR?
Welbutrin SR can interact with many medications including cancer medicine heart rhythm medication blood pressure medication other antidepressants psychiatric medication antihistamines asthma medications or bronchodilators birth control pills hormone replacement vessie / médicaments urinaires Antibiotiques Pilules de régime stimulants Médicaments de TDAH Insuline ou diabète médicaments pris par voie orale des nausées / vomissements / médicaments contre le mala Maladie de Parkinson Syndrome de jambe agitée ou médicament tumoral de la glande hypophysaire utilisée pour prévenir la transplantation d'organe rejet de narcotiques sédatifs stéroïdes théophylline ou ulcères / médicaments intestinaux irritables. Dites à votre médecin tous les médicaments que vous prenez.
Welbutrin SR During Grossesse and Breastfeeding
Welbutrin SR should be used only when prescribed during pregnancy. Infrequently newborns whose mothers have used certain antidepressants during the last 3 months of pregnancy may develop symptoms including persistent feeding or breathing difficulties jitteriness seizures or constant crying. Report symptoms to a doctor. This drug passes into breast milk and may have undesirable effects on a nursing infant. Consult your doctor before breastfeeding.
Informations Complémentaires
Notre centre de médicaments sur les effets secondaires de Wellbutrin SR (Bupropion Hydrochloride) offre une vue complète des informations sur les médicaments disponibles sur les effets secondaires potentiels lors de la prise de ce médicament.
Informations sur les médicaments de la FDA
- Description de la drogue
- Indications
- Effets secondaires
- Interactions médicamenteuses
- Avertissements
- Surdosage
- Contre-indications
- Pharmacologie clinique
- Guide des médicaments
AVERTISSEMENT
Pensées et comportements suicidaires; Et réactions neuropsychiatriques
Suicidalité et médicaments antidépresseurs
Les antidépresseurs ont augmenté le risque de pensées suicidaires et de comportement chez les enfants adolescents et jeunes adultes dans les essais à court terme. Ces essais n'ont pas montré une augmentation du risque de pensées suicidaires et de comportements avec une utilisation d'antidépresseurs chez les sujets de plus de 24 ans; Il y a eu une réduction du risque avec l'utilisation d'antidépresseurs chez les sujets âgés de 65 ans et plus [voir avertissements et PRÉCAUTIONS ].
Chez les patients de tous âges, qui sont lancés sur un traitement antidépresseur, surveillent étroitement pour l'aggravation et pour l'émergence de pensées et de comportements suicidaires. Conseiller les familles et les soignants de la nécessité d'une observation et d'une communication étroites avec le prescripteur [voir avertissements et PRÉCAUTIONS ].
Réactions neuropsychiatriques chez les patients prenant du bupropion pour l'abandon du tabac
De graves réactions neuropsychiatriques se sont produites chez les patients prenant du bupropion pour l'abandon du tabac [voir avertissements et PRÉCAUTIONS ]. The majority of these reactions occurred during bupropion treatment but some occurred in the context of discontinuing treatment. In many cases a causal relations hip to bupropion treatment is not certain because humeur déprimée may be a symptom of nicotine withdrawal. However some of the cases occurred in patients taking bupropion who continued to smoke. Although WELLBUTRIN® SR is not approved for smoking cessation observe all patients for neuropsychiatric reactions. Instruct the patient to contact a healthcare provider if such reactions occur [see AVERTISSEMENTS AND PRÉCAUTIONS ].
Description de Wellbutrin SR
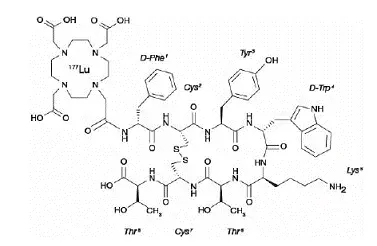
WELLBUTRIN SR (bupropion hydrochloride) an antidepressant of the aminoketone class is chemically unrelated to tricyclic tetracyclic selective serotonin re-uptake inhibitor or other known antidepressant agents. Its structure closely resembles that of diethylpropion; it is related to phenylethylamines. It is designated as (±)-1-(3-chlorophenyl)-2-[(11-dimethylethyl)amino]-1-propanone hydrochloride. The molecular weight is 276.2. The molecular formula is C13H18Clno • HCl. La poudre de chlorhydrate de bupropion est cristalline blanche et très soluble dans l'eau. Il a un goût amer et produit la sensation d'anesthésie locale sur la muqueuse buccale. La formule structurelle est:
 |
Wellbutrin SR est fourni pour l'administration orale sous forme de 100 mg (bleu) 150 mg (violet) et de 200 mg (rose clair) comprimés à libération prolongée de film. Chaque comprimé contient la quantité marquée de chlorhydrate de bupropion et les ingrédients inactifs: hydrochloride de cystéine de cire de carnauba hydrochloride hypromellose de magnésium stéarate microcristallin en polyéthylène glycol glycol polysorbate 80 et dioxyde de titane et est imprimé avec le Black Ink core. De plus, la tablette de 100 mg contient FD
Utilisations pour Wellbutrin SR
La Wellbutrin SR (chlorhydrate de bupropion) est indiquée pour le traitement du trouble dépressif majeur (MDD) tel que défini par le manuel diagnostique et statistique (DSM).
L'efficacité du bupropion dans le traitement d'un épisode dépressif majeur a été établie dans deux essais d'hospitalisation contrôlés de 4 semaines et un essai ambulatoire contrôlé de 6 semaines de sujets adultes atteints de TDM [voir Études cliniques ].
L'efficacité du Wellbutrin SR dans le maintien d'une réponse antidépressive jusqu'à 44 semaines après 8 semaines de traitement aigu a été démontrée dans un essai contrôlé par placebo [voir Études cliniques ].
Dosage pour Wellbutrin SR
Instructions générales pour une utilisation
Pour minimiser le risque de crise augmenter progressivement la dose [voir AVERTISSEMENTS AND PRÉCAUTIONS ]. Wellbutrin SR tablets should be swallowed whole and not crushed divided or chewed. Wellbutrin SR may be taken with or without food.
La dose cible adulte habituelle pour Wellbutrin SR est de 300 mg / jour donnée à 150 mg deux fois par jour. Initier l'administration avec 150 mg / jour donnée en une seule dose quotidienne le matin. Après 3 jours de dosage, la dose peut être augmentée à la dose cible de 300 mg / jour donnée à 150 mg deux fois par jour. Il devrait y avoir un intervalle d'au moins 8 heures entre les doses successives. Un maximum de 400 mg / jour donné à 200 mg deux fois par jour peut être pris en compte pour les patients chez qui aucune amélioration clinique n'est notée après plusieurs semaines de traitement à 300 mg / jour. Pour éviter les concentrations de pointe élevées de bupropion et / ou de ses métabolites, ne dépassent pas 200 mg en aucune dose unique.
Il est généralement convenu que les épisodes aigus de dépression nécessitent plusieurs mois ou plus de traitement médicamenteux antidépresseur au-delà de la réponse dans l'épisode aigu. On ne sait pas si la dose de Wellbutrin SR nécessaire pour le traitement d'entretien est identique à la dose qui a fourni une réponse initiale. Réévaluez périodiquement la nécessité d'un traitement d'entretien et la dose appropriée pour un tel traitement.
Ajustement de la dose chez les patients souffrant de déficience hépatique
Chez les patients présentant une déficience hépatique modérée à sévère (score de l'enfant-PUGH: 7 à 15) La dose maximale de Wellbutrin Sr est de 100 mg / jour ou 150 mg tous les deux jours. Chez les patients atteints d'une déficience hépatique légère (score de l'enfant-Pugh: 5 à 6) envisagez de réduire la dose et / ou la fréquence de dosage [voir Utiliser dans des populations spécifiques Pharmacologie clinique ].
Ajustement de la dose chez les patients souffrant de troubles rénaux
Envisagez de réduire la dose et / ou la fréquence de la SR Wellbutrin chez les patients atteints de troubles rénaux (taux de filtration glomérulaire [GFR] moins de 90 ml / min) [voir Utiliser dans des populations spécifiques Pharmacologie clinique ].
Changeant d'un patient vers ou à partir d'un antidépresseur inhibiteur de la monoamine oxydase (MAOI)
Au moins 14 jours devraient s'écouler entre l'arrêt d'un MAOI destiné à traiter la dépression et l'initiation de la thérapie avec Wellbutrin SR. Inversement, au moins 14 jours devraient être autorisés après l'arrêt de Wellbutrin Sr avant de commencer un antidépresseur maoi [voir Contre-indications Interactions médicamenteuses ].
Utilisation de Wellbutrin SR avec des maons réversibles tels que le linzolide ou le bleu de méthylène
Ne commencez pas Wellbutrin SR chez un patient qui est traité avec un MAOI réversible comme le linézolide ou le bleu de méthylène intraveineux. Les interactions médicamenteuses peuvent augmenter le risque de réactions hypertensives. Chez un patient qui a besoin d'un traitement plus urgent d'une condition psychiatrique, des interventions non pharmacologiques, y compris l'hospitalisation, doivent être envisagées [voir Contre-indications Interactions médicamenteuses ].
Dans certains cas, un patient recevant déjà un traitement avec la SR de la puits de puits peut nécessiter un traitement urgent avec du linézolide ou du bleu de méthylène intraveineux. Si des alternatives acceptables au traitement linézolide ou au bleu de méthylène intraveineux ne sont pas disponibles et les avantages potentiels du traitement au bleu linézolide ou du méthylène intraveineux sont jugés pour l'emporter sur les risques de réactions hypertensives dans un patient particulier que le bleu de méthylène peut être administré. Le patient doit être surveillé pendant 2 semaines ou jusqu'à 24 heures après la dernière dose de linezolide ou de bleu de méthylène intraveineux, selon la première. La thérapie avec Wellbutrin SR peut être repris 24 heures après la dernière dose de linezolide ou de bleu de méthylène intraveineux.
Le risque d'administrer le bleu de méthylène par des routes non intraveineuses (telles que les comprimés oraux ou par injection locale) ou à des doses intraveineuses bien inférieures à 1 mg / kg avec Wellbutrin SR n'est pas claire. Le clinicien doit néanmoins être conscient de la possibilité d'une interaction médicamenteuse avec une telle utilisation [voir Contre-indications Interactions médicamenteuses ].
Comment fourni
Formes et forces posologiques
- 100 mg - comprimés à libération prolongée enrobés de films rounds bleus imprimés avec Wellbutrin Sr 100.
- 150 mg - comprimés à libération prolongée recouvertes de films violets pourpre imprimés avec Wellbutrin SR 150.
- 200 mg - comprimés à libération prolongée enrobés de biconvexe rose lié imprimé avec Wellbutrin SR 200.
Stockage et manipulation
Wellbutrin SR comprimés à libération prolongée 100 mg du chlorhydrate de bupropion est des comprimés en revêtement biconvexes bleus imprimés avec Wellbutrin Sr 100 dans des bouteilles de 60 ( NDC 0173-0947-55) Comprimés.
Wellbutrin SR comprimés à libération prolongée 150 mg du chlorhydrate de bupropion sont des comprimés en revêtement de film de Biconvex pourpre imprimés avec Wellbutrin Sr 150 en bouteilles de 60 ( NDC 0173-0135-55) Comprimés.
Wellbutrin SR comprimés à libération prolongée 200 mg du chlorhydrate de bupropion est des comprimés en revêtement de film biconvexes roses lights imprimés avec Wellbutrin Sr 200 en bouteilles de 60 ( NDC 0173-0722-00) Comprimés.
Stocker à température ambiante de 20 ° à 25 ° C (68 ° à 77 ° F); Excursions autorisées entre 15 ° C et 30 ° C (59 ° F et 86 ° F) [voir Température ambiante contrôlée par l'USP ]. Protect from light and moisture.
GlaxoSmithKline Durham NC 27701.
Effets secondaires for Welbutrin SR
Les effets indésirables suivants sont discutés plus en détail dans d'autres sections de l'étiquetage:
- Pensées et comportements suicidaires chez les adolescents et les jeunes adultes [voir Avertissement en boîte AVERTISSEMENTS AND PRÉCAUTIONS ]
- Symptômes neuropsychiatriques et risque de suicide dans le traitement de l'arrêt du tabac [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Crise [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Hypertension [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Activation de la manie ou de l'hypomanie [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Psychose et autres réactions neuropsychiatriques [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Glaucome d'angle de serrage [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
- Réactions d'hypersensibilité [voir AVERTISSEMENTS AND PRÉCAUTIONS ]
Expérience des essais cliniques
Étant donné que les essais cliniques sont menés dans des conditions de réaction indésirables très variables observées dans les essais cliniques d'un médicament ne peuvent pas être directement comparées aux taux dans les essais cliniques d'un autre médicament et ne peuvent pas refléter les taux observés dans la pratique clinique.
Réactions indésirables conduisant à l'arrêt du traitement
Dans les essais cliniques contrôlés par placebo, 4% 9% et 11% des groupes placebo 300 mg / jour et 400 mg / jour ont respectivement arrêté le traitement en raison de réactions indésirables. Les effets indésirables spécifiques conduisant à l'arrêt dans au moins 1% des groupes de 300 mg / jour ou 400 mg / jour et à un taux au moins deux fois le taux de placebo sont répertoriés dans le tableau 2.
Tableau 2: Arrêt du traitement en raison des effets indésirables des essais contrôlés par placebo
| Réaction indésirable | Placebo (n = 385) | Wellbutrin SR 300 mg / jour (n = 376) | Wellbutrin SR 400 mg / jour (n = 114) |
| Éruption cutanée | 0,0% | 2,4% | 0,9% |
| Nausée | 0,3% | 0,8% | 1,8% |
| Agitation | 0,3% | 0,3% | 1,8% |
| Migraine | 0,3% | 0,0% | 1,8% |
Réactions indésirables couramment observées
Les effets indésirables du tableau 3 se produisant dans au moins 5% des sujets traités avec Wellbutrin SR et à un taux au moins deux fois le taux de placebo sont répertoriés ci-dessous pour les groupes de dose de 300 et 400 mg / jour.
Wellbutrin SR 300 mg / jour: Anorexie bouche sèche rash sweating tinnitus and tremor.
Wellbutrin SR 400 mg / jour: Douleurs abdominales agitation anxiété vertiges bouche sèche insomnia myalgia nausée palpitation pharyngitis sweating tinnitus and urinary frequency.
Les effets indésirables rapportés dans les essais contrôlés par placebo sont présentés dans le tableau 3. Les effets indésirables rapportés ont été classés en utilisant un dictionnaire basé sur Costart.
Tableau 3: Réactions indésirables rapportées par au moins 1% des sujets et à une fréquence plus grande que le placebo dans les essais cliniques contrôlés
| Système corporel / réaction indésirable | Wellbutrin SR 300 mg / jour (n = 376) | Wellbutrin SR 400 mg / jour (n = 114) | Placebo (n = 385) |
| Corps (général) | |||
| Mal de tête | 26% | 25% | 23% |
| Infection | 8% | 9% | 6% |
| Douleurs abdominales | 3% | 9% | 2% |
| Asthénie | 2% | 4% | 2% |
| Douleur thoracique | 3% | 4% | 1% |
| Douleur | 2% | 3% | 2% |
| Fièvre | 1% | 2% | — |
| Cardiovasculaire | |||
| Palpitation | 2% | 6% | 2% |
| Bouffée | 1% | 4% | — |
| Migraine | 1% | 4% | 1% |
| Bouffées de chaleur | 1% | 3% | 1% |
| Digestif | |||
| Bouche sèche | 17% | 24% | 7% |
| Nausée | 13% | 18% | 8% |
| Constipation | 10% | 5% | 7% |
| Diarrhée | 5% | 7% | 6% |
| Anorexie | 5% | 3% | 2% |
| Vomissement | 4% | 2% | 2% |
| Dysphagie | 0% | 2% | 0% |
| Musculo-squelettique | |||
| Myalgie | 2% | 6% | 3% |
| Arthralgie | 1% | 4% | 1% |
| Arthrite | 0% | 2% | 0% |
| Tic | 1% | 2% | — |
| Système nerveux | |||
| Insomnie | 11% | 16% | 6% |
| Vertiges | 7% | 11% | 5% |
| Agitation | 3% | 9% | 2% |
| Anxiété | 5% | 6% | 3% |
| Tremblement | 6% | 3% | 1% |
| Nervosité | 5% | 3% | 3% |
| Somnolence | 2% | 3% | 2% |
| Irritabilité | 3% | 2% | 2% |
| La mémoire a diminué | — | 3% | 1% |
| Paresthésie | 1% | 2% | 1% |
| Stimulation du système nerveux central | 2% | 1% | 1% |
| Respiratoire | |||
| Pharyngite | 3% | 11% | 2% |
| Sinusite | 3% | 1% | 2% |
| Toux accrue | 1% | 2% | 1% |
| Peau | |||
| Transpiration | 6% | 5% | 2% |
| Éruption cutanée | 5% | 4% | 1% |
| Prurit | 2% | 4% | 2% |
| Urticaire | 2% | 1% | 0% |
| Sens spéciaux | |||
| Sonnerie | 6% | 6% | 2% |
| Perversion de goût | 2% | 4% | — |
| Vision floue ou diplopie | 3% | 2% | 2% |
| Urogénital | |||
| Fréquence urinaire | 2% | 5% | 2% |
| Urgence urinaire | — | 2% | 0% |
| Hémorragie vaginalea | 0% | 2% | — |
| Infection des voies urinaires | 1% | 0% | — |
| a Incidence basée sur le nombre de sujets féminins. - Le trait d'union indique des événements indésirables survenant dans plus de 0 mais moins de 0,5% des sujets. |
Autres effets indésirables observés lors du développement clinique du bupropion
En plus des effets indésirables notés ci-dessus, les effets indésirables suivants ont été signalés dans des essais cliniques avec la formulation à libération prolongée de bupropion chez des sujets déprimés et chez les fumeurs non déprimés ainsi que dans les essais cliniques avec la formulation immédiate à libération du bupropion.
Les fréquences des réactions indésirables représentent la proportion de sujets qui ont connu une réaction indésirable émergente au traitement à au moins une occasion des essais contrôlés par placebo pour la dépression (n = 987) ou la cessation de tabagisme (n = 1013) ou des sujets qui ont connu une réaction indésirable nécessitant un désintérêt du traitement dans un essai de surveillance de la marque ouverte avec un SR Wellbutrin (n = 3100). Toutes les effets indésirables émergents du traitement sont inclus, à l'exception de ceux énumérés dans le tableau 3 ceux énumérés dans d'autres sections liées à la sécurité des informations de prescription celles qui ont subsumé les termes Costart qui sont trop généraux ou excessivement spécifiques afin d'être non informatifs qui ne sont pas raisonnablement associés à l'utilisation du médicament et qui ne sont pas graves et qui se sont produits dans moins de 2 sujets.
Les effets indésirables sont en outre classés par système corporel et répertoriés dans l'ordre de diminuer la fréquence en fonction des définitions suivantes de la fréquence: les réactions indésirables fréquentes sont définies comme celles survenant chez au moins 1/100 sujets. Des réactions indésirables peu fréquentes sont celles qui se produisent chez 1/100 à 1/1000 sujets tandis que des événements rares sont ceux qui se produisent chez moins de 1/1000 sujets.
Corps (général): Les frissons soient rares et la photosensibilité des frissons. Rare était un malaise.
Cardiovasculaire: Peu fréquents étaient une tachycardie et une vasodilatation de l'AVC et une vasodilatation de l'hypotension posturale. Les rares étaient la syncope et l'infarctus du myocarde.
Le tramadol est-il bon pour les maux de dos
Digestif: Peu fréquents étaient une fonction hépatique anormale du bruxisme reflux gingivite accru la salivation de la salivation ulcères bouche ulcères stomatite et soif. Rare était un œdème de la langue.
Hémic et lymphatique: Rare était l'ecchymose. Métabolique et nutritionnel: peu fréquent était un œdème et un œdème périphérique.
Musculo-squelettique: Les crampes de jambe peu fréquentes étaient peu fréquentes.
Système nerveux: Peu fréquents étaient une coordination anormale diminuée de la dépersonnalisation de la libido dysphorisation de la dysphorisation émotionnelle hostilité hyperkinésie hypertonie hypertonie ideation suicidaire et vertige. Les rares étaient l'ataxie à l'ataxie et à l'hypomanie.
Respiratoire: Rare était le bronchospasme. Des sens spéciaux: peu fréquents étaient une anomalie d'hébergement et une sécheresse oculaire.
Urogénital: Peu fréquents étaient une polyurie d'impuissance et un trouble de la prostate.
Changements de poids corporel
Dans les essais contrôlés par placebo, les sujets ont subi une prise de poids ou une perte de poids comme indiqué dans le tableau 4.
Tableau 4: Incidence de la prise de poids et de la perte de poids (≥ 5 lb) dans les essais contrôlés par placebo
| Changement de poids | Wellbutrin SR 300 mg / jour (n = 339) | Wellbutrin SR 400 mg / jour (n = 112) | Placebo (n = 347) |
| Gagné> 5 livres. | 3% | 2% | 4% |
| Perdu> 5 livres. | 14% | 19% | 6% |
Dans les essais cliniques menés avec la formulation immédiate à libération de bupropion, 35% des sujets recevant des antidépresseurs tricycliques ont pris du poids par rapport à 9% des sujets traités avec la formulation à libération immédiate du bupropion. Si la perte de poids est un signe majeur présentant le signe de la maladie dépressive d'un patient, le potentiel anorectique et / ou le potentiel de réduction du poids de Wellbutrin SR doit être pris en compte.
Expérience de commercialisation de la poste
Les effets indésirables suivants ont été identifiés lors de l'utilisation post-approbation de Wellbutrin SR et ne sont pas décrits ailleurs dans l'étiquette. Étant donné que ces réactions sont rapportées volontairement d'une population de taille incertaine, il n'est pas toujours possible d'estimer de manière fiable leur fréquence ou d'établir une relation causale à l'exposition au médicament.
Corps (général)
Arthralgie myalgia and fever with rash and other symptoms suggestive of delayed hypersensitivity. These symptoms may resemble serum sickness [see AVERTISSEMENTS AND PRÉCAUTIONS ].
Cardiovasculaire
Compléter les extrasystoles auriculo-ventriculaires complètes hypertension hypertension (dans certains cas sévères) Embolie pulmonaire phlébite et modèle / syndrome de Brugada.
Digestif
Colite Esophagite Hémorragie gums Hémorragie Hépatite Perforation intestinale Pancréatite et ulcère de l'estomac.
Endocrine
HYPONATRÉMIE HYPOLYCÉMIE D'HYPERGLYCÉMIE ET SYNDROME DE LA SÉCRÉTION DES HORMONES ANTIDUURÉTIQUES INAPPOPRIPATIVES.
Hémic et lymphatique
Anémie leucocytose leukopénie lymphadénopathie pancytopénie et thrombocytopénie. Le PT et / ou l'INR modifié rarement associés à des complications hémorragiques ou thrombotiques ont été observés lorsque le bupropion a été co-administré avec de la warfarine.
Métabolique et nutritionnel
Glycosurie.
Musculo-squelettique
Rigidité musculaire / fièvre / rhabdomyolyse et faiblesse musculaire.
Système nerveux
Électroencéphalogramme anormal (EEG) Agression Akinésie aphasie coma terminée Suicide Delirium Dusions Dysarthria Euphoria Extrapyramidal Syndrome (Dyskinesia Dystonia Hypokinsia Parkinsonisms Hallucinations a augmenté la réaction de libido et la réaction de la neuropathie paranoïde de la Néropathe paranoïde.
Respiratoire
Pneumonie.
Peau And Subcutaneous Tissue Disorders
Alopécie œdème angio-œdème exfoliatif Dermatite Hirsutisme Syndrome de Stevens-Johnson aiguë généralisée de pustulose exanthémateuse et réaction médicamenteuse avec l'éosinophilie et les symptômes systémiques (robe).
Sens spéciaux
La surdité a augmenté la pression intraoculaire et la mydriase.
Urogénital
Cystite anormale de l'éjaculation Dyspareunia Dyurie gynécomastie ménopause érection douloureuse salpingite incontinence urinaire rétention urinaire et vaginite.
Interactions médicamenteuses for Welbutrin SR
Potentiel pour les autres médicaments à affecter Wellbutrin SR
Le bupropion est principalement métabolisé en hydroxybupropion par CYP2B6. Par conséquent, le potentiel existe pour les interactions médicamenteuses entre la Wellbutrin SR et les médicaments qui sont des inhibiteurs ou des inducteurs du CYP2B6.
Inhibiteurs du CYP2B6
Ticlopidine et clopidogrel
Le traitement concomitant avec ces médicaments peut augmenter l'exposition au bupropion mais diminuer l'exposition à l'hydroxybupropion. Sur la base de la réponse clinique, l'ajustement de la dose de la SR de la puits de bien-être peut être nécessaire lorsqu'il est co-administré avec des inhibiteurs du CYP2B6 (par exemple la ticlopidine ou le clopidogrel) [voir Pharmacologie clinique ].
Inducteurs de CYP2B6
Ritonavir Lopinavir et Efavirenz
Le traitement concomitant avec ces médicaments peut diminuer l'exposition au bupropion et à l'hydroxybupropion. Une augmentation de la dose de la SR de Wellbutrin peut être nécessaire lorsqu'elle est co-administrée avec du ritonavir lopinavir ou efavirenz [voir Pharmacologie clinique ] mais ne doit pas dépasser la dose maximale recommandée.
Phénobarbital de carbamazépine phénytoïne
Bien qu'il n'ait pas été systématiquement étudié, ces médicaments peuvent induire le métabolisme du bupropion et peuvent diminuer l'exposition au bupropion [voir Pharmacologie clinique ]. If bupropion is used concomitantly with a CYP inducer it may be necessary to increase the dose of bupropion but the maximum recommended dose should not be exceeded.
Potentiel de Wellbutrin SR pour affecter d'autres médicaments
Médicaments métabolisés par CYP2D6
Le bupropion et ses métabolites (érythrohydrobupropion thréohydrobupropion hydroxybupropion) sont des inhibiteurs du CYP2D6. Par conséquent, la co-administration de Wellbutrin SR avec des médicaments métabolisés par CYP2D6 peut augmenter les expositions de médicaments qui sont des substrats de CYP2D6. De tels médicaments comprennent certains antidépresseurs (par exemple la Venlafaxine Nortriptyline Imipramine Desipramine paroxétine fluoxétine et la sertraline) antipsychotiques (par exemple les bêtroqueurs de la rispéridone halopéridol) et les antiarhythmiques (par exemple procédol et le flanc). Lorsqu'il est utilisé concomitamment avec la SR de Wellbutrin, il peut être nécessaire de diminuer la dose de ces substrats CYP2D6, en particulier pour les médicaments avec un indice thérapeutique étroit.
Les médicaments qui nécessitent une activation métabolique par le CYP2D6 sont efficaces (par exemple le tamoxifène) en théoriquement auraient pu réduire l'efficacité lorsqu'ils sont administrés en concomitance avec des inhibiteurs du CYP2D6 tels que le bupropion. Les patients traités en concomitance avec la SR de la wellbutrin et de tels médicaments peuvent nécessiter des doses accrues du médicament [voir Pharmacologie clinique ].
Digoxine
La co-administration de Wellbutrin SR avec la digoxine peut diminuer les taux plasmatiques de digoxine. Surveiller les taux plasmatiques de digoxine chez les patients traités concomitamment avec la SR de la welbutrin et la digoxine [voir Pharmacologie clinique ].
Médicaments qui réduisent le seuil de saisie
Utilisez une extrême prudence lors de la co-administration de Wellbutrin SR avec d'autres médicaments qui abaissent le seuil de crise (par exemple, d'autres produits de bupropion antipsychotiques antidépresseurs théophylline ou corticostéroïdes systémiques). Utilisez de faibles doses initiales et augmentez progressivement la dose [voir Contre-indications AVERTISSEMENTS AND PRÉCAUTIONS ].
Médicaments dopaminergiques (Levodopa et amantadine)
La bupropion levodopa et l'amantadine ont des effets agonistes de dopamine. La toxicité du SNC a été signalée lorsque le bupropion a été co-administré avec la lévodopa ou l'amantadine. Les effets indésirables ont inclus l'agitation d'agitation des tremblements d'ataxie perturbation des vertiges et des étourdissements. Il est présumé que la toxicité résulte des effets cumulatifs des agonistes de la dopamine. Faire preuve de prudence lors de l'administration de Wellbutrin SR concomitamment avec ces médicaments.
Utiliser avec l'alcool
Dans l'expérience de la post-commercialisation, il y a eu de rares rapports d'événements neuropsychiatriques défavorables ou d'une tolérance à l'alcool réduite chez les patients qui buvaient de l'alcool pendant le traitement avec Wellbutrin SR. La consommation d'alcool pendant le traitement par Wellbutrin SR doit être minimisée ou évité.
Inhibiteurs du MAO
Le bupropion inhibe la recapture de la dopamine et de la norépinéphrine. L'utilisation concomitante de MAOI et de bupropion est contre-indiquée car il existe un risque accru de réactions hypertensives si le bupropion est utilisé en même temps que les MAOI. Des études sur les animaux démontrent que la toxicité aiguë du bupropion est améliorée par l'inhibiteur de MAO phénelzine. Au moins 14 jours devraient s'écouler entre l'arrêt d'un MAOI destiné à traiter la dépression et l'initiation du traitement avec Wellbutrin SR. Inversement, au moins 14 jours devraient être autorisés après l'arrêt de Wellbutrin Sr avant de commencer un antidépresseur maoi [voir Posologie et administration Contre-indications ].
Interactions de test médicament-laboratoire
Des tests de dépistage des immunoosises d'urine pour l'urine pour les amphétamines ont été signalés chez des patients prenant du bupropion. Cela est dû au manque de spécificité de certains tests de dépistage. Les résultats des tests en fausse positifs peuvent en résulter même après l'arrêt de la thérapie de bupropion. Les tests de confirmation tels que la chromatographie en phase gazeuse / spectrométrie de masse distingueront le bupropion des amphétamines.
Abus de drogues et dépendance
Substance contrôlée
Le bupropion n'est pas une substance contrôlée.
Abus
Humains
Des essais cliniques contrôlés menés dans des volontaires normaux chez des sujets ayant des antécédents d'abus de médicaments multiples et chez des sujets déprimés ont montré une certaine augmentation de l'activité motrice et de l'agitation / excitation souvent typique de l'activité du stimulant central.
Dans une population d'individus subis par des médicaments d'abus, une seule dose orale de 400 mg d'activité de type amphétamine a produit une légère sous-échelle de la sous-échelle de la morphine-benzedrine des inventaires de recherche de la toxicomanie (ARCI) et un score plus que placebo mais moins de 15 mg de la délexion stimulante de l'annexe II. Ces échelles mesurent les sentiments généraux d'euphorie et de plaisir drogue qui sont souvent associés au potentiel d'abus.
Les résultats des essais cliniques ne sont cependant pas connus pour prédire de manière fiable le potentiel d'abus des médicaments. Néanmoins, les preuves des essais à dose unique suggèrent que la dose quotidienne recommandée de bupropion lorsqu'il est administré par voie orale à des doses divisées n'est pas susceptible de se renforcer de manière significative en amphétamine ou des agresseurs de stimulants du SNC. Cependant, des doses plus élevées (qui n'ont pas pu être testées en raison du risque de crise) pourraient être modestement attrayantes pour ceux qui abusent des médicaments stimulants du SNC.
Wellbutrin SR est destiné à une utilisation orale uniquement. L'inhalation de comprimés écrasés ou l'injection de bupropion dissous a été signalée. Des convulsions et / ou des cas de décès ont été signalés lorsque le bupropion a été administré par voie intranasale ou par injection parentérale.
Animaux
Des études sur les rongeurs et les primates ont démontré que le bupropion présente certaines actions pharmacologiques communes aux psychostimulants. Chez les rongeurs, il a été démontré que l'activité locomotrice provoque une légère réponse du comportement stéréotypée et augmente les taux de réponse dans plusieurs paradigmes de comportement contrôlés par le calendrier. Dans les modèles de primates, évaluant les effets de renforcement positif des médicaments psychoactifs, le bupropion a été auto-administré par voie intraveineuse. Chez le rat, le bupropion a produit des effets de stimulus discriminatifs de type amphétamine et de type cocaïne dans les paradigmes de discrimination médicamenteuse utilisés pour caractériser les effets subjectifs des médicaments psychoactifs.
Avertissements pour Wellbutrin Sr
Inclus dans le cadre du PRÉCAUTIONS section.
Précautions pour Wellbutrin Sr
Pensées et comportements suicidaires chez les enfants adolescents et jeunes adultes
Les patients atteints de TDM à la fois adulte et pédiatrique peuvent subir une aggravation de leur dépression et / ou de l'émergence d'idées et de comportements suicidaires (suicidalité) ou de changements inhabituels dans le comportement, qu'ils prennent ou non des médicaments antidépresseurs et ce risque peut persister jusqu'à ce que une rémission significative se produise. Le suicide est un risque connu de dépression et certains autres troubles psychiatriques et ces troubles eux-mêmes sont les prédicteurs les plus forts du suicide. Il y a eu une préoccupation de longue date que les antidépresseurs peuvent avoir un rôle dans l'induction de l'aggravation de la dépression et de l'émergence de la suicidalité chez certains patients au cours des premières phases du traitement.
Des analyses regroupées des essais à court terme contrôlées par placebo de médicaments antidépresseurs (inhibiteurs sélectifs de la sérotonine [ISRS] et autres) montrent que ces médicaments augmentent le risque de pensée et de comportement suicidaires (suicidalité) chez les adolescents et les jeunes adultes (âgés de 18 ans à 24) avec MDD et d'autres troubles psychiatriques. Les essais cliniques à court terme n'ont pas montré une augmentation du risque de suicidalité avec des antidépresseurs par rapport au placebo chez les adultes au-delà de 24 ans; Il y a eu une réduction des antidépresseurs par rapport au placebo chez les adultes de 65 ans et plus.
Les analyses regroupées des essais contrôlés par placebo chez les enfants et les adolescents atteints de troubles compulsifs obsessionnels (TOC) ou autres troubles psychiatriques incluent un total de 24 essais à court terme de 9 antidépresseurs chez plus de 4400 sujets. Les analyses regroupées des essais contrôlées par placebo chez les adultes atteints de TDM ou d'autres troubles psychiatriques comprenaient un total de 295 essais à court terme (durée médiane de 2 mois) de 11 médicaments antidépresseurs chez plus de 77 000 sujets. Il y avait une variation considérable du risque de suicidalité entre les médicaments, mais une tendance à une augmentation des sujets plus jeunes pour presque tous les médicaments étudiés. Il y avait des différences dans le risque absolu de suicidalité à travers les différentes indications avec l'incidence la plus élevée dans le TDM. Les différences de risque (médicament contre placebo) étaient cependant relativement stables dans les strates d'âge et à travers les indications. Ces différences de risque (différence de lieu de drogue dans le nombre de cas de suicidalité pour 1000 sujets traités) sont fournis dans le tableau 1.
Tableau 1: Différences de risque dans le nombre de cas de suicidalité par groupe d'âge dans les essais contrôlés par placebo d'antidépresseurs chez les sujets pédiatriques et adultes
| Tranche d'âge | Drug-lieu différence dans le nombre de cas de suicidalité pour 1000 sujets traités |
| Augmentation par rapport au placebo | |
| <18 | 14 cas supplémentaires |
| 18-24 | 5 cas supplémentaires |
| Diminue par rapport au placebo | |
| 25-64 | 1 cas de moins |
| ≥65 | 6 cas moins |
Aucun suicide ne s'est produit dans aucun des essais pédiatriques. Il y avait des suicides dans les essais pour adultes, mais le nombre n'était pas suffisant pour parvenir à une conclusion sur l'effet du médicament sur le suicide.
On ne sait pas si le risque de suicidalité s'étend à une utilisation à plus long terme, c'est-à-dire au-delà de plusieurs mois. Cependant, il existe des preuves substantielles provenant d'essais d'entretien contrôlés par placebo chez les adultes souffrant de dépression que l'utilisation d'antidépresseurs peut retarder la récidive de la dépression.
Tous les patients traités avec des antidépresseurs pour toute indication doivent être surveillés de manière appropriée et observés étroitement pour une aggravation clinique et des changements inhabituels dans le comportement, en particulier pendant les premiers mois d'un traitement médicamenteux, soit en période de changements de dose augmentent ou diminuent [voir l'avertissement en boîte].
Les symptômes suivants agitation anxiété attaque l'insomnie Irritabilité Hostilité Agressivité Impulsivité Akathisie (agitation psychomotrice) Hypomanie et manie ont été signalées chez les patients adultes et pédiatriques traités avec des antidépresseurs principaux ainsi que pour d'autres indications psychiatriques et non psychiatriques. Bien qu'un lien causal entre l'émergence de ces symptômes et soit l'aggravation de la dépression et / ou l'émergence d'impulsions suicidaires ne se soient pas établies, il est à craindre que de tels symptômes représentent les précurseurs de la suicidalité émergente.
Une considération doit être accordée à la modification du régime thérapeutique, notamment en désintégrant le médicament chez les patients dont la dépression est constamment pire ou qui éprouve une suicidalité ou des symptômes émergents qui pourraient être des précurseurs pour aggraver la dépression ou la suicidalité, en particulier si ces symptômes sont graves abrupt lors de l'apparition ou ne faisaient pas partie des symptômes de présentation du patient.
Les familles et les soignants des patients traités avec des antidépresseurs pour le TDM ou d'autres indications psychiatriques et non psychiatriques doivent être alertés sur la nécessité de surveiller les patients pour l'émergence de l'agitation irritabilité des changements inhabituels dans le comportement et les autres symptômes décrits ci-dessus ainsi que l'émergence de la suicidie et de signaler ces symptômes immédiatement aux prestataires de soins de santé. Une telle surveillance devrait inclure l'observation quotidienne par les familles et les soignants. Les prescriptions de Wellbutrin SR doivent être rédigées pour la plus petite quantité de comprimés conformes à une bonne gestion des patients afin de réduire le risque de surdose.
Événements indésirables neuropsychiatriques et risque de suicide dans le traitement de l'arrêt du tabac
Wellbutrin SR n'est pas approuvé pour le traitement de l'arrêt du tabac; Cependant, il contient le même ingrédient actif que le médicament à l'arrêt du tabac Zyban. Des événements indésirables neuropsychiatriques graves ont été signalés chez des patients prenant du bupropion pour le sevrage tabagique. Ces rapports de commercialisation ont inclus des changements d'humeur (y compris la dépression et la manie) psychose Hallucinations Paranoïa Dégustes Homicidal Ideatation Aggression Hostilité Agitation Angitation et panique ainsi que la tentative de suicide des idées suicidaires et le suicide terminé [voir Effets indésirables ]. Some patients who stopped smoking may have been experiencing symptoms of nicotine withdrawal including humeur déprimée. Depression rarely including suicidal ideation has been reported in smokers undergoing a smoking cessation attempt without medication. However some of these adverse events occurred in patients taking bupropion who continued to smoke.
Des événements indésirables neuropsychiatriques se sont produits chez les patients sans et avec une maladie psychiatrique préexistante; Certains patients ont connu une aggravation de leurs maladies psychiatriques. Observez les patients pour la survenue d'événements indésirables neuropsychiatriques. Informez les patients et les soignants que le patient doit cesser de prendre de la wellbutrin et contacter immédiatement un fournisseur de soins de santé si l'agitation a déprimé l'humeur ou les changements de comportement ou de pensée qui ne sont pas typiques pour le patient sont observés ou si le patient développe des idées suicidaires ou un comportement suicidaire. Dans de nombreux cas post-commercialisation, une résolution des symptômes après l'arrêt du bupropion a été signalée. Cependant, les symptômes ont persisté dans certains cas; Par conséquent, une surveillance continue et des soins de soutien doivent être fournis jusqu'à ce que les symptômes se résolvent.
Crise d'épilepsie
Wellbutrin SR peut provoquer des crises. Le risque de saisie est lié à la dose. La dose ne doit pas dépasser 400 mg / jour. Augmenter la dose progressivement. Arrêtez Wellbutrin SR et ne redémarrez pas le traitement si le patient connaît une crise.
Le risque de crises est également lié aux facteurs des patients situations cliniques et aux médicaments concomitants qui réduisent le seuil de crise. Considérez ces risques avant de lancer un traitement avec Wellbutrin SR. La SR Wellbutrin est contre-indiquée chez les patients atteints d'un trouble de crise actuel ou de diagnostic préalable de l'anorexie mentale ou de la boulimie ou subissant une abrupte d'arrêt des barbituriques de benzodiazépines d'alcool et de médicaments antiépiléptiques [voir Contre-indications Interactions médicamenteuses ]. The following conditions can also increase the risk of seizure: severe head injury; arteriovenous malformation ; CNS tumor or CNS infection; severe stroke; concomitant use of other medications that lower the seizure threshold (e.g. other bupropion products antipsychotics tricyclic antidepressants theophylline and systemic corticosteroids); metabolic disorders (e.g. hypoglycémie hyponatrémie sévère altération hépatique et hypoxie); usage de drogues illicites (par exemple la cocaïne); ou abus ou abus de médicaments sur ordonnance tels que les stimulants du SNC. Les conditions prédisposantes supplémentaires incluent diabète sucré traité avec des médicaments hypoglycémiques oraux ou de l'insuline; utilisation de médicaments anorectiques; et une consommation excessive d'alcool benzodiazépines sédatifs / hypnotiques ou opiacés.
Incidence de saisie avec l'utilisation de bupropion
Lorsque Wellbutrin SR est dosé jusqu'à 300 mg / jour, l'incidence de la crise est d'environ 0,1% (1/1000) et augmente à environ 0,4% (4/1000) à la dose maximale recommandée de 400 mg / jour.
Le risque de crise peut être réduit si la dose de Wellbutrin SR ne dépasse pas 400 mg / jour donné à 200 mg deux fois par jour et le taux de titrage est progressif.
Hypertension
Le traitement avec Wellbutrin SR peut entraîner une pression artérielle et une hypertension élevées. Évaluez la pression artérielle avant de lancer un traitement avec Wellbutrin SR et surveillez périodiquement pendant le traitement. Le risque d'hypertension augmente si la SR de la welbutrin est utilisée en même temps que les MAOI ou autres médicaments qui augmentent l'activité dopaminergique ou noradrénergique [voir Contre-indications ].
Les données d'un essai comparatif de la formulation à libération prolongée du système transdermique de nicotine HCL (NTS) de Bupropion La combinaison de Bupropion à libération prolongée plus du NTS et du placebo comme aide à la retenue tabagique suggèrent une incidence plus élevée d'hypertension émergente au traitement chez les patients chez les patients. Dans cet essai, 6,1% des sujets traités avec la combinaison de bupropion à libération prolongée et de NTS avaient une hypertension émergente au traitement contre 2,5% 1,6% et 3,1% des sujets traités respectivement avec des NT de bupropion à libération prolongée et un placebo respectivement. La majorité de ces sujets avaient des preuves d'hypertension préexistante. Trois sujets (1,2%) traités avec la combinaison de bupropion et de NTS à libération prolongée et de 1 sujet (0,4%) traité avec des NTs avaient des médicaments d'étude interrompus en raison de l'hypertension par rapport à aucun des sujets traités avec du bupropion à libération prolongée ou du placebo. La surveillance de la pression artérielle est recommandée chez les patients qui reçoivent la combinaison de bupropion et de remplacement de la nicotine.
Dans un essai clinique de la libération immédiate du bupropion chez les sujets MDD avec stable insuffisance cardiaque congestive (N = 36) Le bupropion a été associé à une exacerbation de l'hypertension préexistante chez 2 sujets conduisant à l'arrêt du traitement du bupropion. Il n'y a pas d'essais contrôlés évaluant la sécurité du bupropion chez les patients ayant des antécédents récents d'infarctus du myocarde ou d'une maladie cardiaque instable.
Activation de la manie / hypomanie
Le traitement antidépresseur peut précipiter un épisode maniaque maniaque ou hypomanique. Le risque semble augmenter chez les patients atteints trouble bipolaire ou qui ont des facteurs de risque de trouble bipolaire. Avant d'initier les patients atteints d'écran SR de Wellbutrin pour des antécédents de trouble bipolaire et la présence de facteurs de risque de trouble bipolaire (par exemple, les antécédents familiaux de suicide du trouble bipolaire ou de dépression). Wellbutrin SR n'est pas approuvé pour être utilisé dans le traitement de la dépression bipolaire.
Psychose et autres réactions neuropsychiatriques
Les patients déprimés traités par Wellbutrin SR ont eu une variété de signes et symptômes neuropsychiatriques, notamment les délires hallucinations de la concentration de psychose Paranoïa et confusion. Certains de ces patients avaient un diagnostic de trouble bipolaire. Dans certains cas, ces symptômes ont diminué lors de la réduction de la dose et / ou du retrait du traitement. Demandez aux patients de contacter un professionnel de la santé si de telles réactions se produisent.
Glaucome d'angle
La dilatation pupillaire qui se produit après l'utilisation de nombreux médicaments antidépresseurs, notamment la SR de Wellbutrin, peut déclencher une attaque d'angle chez un patient avec des angles anatomiquement étroits qui n'ont pas d'iridectomie de brevet.
Réactions d'hypersensibilité
Des réactions anaphylactoïdes / anaphylactiques se sont produites lors d'essais cliniques avec du bupropion. Les réactions ont été caractérisées par le prurit urticaire angio-œdème et la dyspnée nécessitant un traitement médical. De plus, il y a eu de rares rapports spontanés post-commercialisation de l'érythème multiforme Stevens-Johnson et anaphylactique choc associé au bupropion. Demandez aux patients d'arrêter Wellbutrin SR et de consulter un fournisseur de soins de santé s'ils développent une réaction allergique ou anaphylactoïde / anaphylactique (par exemple, éruption cutanée pour ruches de la douleur thoracique et essoufflement) pendant le traitement.
Il y a des rapports de fièvre de la myalgie de l'arthralgie avec une éruption cutanée et d'autres symptômes de maladie sérique suggérant une hypersensibilité retardée.
Informations de conseil des patients
Conseiller au patient de lire l'étiquetage des patients approuvé par la FDA ( Guide des médicaments ).
Pensées et comportements suicidaires
Instruisez les patients leurs familles et / ou leurs soignants pour être attentifs à l'émergence de l'agitation anxiété attaque l'insomnie de l'hostilité d'irritabilité Impulsivité d'agressivité Akathisie (l'agitation psychomotrice) Mania Manie, d'autres changements inhabituels dans le comportement de l'aggravation de la dépression et de l'idétion suicidale, en particulier au début du traitement antidépress et lorsque le dose est ajusté en hausse. Conseiller les familles et les soignants des patients à observer pour l'émergence de ces symptômes au quotidien, car les changements peuvent être brusques. De tels symptômes doivent être signalés au prescripteur ou au professionnel de la santé du patient, en particulier s'ils sont gravement abruptes en apparition ou ne faisaient pas partie des symptômes de présentation du patient. Des symptômes comme ceux-ci peuvent être associés à un risque accru de pensée et de comportement suicidaire et indiquer un besoin de surveillance très étroite et éventuellement de changements dans le médicament.
Événements indésirables neuropsychiatriques et risque de suicide dans le traitement de l'arrêt du tabac
Bien que Wellbutrin SR ne soit pas indiqué pour le traitement de l'arrêt du tabac, il contient le même ingrédient actif que Zyban qui est approuvé pour cette utilisation. Informer les patients que certains patients ont connu des changements d'humeur (y compris la dépression et la manie) les hallucinations de psychose paranoïa délires pour l'idéation homicide d'agression hostilité anxiété d'agitation et la panique ainsi que les idées suicidaires et le suicide lors de la tentative de fumer lors de la prise de bupropion. Demandez aux patients d'arrêter le bupropion et de contacter un professionnel de la santé s'ils présentent de tels symptômes [voir AVERTISSEMENTS AND PRÉCAUTIONS Effets indésirables ].
Réactions allergiques graves
Éduquer les patients sur les symptômes de l'hypersensibilité et interrompre Wellbutrin SR s'ils ont une réaction allergique sévère.
Crise d'épilepsie
Demandez aux patients d'arrêter et de ne pas redémarrer Wellbutrin SR s'ils subissent une crise pendant le traitement. Conseillez les patients que l'utilisation excessive ou l'arrêt abrupte des benzodiazépines d'alcool ou les drogues antiépileptiques ou les sédatifs / hypnotiques peuvent augmenter le risque de crise. Conseiller aux patients de minimiser ou d'éviter la consommation d'alcool.
Comme la dose est augmentée pendant le titrage initial à des doses supérieures à 150 mg / jour, les patients ont de prendre des doses de puits de puits à 2 divisions avec au moins 8 heures entre les doses successives pour minimiser le risque de crises.
Glaucome d'angle
Il convient de noter que la prise de Wellbutrin SR peut provoquer une légère dilatation pupillaire qui, chez les individus sensibles glaucome . Le glaucome préexistant est presque toujours un glaucome à angle ouvert car le glaucome à l'angle-clôture lors du diagnostic peut être traité définitivement avec l'iridectomie. Le glaucome à angle ouvert n'est pas un facteur de risque de glaucome d'angle-clôture. Les patients peuvent souhaiter être examinés pour déterminer s'ils sont sensibles à la fermeture d'angle et ont une procédure prophylactique (par exemple l'iridectomie) s'ils sont sensibles [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Produits contenant du bupropion
Éduquer les patients selon lesquels Wellbutrin SR contient le même ingrédient actif (chlorhydrate de bupropion) trouvé dans Zyban qui est utilisé comme aide au traitement du tabac et que le Wellbutrin SR ne devrait pas être utilisé en combinaison avec la formulation de l'étendue de zyban ou de la formulation de l'étendue immédiate et de la réduction immédiate et de l'écart de flux et de l'éclair Formulations et aplenzine La formulation à libération prolongée de l'hydrobromide de bupropion). De plus, il existe un certain nombre de produits génériques de Bupropion HCL pour les formulations à libération immédiate et prolongée.
Potentiel de déficience cognitive et motrice
Informez les patients que tout médicament actif du SNC comme Wellbutrin SR peut nuire à sa capacité à effectuer des tâches nécessitant un jugement ou des compétences motrices et cognitives. Conseillez les patients que, tant qu'ils sont raisonnablement certains que Wellbutrin SR n'affecte pas leurs performances, ils devraient s'abstenir de conduire une automobile ou d'exécuter des machines dangereuses complexes. Wellbutrin SR peut entraîner une diminution de la tolérance à l'alcool.
Médicaments concomitants
Conseiller les patients pour informer leur fournisseur de soins de santé s'ils prennent ou prévoient de prendre des médicaments sur ordonnance ou en vente libre, car les comprimés à libération prolongée de Wellbutrin SR peuvent affecter les uns les autres
Grossesse
Conseiller aux patients de notifier leur fournisseur de soins de santé s'ils tombent enceintes ou ont l'intention de devenir enceintes pendant le traitement avec Wellbutrin SR. Informez les patients qu'il existe un registre d'exposition à la grossesse qui surveille les résultats de la grossesse chez les femmes exposées au Wellbutrin SR pendant la grossesse [voir Utiliser dans des populations spécifiques ].
Informations de stockage
Demandez aux patients de stocker la SR de la puits de puits à température ambiante entre 68 ° F et 77 ° F (20 ° C à 25 ° C) et gardez les comprimés à sec et hors de la lumière.
Informations sur l'administration
Demandez aux patients d'avaler des comprimés Wellbutrin SR entiers afin que le taux de libération ne soit pas modifié. Ne mâchez pas les comprimés de division ou d'écrasement; Ils sont conçus pour libérer lentement le médicament dans le corps. Lorsque les patients prennent plus de 150 mg / jour, demandez-leur de prendre des doses de Wellbutrin à 2 doses à au moins 8 heures d'intervalle pour minimiser le risque de crises. Instruisez les patients s'ils manquent une dose pour ne pas prendre un comprimé supplémentaire pour compenser la dose manquée et prendre le prochain comprimé à l'heure régulière en raison du risque de crise lié à la dose. Instruisez les patients que les comprimés Wellbutrin SR peuvent avoir une odeur. Wellbutrin SR peut être pris avec ou sans nourriture.
Wellbutrin Wellbutrin Sr Wellbutrin XL et Zyban sont des marques détenues ou licenciées au groupe de sociétés GSK. Les autres marques énumérées sont des marques détenues ou licenciées à leurs propriétaires respectives et ne sont pas détenues ou licenciées au groupe de sociétés GSK. Les fabricants de ces marques ne sont pas affiliés et n'approuvent pas le groupe de sociétés GSK ou ses produits.
Toxicologie non clinique
Carcinogenèse Mutagenèse A trouble de la fertilité
Des études de cancérogénicité à vie ont été réalisées chez le rat et les souris à des doses de bupropion jusqu'à 300 et 150 mg / kg / jour respectivement. Ces doses sont environ 7 et 2 fois le MRHD respectivement sur une base de mg / m². Dans l'étude du rat, il y a eu une augmentation des lésions prolifératives nodulaires du foie à des doses de 100 à 300 mg / kg / jour (environ 2 à 7 fois le MRHD sur une base de mg / m²); Les doses plus faibles n'ont pas été testées. La question de savoir si ces lésions peuvent être ou non des précurseurs des néoplasmes du foie ne sont actuellement pas résolus. Des lésions hépatiques similaires n'ont pas été observées dans l'étude de la souris et aucune augmentation des tumeurs malignes du foie et d'autres organes n'a été observée dans l'une ou l'autre étude.
Le bupropion a produit une réponse positive (2 à 3 fois le taux de mutation témoin) dans 2 des 5 souches dans le test de mutagénicité bactérienne Ames. Le bupropion a produit une augmentation des aberrations chromosomiques dans 1 des 3 études cytogénétiques de moelle osseuse de rat in vivo.
Il n'y a eu aucun effet sur la fertilité masculine et féminine lorsque les rats ont été administrés par des doses orales de bupropion jusqu'à 300 mg / kg / jour (environ 7 fois le MRHD sur une base de mg / m²) à des femmes avant l'accouplement et le jour 13 de la gestation ou par la lactation et sur les mâles pendant 60 jours avant et par le fait de le faire. Cependant, des doses de 200 mg / kg / jour (environ 5 fois le MRHD sur une base de mg / m²) ou plus ont provoqué une ataxie transitoire ou des changements comportementaux chez les rats femelles adultes. Il n'y a également eu aucun effet négatif sur la reproduction de la fertilité ou la croissance et le développement de la progéniture masculine ou féminine.
Utiliser dans des populations spécifiques
Grossesse
Grossesse Exposure Registry
Il existe un registre indépendant d'exposition à la grossesse qui surveille les résultats de la grossesse chez les femmes exposées à tout antidépresseur pendant la grossesse. Les prestataires de soins de santé sont encouragés à enregistrer des patients en appelant le National Grossancy Registry pour les antidépresseurs au 1-844-405â6185 ou en visitant en ligne à https://womensmentalhealth.org/research/pregnancyregistry/antidepresses/.
Résumé des risques
Les données des études épidémiologiques sur les femmes enceintes exposées au bupropion au cours du premier trimestre n'ont pas identifié un risque accru de malformations congénitales dans l'ensemble (voir Données ). There are risks to the mother associated with untreated dépression in pregnancy (see Considérations cliniques ). When bupropion was administered to pregnant rats during organogenesis there was no evidence of fetal malformations at doses up to approximately 11 times the maximum recommended human dose (MRHD) of 400 mg/day. When given to pregnant rabbits during organogenesis non-doseâ€related increases in incidence of fetal malformations and skeletal variations were observed at doses approximately equal to the MRHD and greater. Decreased fetal weights were seen at doses twice the MRHD and greater (see Données sur les animaux ).
Le risque de fond estimé pour les principaux malformations congénitales et la fausse couche est inconnue pour la population indiquée. Toutes les grossesses présentent un risque de fond de perte de maltraitance natale ou d'autres résultats indésirables. Dans la population générale américaine, le risque de fond estimé de malformations congénitales majeures et de fausse couche dans les grossesses cliniquement reconnues est respectivement de 2% à 4% et 15% à 20%.
Considérations cliniques
Risque maternel et / ou embryonnaire associé à la maladie
Une étude longitudinale prospective a suivi 201 femmes enceintes ayant des antécédents de troubles dépressifs majeurs qui étaient euthymiques et prenaient des antidépresseurs pendant la grossesse au début de la grossesse. Les femmes qui ont interrompu les antidépresseurs pendant la grossesse étaient plus susceptibles de subir une rechute de dépression majeure que les femmes qui ont continué les antidépresseurs. Considérez les risques pour la mère de la dépression non traitée et des effets potentiels sur le fœtus lors de l'arrêt ou de la modification du traitement avec des médicaments antidépresseurs pendant la grossesse et le post-partum.
Données
Données humaines
Données from the international bupropion Grossesse Registry (675 first trimester exposures) and a retrospective cohort study using the United Healthcare database (1213 first trimester exposures) did not show an increased risk for malformations overall. The Registry was not designed or powered to evaluate specific defects but suggested a possible increase in cardiac malformations.
Aucun risque accru de malformations cardiovasculaires dans l'ensemble n'a été observé après l'exposition au bupropion au cours du premier trimestre. Le taux de malformations cardiovasculaires observés prospectivement lors des grossesses avec exposition au bupropion au cours du premier trimestre du registre international de grossesse était de 1,3% (9 formes cardiovasculaires / 675 Expositions de bupropion maternelle du premier trimestre), ce qui est similaire au taux de fond de malformations cardiovasculaires (approximativement 1%). Les données de la base de données United Healthcare qui avaient un nombre limité de cas exposés avec des malformations cardiovasculaires et une étude cas-témoins (6853 nourrissons atteints de malformations cardiovasculaires et 5763 avec des malformations non cardiovasculaires) de l'étude de la prévention des défauts de la naissance (NBDPS) ont montré une augmentation des risques pour les risques de malformations de malfaisage des cardiaques (NBDPS) ont augmenté de risque de calcul cardiovascar Exposition au cours du premier trimestre.
Les résultats de l'étude sur l'exposition au bupropion au cours du premier trimestre et le risque d'obstruction des tracts de sortie ventriculaire gauche (LVOTO) sont incohérents et ne permettent pas de conclusions concernant une association possible. La base de données United Healthcare manquait de pouvoir suffisant pour évaluer cette association; Les NBDP ont constaté un risque accru de LVOTO (n = 10; OR ajusté = 2,6; IC à 95%: 1,2 5,7) et l'étude de contrôle des cas d'épidémiologie de Slone n'a pas trouvé de risque accru de Lvoto.
Les résultats de l'étude sur l'exposition au bupropion au cours du premier trimestre et le risque de défaut septal ventriculaire (VSD) sont incohérents et ne permettent pas de conclusions concernant une association possible. L'étude de l'épidémiologie de Slone a trouvé un risque accru de VSD après une exposition au bupropion maternelle au premier trimestre (n = 17; ajusté OR = 2,5; IC à 95%: 1,3 5,0) mais n'a trouvé aucun risque accru pour toute autre malformation cardiovasculaire étudiée (y compris Lvoto comme ci-dessus). L'étude de base de données NBDPS et United Healthcare n'a pas trouvé d'association entre l'exposition au bupropion maternelle du premier trimestre et le VSD.
Pour les résultats de LVOTO et VSD, les études ont été limitées par le petit nombre de cas exposés des résultats incohérents entre les études et le potentiel de résultats fortuits de comparaisons multiples dans les études de contrôle.
Données sur les animaux
Dans les études menées chez des rats enceintes et des lapins, le bupropion a été administré par voie orale pendant la période d'organogenèse à des doses allant jusqu'à 450 et 150 mg / kg / jour respectivement (environ 11 et 7 fois le MRHD respectivement sur une base de mg / m²). Il n'y avait aucune preuve de malformations fœtales chez le rat. Lorsqu'ils sont donnés aux lapins enceintes pendant l'organogenèse, des augmentations liées à l'organogenèse dans l'incidence des malformations fœtales et des variations squelettiques ont été observées à la dose la plus faible testée (25 mg / kg / jour approximativement égale à la MRHD sur une base Mg / m²) et plus. Des poids fœtaux diminués ont été observés à des doses de 50 mg / kg / jour (environ 2 fois le MRHD sur une base de mg / m²) et plus. Aucune toxicité maternelle n'était évidente à des doses de 50 mg / kg / jour ou moins.
Dans une étude de développement pré et postnatal, bupropion a administré oralement à des rats enceintes à des doses allant jusqu'à 150 mg / kg / jour (environ 4 fois le MRHD sur une base Mg / m²) de l'implantation embryonnaire par lactation n'a eu aucun effet sur la croissance ou le développement des chiots.
Lactation
Résumé des risques
Données from published literature report the presence of bupropion and its metabolites in human milk (see Données ). There are no data on the effects of bupropion or its metabolites on milk production. Limited data from postmarketing reports have not identified a clear association of adverse reactions in the breastfed infant. The developmental and health benefits of breastfeeding should be considered along with the mother's clinical need for Wellbutrin SR and any potential adverse effects on the breastfed child from Wellbutrin SR or from the underlying maternal condition.
Données
Dans une étude de lactation de 10 femmes, des niveaux de bupropion dosés par voie orale et ses métabolites actifs ont été mesurés dans le lait exprimé. L'exposition quotidienne moyenne du nourrisson (en supposant une consommation quotidienne de 150 ml / kg) au bupropion et à ses métabolites actifs était de 2% de la dose ajustée en poids maternelle. Les rapports de commercialisation ont décrit les crises chez les nourrissons allaités. La relation entre l'exposition au bupropion et ces crises n'est pas claire.
Usage pédiatrique
La sécurité et l'efficacité de la population pédiatrique n'ont pas été établies [voir Avertissement en boîte AVERTISSEMENTS AND PRÉCAUTIONS ].
Utilisation gériatrique
Sur les environ 6000 sujets qui ont participé à des essais cliniques avec des comprimés à libération prolongée de bupropion (essais de dépression et de sevrage tabagique) 275 ont été âgés de ≥ 65 ans et 47 étaient âgés de ≥ 75 ans. De plus, plusieurs centaines de sujets âgés de ≥ 65 ans ont participé à des essais cliniques en utilisant la formulation à libération immédiate du bupropion (essais de dépression). Aucune différence globale de sécurité ou d'efficacité n'a été observée entre ces sujets et les sujets plus jeunes. L'expérience clinique signalée n'a pas identifié de différences dans les réponses entre les patients âgés et les patients plus jeunes, mais une plus grande sensibilité de certaines personnes âgées ne peut pas être exclue.
Le bupropion est largement métabolisé dans le foie aux métabolites actifs qui sont métabolisés et excrétés par les reins. Le risque de réactions indésirables peut être plus élevé chez les patients présentant une fonction rénale altérée. Étant donné que les patients âgés sont plus susceptibles d'avoir une diminution de la fonction rénale, il peut être nécessaire de considérer ce facteur dans la sélection de la dose; il peut être utile de surveiller la fonction rénale [voir Posologie et administration Utiliser dans des populations spécifiques Pharmacologie clinique ].
Trouble rénal
Considérez une dose réduite et / ou une fréquence de dosage de la SR de la puits de puits chez les patients atteints de troubles rénaux (DFG moins de 90 ml / min). Le bupropion et ses métabolites sont dégagés de manière renommée et peuvent s'accumuler chez ces patients plus largement que d'habitude. Surveillez étroitement aux effets indésirables qui pourraient indiquer des expositions élevées au bupropion ou au métabolite [voir Posologie et administration Pharmacologie clinique ].
Trouble hépatique
Chez les patients présentant une déficience hépatique modérée à sévère (score de l'enfant-PUGH: 7 à 15) La dose maximale de Wellbutrin Sr est de 100 mg / jour ou 150 mg tous les deux jours. Chez les patients atteints d'une déficience hépatique légère (score de l'enfant-Pugh: 5 à 6) envisagez de réduire la dose et / ou la fréquence de dosage [voir Posologie et administration Pharmacologie clinique ].
Surdosage Information for Welbutrin SR
Expérience de surdose humaine
Surdosages of up to 30 grams or more of bupropion have been reported. Crise d'épilepsie was reported in approximately one-third of all cases. Other serious reactions reported with overdoses of bupropion alone included hallucinations loss of consciousness mental status changes sinus tachycardia ECG changes such as conduction disturbances (including QRS prolongation) or arrhythmias clonus myoclonus and hyperreflexia. Fièvre muscle rigidity rhabdomyolysis hypotension stupor coma and respiratory failure have been reported mainly when bupropion was part of multiple drug overdoses.
Bien que la plupart des patients soient récupérés sans décès de séquelles associés à des surdoses de bupropion seuls ont été signalés chez des patients ingérant de grandes doses de médicament. Plusieurs crises incontrôlées d'insuffisance cardiaque de la bradycardie et un arrêt cardiaque avant le décès ont été signalés chez ces patients.
Gestion de la surdosage
Consultez un centre de contrôle de poison certifié pour des conseils et des conseils à jour. Appelez le 1-800-222â1222 ou reportez-vous à www.poison.org.
Il n'y a pas d'antidotes connus pour le bupropion. En cas de surdose, fournir des soins de soutien, y compris une supervision médicale étroite et une surveillance. Considérez la possibilité d'une surdose de médicaments multiples. Assurer une oxygénation et une ventilation adéquates des voies respiratoires. Surveillez le rythme cardiaque et les signes vitaux. L'induction des vomissements n'est pas recommandée.
Contre-indications for Welbutrin SR
- Wellbutrin SR est contre-indiqué chez les patients atteints d'un trouble de crise.
- La Wellbutrin SR est contre-indiquée chez les patients présentant un diagnostic actuel ou préalable de boulimie ou d'anorexie mentale car une incidence plus élevée de crises a été observée chez ces patients traités avec la formulation à libération immédiate du bupropion [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
- Wellbutrin SR est contre-indiqué chez les patients subissant une abondance abrupte des barbituriques de benzodiazépines à l'alcool et des médicaments antiépileptiques [voir AVERTISSEMENTS AND PRÉCAUTIONS Interactions médicamenteuses ].
- L'utilisation de MAOI (destinée à traiter les troubles psychiatriques) concomitamment avec la SR de la Wellbutrin ou dans les 14 jours suivant l'arrêt du traitement avec Wellbutrin SR est contre-indiqué. Il existe un risque accru de réactions hypertensives lorsque la SR de la welbutrin est utilisée en concomitance avec les MAOI. L'utilisation de Wellbutrin SR dans les 14 jours suivant l'arrêt du traitement avec un MAOI est également contre-indiquée. Commencer le Wellbutrin SR chez un patient traité avec des MAOI réversibles tels que le linezolide ou le bleu de méthylène intraveineux est contre-indiqué [voir Posologie et administration AVERTISSEMENTS AND PRÉCAUTIONS Interactions médicamenteuses ].
- Wellbutrin SR est contre-indiqué chez les patients atteints d'hypersensibilité connue au bupropion ou à d'autres ingrédients de Wellbutrin SR. Des réactions anaphylactoïdes / anaphylactiques et le syndrome de Stevens-Johnson ont été signalés [voir AVERTISSEMENTS AND PRÉCAUTIONS ].
Pharmacologie clinique for Welbutrin SR
Mécanisme d'action
Le mécanisme exact de l'action antidépressive du bupropion n'est pas connu mais est présumé être lié aux mécanismes noradrénergiques et / ou dopaminergiques. Le bupropion est un inhibiteur relativement faible de la recapture neuronale de la noradrénaline et dopamine et n'inhibe pas la recapture de la sérotonine. Le bupropion n'inhibe pas la monoamine oxydase.
Pharmacocinétique
Le bupropion est un mélange racémique. L'activité pharmacologique et la pharmacocinétique des énantiomères individuels n'ont pas été étudiées. La demi-vie moyenne d'élimination (± ET) du bupropion après une possibilité chronique est de 21 (± 9) heures et des concentrations plasmatiques en régime permanent de bupropion sont atteintes dans les 8 jours.
Absorption
La biodisponibilité absolue du Wellbutrin SR chez l'homme n'a pas été déterminée car une formulation intraveineuse à usage humain n'est pas disponible. Cependant, il semble probable que seule une petite proportion de toute dose administrée par voie orale atteint la circulation systémique intacte. Dans les études de rats et de chiens, la biodisponibilité du bupropion variait de 5% à 20%.
Chez l'homme suivant l'administration orale de la concentration plasmatique de pic (CMAX) du pic (CMAX) du bupropion est généralement obtenu dans les 3 heures.
Dans un essai comparant l'administration chronique avec Wellbutrin SR 150 mg deux fois par jour à la formulation de libération immédiate du bupropion 100 mg 3 fois par jour, le CMAX à l'état d'équilibre pour le bupropion après l'administration de la formulation immédiate de la formulation du bupropion. L'exposition (AUC) au bupropion était équivalente pour les deux formulations. La bioequivalence a également été démontrée pour les trois principaux métabolites actifs (c'est-à-dire l'hydroxybupropion thréohydrobupropion et l'érythrohydrobupropion) pour CMAX et AUC. Ainsi, à l'état d'équilibre de la Wellbutrin SR donnée deux fois par jour et la formulation à libération immédiate du bupropion donné 3 fois par jour est essentiellement bioéquivalent pour le bupropion et les 3 métabolites quantitativement importants.
Wellbutrin SR peut être pris avec ou sans nourriture. Le bupropion CMAX et l'AUC ont été augmentés de 11% à 35% et 16% à 19% respectivement lorsque Wellbutrin SR a été administré avec de la nourriture à des volontaires sains dans trois essais. L'effet alimentaire n'est pas considéré comme cliniquement significatif.
Distribution
Les tests in vitro montrent que le bupropion est lié à 84% aux protéines plasmatiques humaines à des concentrations allant jusqu'à 200 mcg / ml. L'étendue de la liaison aux protéines du métabolite de l'hydroxybupropion est similaire à celle du bupropion; Alors que l'étendue de la liaison aux protéines du métabolite de thréohydrobupropion est d'environ la moitié de celle observée avec le bupropion.
Métabolisme
Le bupropion est largement métabolisé chez l'homme. Trois métabolites sont actifs: l'hydroxybupropion qui est formée via l'hydroxylation du groupe tert-butyle de bupropion et les isomères d'alcool amino thréohydrobupropion et érythrohydrobupropion qui sont formés via la réduction du groupe carbonyle. Les résultats in vitro suggèrent que le CYP2B6 est la principale isoenzyme impliquée dans la formation d'hydroxybupropion tandis que les enzymes du cytochrome P450 ne sont pas impliquées dans la formation de thréohydrobupropion. L'oxydation de la chaîne latérale de bupropion entraîne la formation d'un conjugué glycine d'acide méta-chlorobenzoïque qui est ensuite excrété comme le métabolite urinaire majeur. La puissance et la toxicité des métabolites par rapport au bupropion n'ont pas été entièrement caractérisées. Cependant, il a été démontré dans un test de dépistage d'antidépresseur chez la souris que l'hydroxybupropion est la moitié aussi puissante que le bupropion tandis que le trois-trébupropion et l'érythrohydrobupropion sont 5 fois moins puissants que le buprope. Cela peut être d'une importance clinique car les concentrations plasmatiques des métabolites sont aussi élevées que celles du bupropion.
Après une administration à dose unique de Wellbutrin SR chez l'homme, le CMAX de l'hydroxybupropion se produit environ 6 heures après la dose et est environ 10 fois le niveau de pointe du médicament parent à l'état d'équilibre. La demi-vie d'élimination de l'hydroxybupropion est d'environ 20 (± 5) heures et son ASC à l'état d'équilibre est environ 17 fois celle du bupropion. Les concentrations de temps à culminer pour les métabolites érythrohydrobupropion et thréohydrobupropion sont similaires à celles du métabolite de l'hydroxybupropion. Cependant, leur demi-vie d'élimination est plus longue de 33 (± 10) et 37 (± 13) heures respectivement et les AUC à l'état d'équilibre sont respectivement de 1,5 et 7 fois celle du bupropion.
Le bupropion et ses métabolites présentent une cinétique linéaire après une administration chronique de 300 à 450 mg / jour.
Élimination
Suivant l'administration orale de 200 mg de 14C-Bupropion chez l'homme 87% et 10% de la dose radioactive ont été récupérés respectivement dans l'urine et les excréments. Seulement 0,5% de la dose orale a été excrété sous forme de bupropion inchangée.
Populations spécifiques
Les facteurs ou les conditions altérant la capacité métabolique (par exemple, les maladies du foie insuffisance cardiaque congestive [CHF] médicaments concomitants, etc.), etc. L'élimination des principaux métabolites du bupropion peut être affectée par une fonction rénale ou hépatique réduite car ce sont des composés modérément polaires et sont susceptibles de subir un métabolisme ou une conjugaison supplémentaire dans le foie avant l'excrétion urinaire.
Patients souffrant de troubles rénaux
Il y a des informations limitées sur la pharmacocinétique du bupropion chez les patients souffrant de troubles rénaux. Une comparaison entre les sujets normaux et les sujets avec une insuffisance rénale terminale a démontré que le médicament parent CMAX et les valeurs AUC était comparable dans les 2 groupes tandis que l'hydroxybupropion et le thréohydrobupropion métabolites ont eu une augmentation de 2,3 et 2,8 fois dans l'AUC pour les sujets avec une insuffisance rénale finale. A second trial comparing normal subjects and subjects with moderate-to-severe renal impairment (GFR 30.9 ± 10.8 mL/min) showed that after a single 150-mg dose of sustained-release bupropion exposure to bupropion was approximately 2-fold higher in subjects with impaired renal function while levels of the hydroxybupropion and threo/erythrohydrobupropion Les métabolites (combinés) étaient similaires dans les 2 groupes. Le bupropion est largement métabolisé dans le foie à des métabolites actifs qui sont métabolisés et ensuite excrétés par les reins. L'élimination des principaux métabolites du bupropion peut être réduite par une altération de la fonction rénale. La Wellbutrin SR doit être utilisée avec prudence chez les patients souffrant de troubles rénaux et une fréquence et / ou une dose réduites doivent être envisagées [voir Utiliser dans des populations spécifiques ].
Patients souffrant de déficience hépatique
L'effet de la déficience hépatique sur la pharmacocinétique du bupropion a été caractérisé dans 2 essais à dose unique, un chez des sujets atteints d'une maladie du foie alcoolique et un chez des sujets atteints de cirrhose légère à sévère. Le premier essai a démontré que la demi-vie de l'hydroxybupropion était significativement plus longue chez 8 sujets atteints d'une maladie hépatique alcoolique que chez 8 volontaires sains (32 ± 14 heures contre 21 ± 5 heures respectivement). Bien qu'il n'ait pas été statistiquement significatif, les AUC pour le bupropion et l'hydroxybupropion étaient plus variables et avaient tendance à être plus élevés (de 53% à 57%) chez des volontaires atteints d'une maladie hépatique alcoolique. Les différences de demi-vie pour le bupropion et les autres métabolites dans les 2 groupes étaient minimes.
Le deuxième essai n'a démontré aucune différence statistiquement significative dans la pharmacocinétique du bupropion et ses métabolites actifs chez 9 sujets atteints de cirrhose hépatique légère à modérer par rapport à 8 volontaires sains. Cependant, plus de variabilité a été observée dans certains des paramètres pharmacocinétiques du bupropion (AUC Cmax et Tmax) et de ses métabolites actifs (T½) chez les sujets avec une cirrhose hépatique légère à modérer. Chez les sujets atteints de cirrhose hépatique sévère, des altérations importantes de la pharmacocinétique du bupropion et de ses métabolites ont été observées (tableau 5).
Tableau 5: Pharmacocinétique du bupropion et des métabolites chez les patients atteints de cirrhose hépatique sévère: rapport par rapport aux témoins appariés sains
| Cmax | AUC | tory | T maxa | |
| Bupropion | 1.69 | 3.12 | 1.43 | 0,5 h |
| Hydroxybupropion | 0.31 | 1.28 | 3.88 | 19 h |
| Direction / érythrohydrobupropi sur l'alcool amino | 0.69 | 2.48 | 1.96 | 20 h |
| a Différence. |
Patients souffrant de dysfonction ventriculaire gauche
Au cours d'un essai de dosage chronique avec du bupropion chez 14 sujets déprimés à dysfonction ventriculaire gauche (histoire de CHF ou un cœur élargi sur les rayons X), il n'y avait aucun effet apparent sur la pharmacocinétique du bupropion ou ses métabolites par rapport aux volontaires sains.
Âge
Les effets de l'âge sur la pharmacocinétique du bupropion et de ses métabolites n'ont pas été entièrement caractérisés, mais une exploration des concentrations de bupropion à l'état d'équilibre de plusieurs essais d'efficacité de dépression impliquant des sujets dosés dans une plage de 300 à 750 mg / jour sur un calendrier de 3 fois. Un essai pharmacocinétique à dose unique a démontré que la disposition du bupropion et de ses métabolites chez les sujets âgés était similaire à celui des sujets plus jeunes. Ces données suggèrent qu'il n'y a aucun effet important de l'âge sur la concentration de bupropion; Cependant, un autre essai de pharmacocinétique unique et à dose multiple a suggéré que les personnes âgées courent un risque accru d'accumulation de bupropion et de ses métabolites [voir Utiliser dans des populations spécifiques ].
Patients masculins et féminins
L'analyse regroupée des données pharmacocinétiques de bupropion de 90 mâles en bonne santé et 90 volontaires en bonne santé n'a révélé aucune différence liée au sexe dans les concentrations plasmatiques maximales de bupropion. L'exposition systémique moyenne (AUC) était environ 13% plus élevée chez les volontaires masculins par rapport aux femmes volontaires. La signification clinique de cette constatation est inconnue.
Fumeurs
Les effets du tabagisme sur la pharmacocinétique du bupropion ont été étudiés chez 34 volontaires sains et femmes; 17 étaient des fumeurs de cigarettes chroniques et 17 étaient des non-fumeurs. Après l'administration orale d'une seule dose de 150 mg de bupropion, il n'y avait pas de différences statistiquement significatives dans l'ASC de Cmax Half-Life Tmax ou la clairance du bupropion ou de ses métabolites actifs entre les fumeurs et les non-fumeurs.
Études d'interaction médicamenteuse
Potentiel pour les autres médicaments à affecter Wellbutrin SR: des études in vitro indiquent que le bupropion est principalement métabolisé en hydroxybupropion par le CYP2B6. Par conséquent, le potentiel existe pour les interactions médicamenteuses entre la Wellbutrin SR et les médicaments qui sont des inhibiteurs ou des inducteurs du CYP2B6. En outre, des études in vitro suggèrent que la paroxétine sertraline norfluoxetine fluvoxamine et le nelfinavir inhibent l'hydroxylation du bupropion.
Inhibiteurs du CYP2B6
Ticlopidine Clopidogrel
Dans un essai chez des volontaires mâles en bonne santé, un clopidogrel 75 mg une fois par jour ou ticlopidine 250 mg deux fois par jour, une augmentation des expositions (CMAX et AUC) de bupropion de 40% et 60% pour le clopidogrel et de 38% et 85% pour la ticlopidine respectivement. Les expositions (CMAX et AUC) de l'hydroxybupropion ont diminué respectivement de 50% et 52% par clopidogrel et 78% et 84% respectivement par la ticlopidine. On pense que cet effet est dû à l'inhibition de l'hydroxylation du bupropion catalysée par le CYP2B6.
Prasugrel
Prasugrel is a weak inhibitor of CYP2B6. In healthy subjects prasugrel increased bupropion Cmax and AUC values by 14% and 18% respectively and decreased Cmax and AUC values of hydroxybupropion an active metabolite of bupropion by 32% and 24% respectively.
Cimétidine
Le métabolite de thréohydrobupropion du bupropion ne semble pas être produit par les enzymes du cytochrome P450. Les effets de l'administration concomitante de cimétidine sur la pharmacocinétique du bupropion et de ses métabolites actifs ont été étudiés chez 24 jeunes volontaires en bonne santé. Après l'administration orale de bupropion 300 mg avec et sans cimétidine 800 mg, la pharmacocinétique du bupropion et de l'hydroxybupropion n'a pas été affectée. Cependant, il y a eu des augmentations de 16% et 32% de l'ASC et du CMAX respectivement des fractions combinées de Thréohydrobupropion et érythrohydrobupropion.
Citalopram
Citalopram did not affect the pharmacokinetics of bupropion and its three metabolites.
Inducteurs de CYP2B6
Ritonavir et lopinavir
Dans un essai volontaire sain, le ritonavir 100 mg deux fois par jour a réduit l'ASC et le CMAX de bupropion de 22% et 21% respectivement. L'exposition du métabolite de l'hydroxybupropion a été diminuée de 23%, la thréohydrobupropion a diminué de 38% et l'érythrohydrobupropion a diminué de 48%.
Dans un deuxième essai de bénévolat sain, le ritonavir à une dose de 600 mg deux fois par jour a diminué l'ASC et le CMAX du bupropion de 66% et 62% respectivement. L'exposition du métabolite de l'hydroxybupropion a diminué de 78%, la thréohydrobupropion a diminué de 50% et l'érythrohydrobupropion a diminué de 68%.
Dans un autre essai de bénévolat sain, lopinavir 400 mg / ritonavir 100 mg deux fois par jour a diminué de 57% de Bupropion AUC et CMAX. L'AUC et le CMAX de l'hydroxybupropion ont été diminués respectivement de 50% et 31%.
Efavirenz
Dans un essai de volontaires sains, Efavirenz 600 mg une fois par jour pendant 2 semaines a réduit l'ASC et le CMAX de bupropion d'environ 55% et 34% respectivement. L'ASUC â
Phénobarbital de carbamazépine phénytoïne
Bien qu'il n'ait pas été systématiquement étudié, ces médicaments peuvent induire le métabolisme du bupropion.
Potentiel de Wellbutrin SR pour affecter d'autres médicaments
Les données sur les animaux ont indiqué que le bupropion peut être un inducteur des enzymes de métabolisation des médicaments chez l'homme. Dans un essai après l'administration chronique de bupropion 100 mg trois fois par jour à 8 volontaires masculins en bonne santé pendant 14 jours, il n'y avait aucune preuve d'induction de son propre métabolisme. Néanmoins, il peut y avoir un potentiel d'altérations cliniquement importantes des taux sanguins des médicaments co-administrés.
Médicaments métabolisés par CYP2D6
Le bupropion in vitro et ses métabolites (érythrohydrobupropion thréohydrobupropion hydroxybupropion) sont des inhibiteurs du CYP2D6. Dans un essai clinique de 15 sujets masculins (âgés de 19 à 35 ans) qui étaient de vastes métaboliseurs de bupropion CYP2D6 300 mg / jour suivis d'une dose unique de 50 mg desipramine ont augmenté le CMAX AUC et T½ de la desipramine en moyenne d'environ 2 à 5 et 2 et 2 fois. L'effet était présent pendant au moins 7 jours après la dernière dose de bupropion. L'utilisation concomitante de bupropion avec d'autres médicaments métabolisés par CYP2D6 n'a pas été officiellement étudiée.
Citalopram
Bien que le citalopram ne soit pas principalement métabolisé par le CYP2D6 dans un essai, le bupropion a augmenté le CMAX et l'AUC du citalopram de 30% et 40% respectivement.
Lamotrigine
Plusieurs doses orales de bupropion n'ont eu aucun effet statistiquement significatif sur la pharmacocinétique à dose unique de la lamotrigine chez 12 volontaires sains.
Digoxine
Les données de la littérature ont montré que l'exposition à la digoxine a été diminuée lorsqu'une dose orale unique de 0,5 mg de digoxine a été administrée 24 heures après une seule dose orale de bupropion de 150 mg à libération prolongée chez des volontaires sains.
Études cliniques
L'efficacité de la formulation à libération immédiate du bupropion dans le traitement du trouble dépressif majeur a été établie dans deux essais contrôlés par un placebo de 4 semaines chez les patients hospitalisés adultes avec MDD (essais 1 et 2 dans le tableau 6) et dans un essai contrôlé par un placebo de 6 semaines chez les patients externes adultes avec MDD (essai 3 dans le tableau 6). Dans le premier essai, la plage de dose de bupropion était de 300 mg à 600 mg / jour administrée en doses divisées; 78% des sujets ont été traités avec des doses de 300 mg à 450 mg / jour. Cet essai a démontré l'efficacité de la formulation immédiate à libération de bupropion par l'échelle totale de la dépression de Hamilton (HDRS) Score de l'humeur déprimée HDRS (point 1) et le score de gravité des impressions mondiales cliniques (CGI). Le deuxième essai comprenait 2 doses de formulation à libération immédiate du bupropion (300 et 450 mg / jour) et du placebo. Cet essai a démontré l'efficacité de la formulation à libération immédiate du bupropion mais uniquement à la dose de 450 mg / jour. Les résultats de l'efficacité ont été significatifs pour le score total HDRS et le score CGI-S mais pas pour le HDRS, le point 1. Dans le troisième essai, les patients externes ont été traités avec 300 mg / jour de la formulation à libération immédiate du bupropion. Cet essai a démontré l'efficacité de la formulation à libération immédiate du bupropion, mesurée par le score total HDRS, le HDRS Point 1 L'échelle de notation de dépression de Montgomery-Asberg (MADRS) Le score CGI-S et le score de l'échelle CGI-Improvation (CGI-I).
Tableau 6: Efficacité du bupropion à libération immédiate pour le traitement du trouble dépressif majeur
| Numéro d'essai | Groupe de traitement | Mesure d'efficacité primaire: HDRS | ||
| Score de base moyen (SD) | Score moyen LS à la visite de point final (SE) | Placebo-subtracted Differencea (95% là-bas) | ||
| Procès 1 | Bupropion à libération immédiate 300-600 mg / jourb (n = 48) | 28,5 (5.1) | 14.9 (1.3) | -4.7 (-8,8 -0,6) |
| Placebo (n = 27) | 29.3 (7.0) | 19.6 (1.6) | — | |
| Score de base moyen (SD) | LS MANGE CHANGE de la ligne de base (SE) | Placebo-subtracted Differencea (95% là-bas) | ||
| Procès 2 | Bupropion à libération immédiate 300 mg / jour (n = 36) | 32.4 (5.9) | -15.5 (1.7) | -4.1 |
| Bupropion à libération immédiate 450 mg / jourb (n = 34) | 34.8 (4.6) | -17.4 (1.7) | -5.9 (-10,5 -1,4) | |
| Placebo (n = 39) | 32.9 (5.4) | -11,5 (1.6) | — | |
| Procès 3 | Bupropion à libération immédiate 300 mg / jourb (n = 110) | 26,5 (4.3) | -12.0 (que) | -3.9 (-5.7 -1.0) |
| Placebo (n = 106) | 27.0 (3.5) | -8,7 (que) | - | |
| N: taille de l'échantillon; SD: écart-type; SE: erreur standard; LS signifie: les moindres carrés moyens; IC: Intervalle de confiance non ajusté inclus pour les doses qui se sont révélées efficaces; NA: Non disponible. a Différence (médicament moins placebo) dans les estimations des moindres carrés par rapport au paramètre d'efficacité primaire. Pour l'essai 1, il fait référence au score moyen lors de la visite du point final; Pour les essais 2 et 3, il fait référence au changement moyen de la ligne de base à la visite du point final. b Les doses qui sont démontrées sont statistiquement significativement supérieures au placebo. |
Bien qu'il n'y ait pas encore encore d'essais indépendants démontrant que l'efficacité antidépressive de la formulation à libération prolongée des essais de bupropion a démontré la bioéquivalence des formes de bupropion à libération immédiate et à libération dur bupropion en ce qui concerne le taux et l'étendue de l'absorption pour le médicament parent et les métabolites.
Dans un essai à plus long terme, les patients externes répondant aux critères DSM-IV pour les principaux troubles dépressifs de type récurrent qui avaient répondu lors d'un essai ouvert de 8 semaines sur Wellbutrin SR (150 mg twice par jour) ont été randomisés à la poursuite de leur même dose de relances. La réponse pendant la phase ouverte a été définie comme un score d'amélioration CGI de 1 (très amélioré) ou 2 (beaucoup amélioré) pour chacune des 3 dernières semaines. La rechute pendant la phase en double aveugle a été définie comme le jugement de l'investigateur selon lequel un traitement médicamenteux était nécessaire pour aggraver les symptômes dépressifs. Les patients recevant un traitement continu avec Wellbutrin SR ont connu des taux de rechute significativement inférieurs au cours des 44 semaines suivantes par rapport à celles recevant un placebo.
Informations sur les patients pour Wellbutrin SR
Wellbutrin SR
(Eh bien BYU-Trin)
(chlorhydrate de bupropion) Comprimés à libération prolongée
Important: assurez-vous de lire les trois sections de ce guide de médicaments. La première section concerne le risque de pensées et d'actions suicidaires avec des antidépresseurs; La deuxième section concerne le risque de changements dans la pensée et le comportement de la dépression et des pensées ou des actions suicidaires avec les médicaments utilisés pour arrêter de fumer; Et la troisième section est intitulée Quelles autres informations importantes devrais-je savoir sur Wellbutrin SR?
Dépression des médicaments antidépresseurs et autres maladies mentales graves et pensées ou actions suicidaires
Cette section du guide des médicaments ne concerne que le risque de pensées suicidaires et d'actions avec des médicaments antidépresseurs.
Quelles sont les informations les plus importantes que je devrais connaître sur la dépression des médicaments antidépresseurs et d'autres maladies mentales graves et des pensées ou des actions suicidaires?
1. Les médicaments antidépresseurs peuvent augmenter le risque de pensées ou d'actions suicidaires chez certains enfants adolescents ou jeunes adultes au cours des premiers mois de traitement.
2. La dépression ou d'autres maladies mentales graves sont les causes les plus importantes des pensées et des actions suicidaires. Certaines personnes peuvent avoir un risque particulièrement élevé d'avoir des pensées ou des actions suicidaires. Il s'agit notamment des personnes qui ont (ou qui ont une histoire familiale de maladie bipolaire (également appelée maladie maniaco-dépressive) ou des pensées ou des actions suicidaires.
3. Comment puis-je surveiller et essayer d'empêcher les pensées et les actions suicidaires en moi-même ou un membre de la famille?
- Portez une attention particulière à tout changement, en particulier les changements soudains dans les pensées ou les sentiments des comportements de l'humeur. Ceci est très important lorsqu'un médicament antidépresseur est démarré ou lorsque la dose est modifiée.
- Appelez immédiatement votre fournisseur de soins de santé pour signaler des changements nouveaux ou soudains dans les pensées ou les sentiments du comportement de l'humeur.
- Gardez toutes les visites de suivi avec votre fournisseur de soins de santé comme prévu. Appelez le fournisseur de soins de santé entre les visites au besoin, surtout si vous avez des inquiétudes concernant les symptômes.
Appelez votre fournisseur de soins de santé immédiatement si vous ou votre membre de votre famille avez l'un des symptômes suivants, surtout s'ils sont nouveaux pires ou vous inquiétez:
- Réflexions sur le suicide ou la mort
- Difficulté à dormir (insomnia)
- tente de se suicider
- irritabilité nouvelle ou pire
- Dépression nouvelle ou pire
- Agir agressif étant en colère ou violent
- Anxiété nouvelle ou pire
- Agissant sur des impulsions dangereuses
- Se sentir très agité ou agité
- Une augmentation extrême de l'activité et de la parole (manie)
- crises de panique
- Autres changements inhabituels dans le comportement ou l'humeur
De quoi d'autre dois-je savoir sur les médicaments antidépresseurs?
- N'arrêtez jamais un médicament antidépresseur sans d'abord parler à un fournisseur de soins de santé. L'arrêt d'un médicament antidépresseur peut soudainement provoquer d'autres symptômes.
- Les antidépresseurs sont des médicaments utilisés pour traiter la dépression et d'autres maladies. Il est important de discuter de tous les risques de traitement de la dépression et des risques de ne pas le traiter. Les patients et leurs familles ou autres soignants devraient discuter de tous les choix de traitement avec le fournisseur de soins de santé et pas seulement l'utilisation d'antidépresseurs.
- Les médicaments antidépresseurs ont d'autres effets secondaires. Parlez au fournisseur de soins de santé des effets secondaires du médicament prescrit à vous ou à un membre de votre famille.
- Les médicaments antidépresseurs peuvent interagir avec d'autres médicaments. Connaissez tous les médicaments que vous ou le membre de votre famille prenez. Gardez une liste de tous les médicaments pour montrer le fournisseur de soins de santé. Ne démarrez pas de nouveaux médicaments sans d'abord vérifier avec votre fournisseur de soins de santé.
On ne sait pas si Wellbutrin SR est sûr et efficace chez les enfants de moins de 18 ans.
Arrêter de fumer des médicaments qui fusionnent les changements dans la pensée et le comportement de la dépression et des pensées ou des actions suicidaires
Cette section du guide des médicaments ne concerne que le risque de changements dans la pensée et le comportement de la dépression et des pensées ou des actions suicidaires avec des médicaments utilisés pour arrêter de fumer. Bien que Wellbutrin SR ne soit pas un traitement pour arrêter de fumer, il contient le même ingrédient actif (chlorhydrate de bupropion) que Zyban qui est utilisé pour aider les patients à arrêter de fumer.
Parlez à votre fournisseur de soins de santé ou à votre fournisseur de soins de santé de votre famille à propos:
- Tous les risques et avantages des médicaments-fumeurs
- Tous les choix de traitement pour arrêter de fumer
Lorsque vous essayez d'arrêter de fumer avec ou sans bupropion, vous pouvez avoir des symptômes qui peuvent être dus au retrait de la nicotine, notamment:
- inspirer de fumer
- frustration
- agitation
- humeur déprimée
- colère
- diminution de la fréquence cardiaque
- Difficulté à dormir
- Se sentir anxieux
- appétit accru
- irritabilité
- difficulté à se concentrer
- prise de poids
Certaines personnes ont même ressenti des pensées suicidaires lorsqu'ils essaient d'arrêter de fumer sans médicament. Parfois, arrêter de fumer peut entraîner une aggravation des problèmes de santé mentale que vous avez déjà comme la dépression.
Certaines personnes ont eu un effet secondaire sérieux tout en prenant du bupropion pour les aider à arrêter de fumer, notamment: Des problèmes de santé mentale nouveaux ou pires tels que les changements de comportement ou la réflexion sur l'agression de l'agression dépression de l'agitation ou des pensées ou des actions suicidaires. Certaines personnes présentaient ces symptômes lorsqu'ils ont commencé à prendre du bupropion et d'autres les ont développés après plusieurs semaines de traitement ou après l'arrêt du bupropion. Ces symptômes se sont produits plus souvent chez les personnes qui avaient des antécédents de problèmes de santé mentale avant de prendre du bupropion que chez les personnes sans antécédents de problèmes de santé mentale.
Arrêtez de prendre Wellbutrin SR et appelez votre fournisseur de soins de santé immédiatement si vous votre famille ou votre soignant remarquez l'un de ces symptômes. Travaillez avec votre fournisseur de soins de santé pour décider si vous devez continuer à prendre Wellbutrin SR. Chez de nombreuses personnes, ces symptômes ont disparu après avoir arrêté Wellbutrin SR, mais chez certaines personnes, les symptômes ont continué après l'arrêt de la Wellbutrin SR. Il est important pour vous de suivre votre fournisseur de soins de santé jusqu'à ce que vos symptômes disparaissent. Avant de prendre Wellbutrin SR, dites à votre fournisseur de soins de santé si vous avez déjà eu une dépression ou d'autres problèmes de santé mentale. Vous devriez également informer votre professionnel de la santé des symptômes que vous avez présentés à d'autres moments où vous avez essayé d'arrêter de fumer avec ou sans bupropion.
Quelles autres informations importantes devrais-je savoir sur Wellbutrin SR?
- Crise d'épilepsies: There is a chance of having a seizure (convulsion fit) with Wellbutrin SR especially in people:
- avec certains problèmes médicaux.
- qui prennent certains médicaments.
Les chances d'avoir des crises augmentent avec des doses plus élevées de Wellbutrin SR. Pour plus d'informations, voir les sections qui ne devraient pas prendre Wellbutrin SR? Et que dois-je dire à mon fournisseur de soins de santé avant de prendre Wellbutrin SR? Parlez à votre fournisseur de soins de santé de toutes vos conditions médicales et de tous les médicaments que vous prenez. Ne prenez pas d'autres médicaments pendant que vous prenez Wellbutrin SR à moins que votre fournisseur de soins de santé n'ait dit qu'il était normal de les prendre.
Si vous avez une crise tout en prenant Wellbutrin SR, arrêtez de prendre les comprimés et appelez immédiatement votre fournisseur de soins de santé. Ne reprenez pas à nouveau Wellbutrin SR si vous avez une crise.
- Hypertension artérielle (hypertension). Certaines personnes ont une pression artérielle élevée qui peut être grave tout en prenant Wellbutrin SR. Les risques d'hypertension artérielle peuvent être plus élevés si vous utilisez également une thérapie de remplacement de la nicotine (comme un patch de nicotine) pour vous aider à arrêter de fumer (voir la section de ce guide de médicament appelé Comment dois-je prendre Wellbutrin SR?).
- Épisodes maniaques. Certaines personnes peuvent avoir des périodes de manie tout en prenant Wellbutrin SR, notamment:
- Énergie considérablement augmentée
- De graves problèmes de sommeil
- Pensées de course
- Comportement téméraire
- Idées inhabituellement grandes
- Bonheur excessif ou irritabilité
- Parler de plus ou de plus vite que d'habitude
Si vous avez l'un des symptômes ci-dessus de Mania, appelez votre fournisseur de soins de santé.
- Pensées ou comportements inhabituels. Certains patients ont des pensées ou des comportements inhabituels tout en prenant Wellbutrin SR, y compris les délires (croyez que vous êtes quelqu'un d'autre) les hallucinations (voir ou entendre des choses qui ne sont pas là) paranoïa (sentant que les gens sont contre vous) ou se sentent confus. Si cela vous arrive, appelez votre fournisseur de soins de santé.
- Problèmes visuels.
- douleurs oculaires
- changements de vision
- gonflement ou rougeur dans ou autour de l'œil
Seules certaines personnes sont à risque de ces problèmes. Vous voudrez peut-être subir un examen de la vue pour voir si vous êtes à risque et recevoir un traitement préventif si vous l'êtes.
- Réactions allergiques graves. Certaines personnes peuvent avoir des réactions allergiques graves à Wellbutrin SR. Arrêtez de prendre Wellbutrin SR et appelez votre fournisseur de soins de santé tout de suite Si vous obtenez une éruption cutanée des ruches qui démangent la fièvre des glandes lymphatiques gonflées des plaies douloureuses dans la bouche ou autour des yeux gonflant les lèvres ou la douleur de la poitrine ou avez du mal à respirer. Ce pourraient être des signes d'une réaction allergique grave.
Qu'est-ce que Wellbutrin SR?
Wellbutrin SR is a prescription medicine used to treat adults with a certain type of dépression called major depressive disorder.
Qui ne devrait pas prendre Wellbutrin SR?
Ne prenez pas Wellbutrin SR si vous
- avoir ou souffrir d'un trouble de crise ou d'une épilepsie.
- avoir ou souffrir d'un trouble de l'alimentation comme l'anorexie mentale ou la boulimie.
- prennent tout autre médicament contenant du bupropion, y compris Zyban (utilisé pour aider les gens à arrêter de fumer) Wellbutrin Wellbutrin XL aplenzin ou Forfivo XL. Bupropion is the same active ingredient that is in Wellbutrin SR.
- Buvez beaucoup d'alcool et arrêtez brusquement de boire ou utilisez des médicaments appelés sédatifs (ceux-ci vous rendent somnolent) des benzodiazépines ou des médicaments anti-séparation et vous cessez de les utiliser tout d'un coup.
- Prenez un inhibiteur de la monoamine oxydase (MAOI). Demandez à votre fournisseur de soins de santé ou à votre pharmacien si vous ne savez pas si vous prenez un MAOI, y compris le linezolide antibiotique.
- Ne prenez pas de MAOI dans les 2 semaines suivant l'arrêt de Wellbutrin SR, sauf indication contraire de le faire par votre fournisseur de soins de santé.
- Ne commencez pas Wellbutrin SR si vous avez cessé de prendre un MAOI au cours des 2 dernières semaines, sauf indication contraire de le faire par votre fournisseur de soins de santé.
- sont allergiques à l'ingrédient actif dans le bupropion Wellbutrin SR ou à l'un des ingrédients inactifs. Voir la fin de ce guide de médicaments pour une liste complète des ingrédients dans Wellbutrin SR.
Que dois-je dire à mon fournisseur de soins de santé avant de prendre Wellbutrin SR?
Dites à votre fournisseur de soins de santé si vous avez déjà eu des pensées ou des actions suicidaires de dépression ou d'autres problèmes de santé mentale. Voir la dépression des médicaments antidépresseurs et d'autres maladies mentales graves et des pensées ou des actions suicidaires.
- Parlez à votre fournisseur de soins de santé de vos autres conditions médicales, y compris si vous:
- ont des problèmes hépatiques, en particulier la cirrhose du foie.
- avoir des problèmes rénaux.
- ont ou ont subi un trouble de l'alimentation comme l'anorexie mentale ou la boulimie.
- ont subi une blessure à la tête.
- ont eu une crise (convulsion ajustée).
- avoir une tumeur dans votre système nerveux (cerveau ou colonne vertébrale).
- ont eu un crise cardiaque problèmes cardiaques ou pression artérielle élevée.
- sont un diabétique prenant de l'insuline ou d'autres médicaments pour contrôler votre glycémie.
- boire de l'alcool.
- abuser des médicaments sur ordonnance ou des médicaments de rue.
- sont enceintes ou prévoient de devenir enceintes. Parlez à votre fournisseur de soins de santé du risque pour votre bébé à naître si vous prenez Wellbutrin SR pendant la grossesse.
- Dites à votre fournisseur de soins de santé si vous devenez enceinte ou si vous pensez que vous êtes enceinte pendant le traitement avec Wellbutrin SR.
- Si vous tombez enceinte pendant le traitement avec Wellbutrin SR, parlez à votre fournisseur de soins de santé de l'inscription auprès du National Grossancy Registry pour les antidépresseurs. Vous pouvez vous inscrire en appelant le 1-844-405-6185.
- allaitent ou prévoient d'allaiter pendant le traitement avec Wellbutrin SR. Wellbutrin Sr passe dans votre lait. Parlez à votre fournisseur de soins de santé de la meilleure façon de nourrir votre bébé pendant le traitement avec Wellbutrin SR.
Parlez à votre fournisseur de soins de santé de tous les médicaments que vous prenez y compris les médicaments en vente libre sur ordonnance des vitamines et des suppléments à base de plantes. De nombreux médicaments augmentent vos chances d'avoir des convulsions ou d'autres effets secondaires graves si vous les prenez pendant que vous prenez Wellbutrin SR.
Comment dois-je prendre Wellbutrin SR?
- Prenez Wellbutrin SR exactement comme prescrit par votre fournisseur de soins de santé. Ne changez pas votre dose ou n'arrêtez pas de prendre Wellbutrin SR sans parler d'abord à votre fournisseur de soins de santé.
- Avalez les comprimés Wellbutrin Sr entiers. Ne mâchez pas ou n'écrasez pas les comprimés Wellbutrin SR. Si vous faites, le médicament sera libéré dans votre corps trop rapidement. Si cela se produit, vous pouvez être plus susceptible d'obtenir des effets secondaires, y compris des crises. Dites à votre fournisseur de soins de santé si vous ne pouvez pas avaler des comprimés.
- Wellbutrin SR tablets may have an odor. This is normal.
- Prenez Wellbutrin SR en même temps chaque jour.
- Prenez vos doses de Wellbutrin SR à au moins 8 heures d'intervalle.
- Vous pouvez prendre Wellbutrin SR avec ou sans nourriture.
- Si vous manquez une dose, ne prenez pas une dose supplémentaire pour compenser la dose que vous avez manquée. Attendez et prenez votre prochaine dose à l'heure régulière. C'est très important. Trop de Wellbutrin SR peut augmenter vos chances d'avoir une crise.
- Si vous prenez trop de Wellbutrin SR ou une surdose, appelez immédiatement votre salle d'urgence ou votre centre de contrôle du poison local.
- Ne prenez aucun autre médicament en prenant Wellbutrin SR à moins que votre professionnel de la santé ne vous ait dit que tout allait bien.
- Si vous prenez Wellbutrin SR pour le traitement du trouble dépressif majeur, cela peut vous prendre plusieurs semaines pour penser que Wellbutrin SR fonctionne. Une fois que vous vous sentez mieux, il est important de continuer à prendre Wellbutrin SR exactement comme indiqué par votre fournisseur de soins de santé. Appelez votre fournisseur de soins de santé si vous ne vous sentez pas Wellbutrin SR fonctionne pour vous.
Que dois-je éviter en prenant Wellbutrin SR?
- Limiter ou éviter d'utiliser de l'alcool pendant le traitement avec Wellbutrin SR. Si vous buvez habituellement beaucoup d'alcool, parlez avec votre fournisseur de soins de santé avant de vous arrêter soudainement. Si vous arrêtez soudainement de boire de l'alcool, vous pouvez augmenter vos chances d'avoir des crises.
- Ne conduisez pas de voiture et n'utilisez pas de machines lourdes tant que vous ne savez pas comment Wellbutrin SR vous affecte. Wellbutrin SR peut affecter votre capacité à faire ces choses en toute sécurité.
Quels sont les effets secondaires possibles de Wellbutrin SR?
Wellbutrin SR can cause serious side effects. See the sections at the beginning of this Guide des médicaments for information about serious side effects of WELLBUTRIN.
Les effets secondaires les plus courants de Wellbutrin SR comprennent:
- mal de tête
- vertiges
- bouche sèche
- mal de gorge
- nausée
- constipation
- Difficulté à dormir
Si vous avez des nausées, prenez vos médicaments avec de la nourriture. Si vous avez du mal à dormir, ne vous approchez pas de votre médicament.
Dites immédiatement votre fournisseur de soins de santé des effets secondaires qui vous dérangent.
Ce ne sont pas tous les effets secondaires possibles de Wellbutrin SR. Pour plus d'informations, demandez à votre fournisseur de soins de santé ou à votre pharmacien.
Appelez votre médecin pour des conseils médicaux sur les effets secondaires. Vous pouvez signaler les effets secondaires à la FDA au 1-800-FDA-1088.
Vous pouvez également signaler les effets secondaires à GlaxoSmithKline au 1-888-825-5249.
Comment dois-je stocker Wellbutrin SR?
- Stocker Wellbutrin SR à température ambiante entre 68 ° F et 77 ° F (20 ° C à 25 ° C).
- Gardez Wellbutrin SR à sec et hors de la lumière.
Gardez Wellbutrin SR et tous les médicaments hors de portée des enfants.
Informations générales sur l'utilisation sûre et efficace de Wellbutrin SR.
Les médicaments sont parfois prescrits à des fins autres que celles énumérées dans un guide de médicaments. N'utilisez pas Wellbutrin SR pour une condition pour laquelle il n'a pas été prescrit. Ne donnez pas Wellbutrin SR à d'autres personnes même si elles présentent les mêmes symptômes que vous. Cela peut leur faire du mal.
Si vous passez un test de dépistage des médicaments d'urine Wellbutrin SR peut rendre le résultat de test positif pour les amphétamines. Si vous dites à la personne qui vous donne le test de dépistage des médicaments que vous prenez Wellbutrin SR, il peut effectuer un test de dépistage de médicaments plus spécifique qui ne devrait pas avoir ce problème.
Ce guide de médicaments résume des informations importantes sur Wellbutrin SR. Si vous souhaitez plus d'informations, parlez avec votre fournisseur de soins de santé. Vous pouvez demander à votre fournisseur de soins de santé ou à votre pharmacien d'information sur Wellbutrin SR qui est écrit pour les professionnels de la santé. Pour plus d'informations sur Wellbutrin SR, appelez le 1-888-825-5249.
Quels sont les ingrédients de Wellbutrin SR?
Ingrédient actif: chlorhydrate de bupropion.
Ingrédients inactifs: Hydrochloride de cystéine de cire de carnauba Hypromellose Magnésium stéarate microcristallin cellulose polyéthylène glycol polysorbate 80 et dioxyde de titane. Les tablettes sont imprimées avec de l'encre noire comestible. De plus, la tablette de 100 mg contient FD
Ce guide de médicaments a été approuvé par la Food and Drug Administration des États-Unis.