Rhumatrex
Les Informations Présentées Sur Ce Site Ne Constituent Pas Un Avis Médical. Nous Ne Vendons Rien. L'Exactitude De La Traduction N'Est Pas Garantie. Clause De Non-Responsabilité
Résumé
Qu'est-ce que Rheumatrex?
Rhumatrex (méthotrexate) est un médicament antimétabolite qui est utilisé pour traiter certains cancers de graves maladies cutanées telles que sévères psoriasis et traiter les formes de polyarthrite rhumatoïde. Rhumatrex est disponible en générique formulaire.
Quels sont les effets secondaires de Rhumatrex?
Les effets secondaires de Rheumatrex comprennent:
- Inflammation des lèvres et de la bouche
- nausée
- vomissement
- estomac renversé
- douleurs abdominales
- vertiges
- sentiment fatigué
- mal de tête
- Saignement de vos gencives
- vision floue et
- Nombre faible de cellules blanches dans le sang (leukopénie).
Dites à votre médecin si vous avez des effets secondaires graves de Rhumatrex, notamment:
Qu'est-ce que le cytomel est utilisé pour traiter
- toux à sec
- essoufflement;
- diarrhée
- plaques ou plaies blanches à l'intérieur de votre bouche ou sur vos lèvres;
- du sang dans votre urine ou vos selles;
- uriner moins que d'habitude ou pas du tout;
- La fièvre des refroidissements du corps fait mal aux symptômes de la grippe;
- mal de gorge et maux de tête avec un épluche à cloques sévères et une éruption cutanée rouge;
- Peau pâle facile ecchymose ou faiblesse saignante;
- Perte d'appétit des selles de couleur argile d'urine foncée ou jaunisse (jaunissement de la peau ou des yeux).
Dosage pour rhumatrex
La dose de rhumatrex est conçue pour le problème de chaque patient et peut aller d'environ 7,5 mg par semaine à 30 mg par jour en fonction du processus pathologique et du jugement du médecin. Rhumatrex a été utilisé chez les enfants atteints de rhumatoïde juvénile arthrite et les doses ont été individualisées.
Quelles substances ou suppléments de médicaments interagissent avec Rhumatrex?
Rhumatrex peut interagir avec les rétinoïdes azathioprine chloramphénicol hydroxychloroquine stéroïdes médicaments sulfa phénytoïne probénécide tétracycline théophylline Traitements de l'or oral médicaments antibiotiques pénicillinaires pour les médicaments contre l'acide de l'estomac (anti-inflammatoires anti-inflammatoires). Dites à votre médecin tous les médicaments et suppléments que vous utilisez.
Rhumatrex pendant la grossesse et l'allaitement
Rhumatrex ne doit pas être utilisé chez les femmes enceintes ou allaitées.
Informations Complémentaires
Notre centre de médicaments sur les effets secondaires de Rheumatrex offre une vue complète des informations sur les médicaments disponibles sur les effets secondaires potentiels lors de la prise de ce médicament.
Informations sur les médicaments de la FDA
- Description de la drogue
- Indications
- Dosage
- Effets secondaires
- Interactions médicamenteuses
- Avertissements
- Surdosage
- Contre-indications
- Pharmacologie clinique
- Guide des médicaments
AVERTISSEMENT
Le méthotrexate ne doit être utilisé que par les médecins dont les connaissances et l'expérience incluent l'utilisation d'un traitement antimétabolite en raison de la possibilité de réactions toxiques graves (qui peuvent être fatales):
Le méthotrexate ne doit être utilisé que dans les maladies néoplasiques mettant la vie en danger ou chez les patients atteints de psoriasis ou de polyarthrite rhumatoïde atteinte d'une maladie invalidante récalcitrante sévère qui n'est pas suffisamment sensible à d'autres formes de thérapie.
Des décès ont été signalés avec l'utilisation de méthotrexate dans le traitement du psoriasis maligne et de la polyarthrite rhumatoïde. Les patients doivent être étroitement surveillés pour les toxicités du poumon du foie et des reins de la moelle osseuse. (Voir PRÉCAUTIONS .)
Les patients doivent être informés par leur médecin des risques impliqués et être soumis aux soins d'un médecin tout au long de la thérapie.
- Il a été rapporté que le méthotrexate provoque la mort fœtale et / ou les anomalies congénitales. Par conséquent, il n'est pas recommandé pour les femmes de potentiel de procréation, sauf s'il existe des preuves médicales claires que les avantages peuvent l'emporter sur les risques considérés. Les femmes enceintes atteints de psoriasis ou de polyarthrite rhumatoïde ne devraient pas recevoir de méthotrexate. (Voir Contre-indications .)
- L'élimination du méthotrexate est réduite chez les patients atteints d'ascite altérée de la fonction rénale ou des épanchements pleuraux. Ces patients nécessitent une surveillance particulièrement minutieuse de la toxicité et nécessitent une réduction de la dose ou dans certains cas d'arrêt de l'administration de méthotrexate.
- Une suppression de la moelle osseuse inattendue (parfois mortelle), l'anémie aplasique et la toxicité gastro-intestinale ont été signalées avec une administration concomitante de méthotrexate (généralement en dose élevée) ainsi que certains médicaments anti-inflammatoires non stéroïdiens (NSIDS). (Voir PRÉCAUTIONS: Interactions médicamenteuses .)
- Le méthotrexate provoque une fibrose et une cirrhose de l'hépatotoxicité, mais généralement seulement après une utilisation prolongée. Des élévations enzymes hépatiques aiguës sont fréquemment observées. Ceux-ci sont généralement transitoires et asymptomatiques et ne semblent pas non plus prédictifs d'une maladie hépatique ultérieure. La biopsie hépatique après une utilisation soutenue montre souvent des changements histologiques et la fibrose et la cirrhose ont été rapportées; Ces dernières lésions peuvent ne pas être précédées de symptômes ou de tests de fonction hépatique anormaux dans la population de psoriasis. Pour cette raison, les biopsies hépatiques périodiques sont généralement recommandées pour les patients psoriasiques qui sont sous traitement à long terme. Des anomalies persistantes dans les tests de la fonction hépatique peuvent précéder l'apparition de la fibrose ou de la cirrhose dans la population de polyarthrite rhumatoïde. (Voir PRÉCAUTIONS Toxicité du système d'organes Hépatique .)
- La maladie pulmonaire induite par le méthotrexate est une lésion potentiellement dangereuse qui peut se produire de manière aiguë à tout moment pendant le traitement et qui a été signalée à des doses aussi faibles que 7,5 mg / semaine. Ce n'est pas toujours entièrement réversible. Les symptômes pulmonaires (en particulier une toux sèche non productive) peuvent nécessiter une interruption du traitement et une enquête minutieuse.
- La diarrhée et la stomatite ulcéreuse nécessitent une interruption du traitement; Sinon, une entérite hémorragique et la mort par perforation intestinale peuvent se produire.
- Les lymphomes malins qui peuvent régresser après le retrait du méthotrexate peuvent survenir chez les patients recevant du méthotrexate à faible dose et peuvent donc ne pas nécessiter un traitement cytotoxique. Arrêtez d'abord Metho Trexate et si le lymphome ne régresse pas le traitement approprié doit être institué.
- Comme d'autres médicaments cytotoxiques, le méthotrexate peut induire un syndrome de lyse tumorale chez les patients atteints de tumeurs en croissance rapide. Des mesures de soutien appropriées et pharmacologiques peuvent empêcher ou soulager cette complication.
- Des réactions cutanées de temps parfois mortelles ont été rapportées après des doses uniques ou multiples de méthotrexate. Des réactions se sont produites quelques jours suivant l'administration de méthotrexate intraveineuse ou intrathécale intramusculaire orale. La récupération a été signalée avec l'arrêt du traitement. (Voir PRÉCAUTIONS Toxicité du système d'organes Peau .)
- Les infections opportunistes potentiellement mortelles, en particulier la pneumonie de Pneumocystis carinii, peuvent survenir avec un traitement par méthotrexate.
- Le méthotrexate donné en même temps que la radiothérapie peut augmenter le risque de nécrose des tissus mous et d'ostéonécrose.
Description de Rheumatrex
Le méthotrexate (anciennement l'améthoptérine) est un antimétabolite utilisé dans le traitement de certaines maladies néoplasiques du psoriasis sévère et de la polyarthrite rhumatoïde adulte.
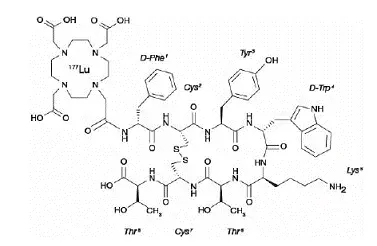
Le méthotrexate chimiquement est n- [4 - [[(24-diamino-6-pteridinyl) méthyl] méthylamino] benzoyl] -l-glutamique. La formule structurelle est:
 |
Poids moléculaire: 454,4520H22N8O5
Les comprimés de méthotrexate USP pour l'administration orale sont disponibles dans un système d'emballage désigné comme les comprimés de méthotrexate Rhumatrex® Pack de dose USP pour le traitement avec un calendrier de dosage hebdomadaire de 5 mg 7,5 mg 10 mg 12,5 mg 15 mg 17,5 mg et 20 mg. Les comprimés de méthotrexate USP contiennent une quantité de méthotrexate de sodium équivalent à 2,5 mg de méthotrexate et les ingrédients inactifs suivants: stéarate de magnésium de lactose et amidon prégelatinisé.
Utilisations pour rhumatrex
Maladies néoplasiques
Le méthotrexate est indiqué dans le traitement du choriocarcinome gestationnel chorioadénome destruens et taupe hydatidiforme.
Le méthotrexate est utilisé en traitement d'entretien en combinaison avec d'autres agents chimiothérapeutiques.
Le méthotrexate est utilisé seul ou en combinaison avec d'autres agents anticancéreux dans le traitement des cancers épidermoïdes du cancer du sein des fungoides de mycose avancés par la tête et le cou (lymphome cutané) et le cancer du poumon en particulier les cellules squameuses et les petits types de cellules. Le méthotrexate est également utilisé en combinaison avec d'autres agents chimiothérapeutiques dans le traitement des lymphomes non hodgkiniens avancés.
Psoriasis
Le méthotrexate est indiqué dans le contrôle symptomatique du psoriasis invalidante récalcitrante sévère qui ne répond pas adéquatement à d'autres formes de thérapie mais seulement lorsque le diagnostic a été établi comme par biopsie et / ou après une consultation dermatologique . Il est important de s'assurer qu'une poussée de psoriasis n'est pas due à une maladie concomitante non diagnostiquée affectant les réponses immunitaires.
Polyarthrite rhumatoïde, y compris la polyarthrite rhumatoïde juvénile à cours polyarticulaire
Le méthotrexate est indiqué dans la prise en charge d'adultes sélectionnés atteints de polyarthrite rhumatoïde active sévère (critères ACR) ou d'enfants atteints de polyarthrite rhumatoïde juvénile active à des fins polyarticulaires qui ont eu une réponse thérapeutique insuffisante à ou sont induïdes d'un essai adéquat de premier essai (nsAints).
Les AINS d'aspirine et / ou les stéroïdes à faible dose peuvent être poursuivis, bien que la possibilité d'une toxicité accrue avec l'utilisation concomitante d'AINS, y compris des salicylates, n'a pas été entièrement explorée. (Voir PRÉCAUTIONS: Interactions médicamenteuses .) Steroids may be reduced gradually in patients who respond to methotrexate. Combined use of methotrexate with gold penicillamine hydroxychloroquine sulfasalazine or cytotoxic agents has not been studied et may increase the incidence of adverse effects. Rest et physiotherapy as indicated should be continued.
Dosage pour rhumatrex
Maladies néoplasiques
L'administration orale sous forme de comprimé est souvent préférée lorsque de faibles doses sont administrées car l'absorption est rapide et des taux sériques efficaces sont obtenus.
Choriocarcinome et maladies trophoblastiques similaires
Le méthotrexate est administré par voie orale ou intramusculaire à des doses de 15 à 30 mg par jour pour un cours de cinq jours. Ces cours sont généralement répétés pendant 3 à 5 fois, comme l'exige les périodes de repos d'une ou plusieurs semaines interposées entre les cours jusqu'à ce que tout symptôme toxique manifestant se calment. L'efficacité de la thérapie est généralement évaluée par une analyse quantitative 24 heures sur 24 de la gonadotrophine chorionique urinaire (HCG) qui doit revenir à la normale ou moins de 50 UI / 24 heures généralement après le troisième ou quatrième parcours et être généralement suivie d'une résolution complète des lésions mesurables en 4 à 6 semaines. Un à deux cours de méthotrexate après normalisation du HCG sont généralement recommandés. Avant que chaque cours du médicament, une évaluation clinique, une affaire est essentielle. La combinaison cyclique de la thérapie du méthotrexate avec d'autres médicaments antitumorales a été signalée comme utile.
Étant donné que la taupe hydatidiforme peut précéder le choriocarcinome prophylactique chimiothérapie avec du méthotrexate a été recommandé.
Le chorioadénome destruens est considéré comme une forme invasive de taupe hydatidiforme. Le méthotrexate est administré dans ces états pathologiques à des doses similaires à celles recommandées pour le choriocarcinome.
Leucémie
La leucémie lymphoblastique aiguë chez les patients pédiatriques et les jeunes adolescents est le plus sensible à la chimiothérapie actuelle. Chez les jeunes adultes et les patients plus âgés, la rémission clinique est plus difficile à obtenir et les rechutes précoces sont plus courantes. Le méthotrexate seul ou en combinaison avec des stéroïdes a été utilisé initialement pour l'induction de la rémission dans les leucémies lymphoblastiques aiguës. Plus récemment, la corticothérapie en combinaison avec d'autres médicaments antileucémiques ou dans les combinaisons cycliques avec le méthotrexate incluses a semblé produire des rémissions rapides et efficaces. Lorsqu'il est utilisé pour l'induction de méthotrexate à des doses de 3,3 mg / m² en combinaison avec 60 mg / m² de prednisone, compte tenu des rémissions quotidiennes produites chez 50% des patients traités généralement dans une période de 4 à 6 semaines. Le méthotrexate en combinaison avec d'autres agents semble être le médicament de choix pour assurer l'entretien des rémissions induites par le médicament. Lorsque la rémission est obtenue et que des soins de soutien ont produit un traitement général de l'entretien de l'amélioration clinique sont lancés comme suit: le méthotrexate est administré 2 fois par semaine, soit par voie intramusculaire, à des doses hebdomadaires totales de 30 mg / m². Il a également été donné à des doses de 2,5 mg / kg par voie intraveineuse tous les 14 jours. Si et quand une rechute se produit, la réinduction de la rémission peut à nouveau être généralement obtenue en répétant le régime d'induction initial.
Une variété de régimes de chimiothérapie combinés ont été utilisés pour la thérapie d'induction et d'entretien dans la leucémie lymphoblastique aiguë. Le médecin doit être familier avec les nouvelles progrès de la thérapie antileucémique.
Lymphomes
Dans les stades tumoraux de Burkitt, le méthotrexate I-II a produit des rémissions prolongées dans certains cas. La posologie recommandée est de 10 à 25 mg / jour par voie orale pendant 4 à 8 jours. Au stade III, le méthotrexate est généralement donné en concomitance avec d'autres agents antitumoraux. Le traitement à toutes les étapes se compose généralement de plusieurs cours de médicament interposés avec des périodes de repos de 7 à 10 jours. Les lymphosarcomes au stade III peuvent répondre à un traitement médicamenteux combiné avec le méthotrexate donné à des doses de 0,625 à 2,5 mg / kg par jour.
Mycosis fungoides (lymphome cutané des lymphocytes T)
La thérapie avec du méthotrexate en tant qu'agent unique semble produire des réponses cliniques chez jusqu'à 50% des patients traités. Le dosage aux premiers stades est habituellement de 5 à 50 mg une fois par semaine. La réduction de la dose ou la cessation est guidée par la réponse du patient et la surveillance hématologique. Le méthotrexate a également été administré deux fois par semaine dans des doses allant de 15 à 37,5 mg chez les patients qui ont mal répondu à un traitement hebdomadaire.
Psoriasis Rheumatoid Arthritis et Juvenile Rheumatoid Arthritis
Polyarthrite rhumatoïde adulte
Horaires de dosage de démarrage recommandé
- Doses orales uniques de 7,5 mg une fois par semaine.
- Dosages oraux divisés de 2,5 mg à des intervalles de 12 heures pour 3 doses données comme cours une fois par semaine
Polymatoïde juvénile de cours polyarticulaire
La dose de départ recommandée est de 10 mg / m² donnée une fois par semaine.
Pour les doses de PR adulte de RA ou de trame polyarticulaire peuvent être ajustées progressivement pour obtenir une réponse optimale. Une expérience limitée montre une augmentation significative de l'incidence et de la gravité des réactions toxiques graves, en particulier la suppression de la moelle osseuse à des doses supérieures à 20 mg / semaine chez les adultes. Bien qu'il existe une expérience avec des doses allant jusqu'à 30 mg / m² / semaine chez les enfants, il y a trop peu de données publiées pour évaluer comment les doses supérieures à 20 mg / m² / semaine pourraient affecter le risque de toxicité grave chez les enfants. L'expérience suggère cependant que les enfants recevant 20 à 30 mg / m² / semaine (0,65 à 1,0 mg / kg / semaine) peuvent avoir une meilleure absorption et moins d'effets secondaires gastro-intestinaux si le méthotrexate est administré par voie intramusculaire ou par voie sous-cutanée.
La réponse thérapeutique commence généralement dans les 3 à 6 semaines et le patient peut continuer à s'améliorer pendant encore 12 semaines ou plus.
La durée optimale du traitement est inconnue. Des données limitées disponibles à partir d'études à long terme chez les adultes indiquent que l'amélioration clinique initiale est maintenue pendant au moins deux ans avec une thérapie continue. Lorsque le méthotrexate est interrompu, l'arthrite s'aggrave généralement dans les 3 à 6 semaines.
Le patient doit être pleinement informé des risques impliqués et doit être sous la surveillance constante du médecin. (Voir Informations sur les patients .) Assessment of hematologic hepatic renal et pulmonary function should be made by history physical examination et laboratory tests before beginning periodically during et before reinstituting methotrexate therapy. (Voir PRÉCAUTIONS .) Appropriate steps should be taken to avoid conception during methotrexate therapy. (Voir PRÉCAUTIONS et Contre-indications .)
La thérapie hebdomadaire peut être instituée avec les comprimés de méthotrexate Rheumatrex® USP 2,5 mg de dose qui sont conçus pour fournir des doses sur une plage de 5 mg à 20 mg administrée en tant que dose hebdomadaire unique. Les packs de dose ne sont pas recommandés pour l'administration de méthotrexate à des doses hebdomadaires supérieures à 20 mg. Tous les horaires doivent être continuellement adaptés au patient individuel. Une dose de test initiale peut être donnée avant le calendrier de dosage régulier pour détecter toute sensibilité extrême aux effets indésirables. (Voir Effets indésirables .) Maximal myelosuppression usually occurs in seven to ten days.
Psoriasis : Horaires de dose de démarrage recommandés
- Horaire hebdomadaire de dose de messagerie instantanée orale unique ou iv : 10 à 25 mg par semaine jusqu'à ce que une réponse adéquate soit obtenue.
- Horaire de dose orale divisée : 2,5 mg à des intervalles de 12 heures pour trois doses.
Dosages in each schedule may be gradually adjusted to achieve optimal clinical response; 30 mg/week should not ordinarily be exceeded.
Une fois que la réponse clinique optimale a été obtenue, chaque programme de dosage doit être réduit à la quantité la plus faible possible de médicament et à la période de repos la plus longue possible.
L'utilisation du méthotrexate peut permettre le retour à la thérapie topique conventionnelle qui devrait être encouragée.
Manutention et élimination
Des procédures de manipulation et d'élimination appropriées des médicaments anticancéreuses doivent être prises en compte. Plusieurs lignes directrices sur ce sujet ont été publiées.1-5 Il n'y a aucun accord général que toutes les procédures recommandées dans les directives sont nécessaires ou appropriées.
Comment fourni
Oral
Description
Les comprimés de méthotrexate USP contiennent une quantité de méthotrexate de sodium équivalent à 2,5 mg de méthotrexate et sont des comprimés jaunes convexes ronds notés en deux sur un côté gravé avec m au-dessus du score et 1 en dessous.
Comprimés de méthotrexate rhumatrex® USP 2,5 mg de dose - (chaque comprimé équivalent à 2,5 mg de méthotrexate)
NDC 67253-580-42 - comprimés de méthotrexate Rheumatrex® Pack de dose USP - 4 cartes contenant chacune deux comprimés de 2,5 mg, soit 5 mg par semaine.
NDC 67253-580-43 - comprimés de méthotrexate Rheumatrex® Pack de dose USP - 4 cartes contenant chacune trois comprimés de 2,5 mg, soit 7,5 mg par semaine.
NDC 67253-580-44 - comprimés de méthotrexate Rheumatrex® Pack de dose USP - 4 cartes contenant chacune quatre comprimés de 2,5 mg, soit 10 mg par semaine.
NDC 67253-580-45 - comprimés de méthotrexate Rheumatrex® Pack de dose USP - 4 cartes contenant chacune cinq comprimés de 2,5 mg, soit 12,5 mg par semaine.
NDC 67253-580-46 - comprimés de méthotrexate Rheumatrex® Pack de dose USP - 4 cartes contenant chacune six comprimés de 2,5 mg, soit 15 mg par semaine.
NDC 67253-580-47 - comprimés de méthotrexate Rheumatrex® Pack de dose USP - 4 cartes contenant chacune sept comprimés de 2,5 mg, soit 17,5 mg par semaine.
NDC 67253-580-48 - comprimés de méthotrexate Rheumatrex® Pack de dose USP - 4 cartes contenant chacune huit comprimés de 2,5 mg, soit 20 mg par semaine.
Stocker à 20 ° -25 ° C (68 ° -77 ° F) [voir Température ambiante contrôlée par l'USP ]. Protéger de la lumière.
Références
1. Contrôle de l'exposition professionnelle aux médicaments dangereux (directives de pratique de l'OSHA). Am J Health Syst Pharm 1996: 53: 1669-1685.
2. Commission nationale de l'étude sur l'exposition cytotoxique - Recommandations pour gérer les agents cytotoxiques. Disponible auprès de Louis P. Jeffrey SC D Président de la Commission nationale de l'étude sur l'exposition cytotoxique Massachusetts College of Pharmacy and Allied Health Sciences 179 Longwood Avenue Boston Massachusetts 02115.
3. Clinical Oncological Society of Australia: Lignes directrices et recommandations pour la manipulation sûre des agents antinéoplasiques. Med J Australia 1983; 1: 426-428.
4. Jones RB et al. Manipulation sûre des agents chimiothérapeutiques: un rapport du Mount Sinai Medical Center. CA - Un Journal du cancer pour les cliniciens septembre / octobre 1983; 258-263.
5. Bulletin d'assistance technique de l'American Society of Hospital Pharmaciens sur la gestion des médicaments cytotoxiques et dangereux. Am J Hosp Pharm 1990; 47: 1033-1049.
Fabriqué pour: Dava Pharmaceuticals Inc. Fort Lee NJ 07024 USA. Par: Excella Gmbh Feucht Allemagne. Rev. 09/10
Effets secondaires for Rheumatrex
En général, l'incidence et la gravité des effets secondaires aigus sont liés à la dose et à la fréquence de l'administration. Les réactions les plus graves sont discutées ci-dessus sous la toxicité du système organique dans la section de précaution. Cette section doit également être consultée lorsque vous recherchez des informations sur les effets indésirables avec le méthotrexate.
Les réactions indésirables les plus fréquemment rapportées comprennent la stomatite ulcéreuse les nausées et la détresse abdominale. D'autres effets indésirables fréquemment signalés sont les frissons de fatigue indus du malaise et les étourdissements de la fièvre et la diminution de la résistance à l'infection. D'autres effets indésirables qui ont été signalés avec le méthotrexate sont répertoriés ci-dessous par le système d'organes. Dans le cadre d'oncologie, le traitement concomitant et la maladie sous-jacente rendent difficile l'attribution spécifique d'une réaction au méthotrexate.
Effets secondaires de Cozaar 50 mg
Système alimentaire: gingivite pharyngite stomatite anorexie nausée nausées vomissements diarrhée hématemèse melena ulcération gastro-intestinale et entérite pancréatite de saignement.
Troubles du système sanguin et lymphatique: hématopoïèse supprimée provoquant une anémie anémie aplasique pancytopénie leukopénie neutropénie et/or thrombocytopenia lymphadenopathy et lymphoproliferative disorders (including reversible). L'hypogammaglobulinémie a été signalée rarement.
Cardiovasculaire: Péricardite Hypotension de l'épanchement péricardique et événements thromboemboliques (y compris la thrombose artérielle thrombose cérébrale thrombose profonde thrombose de la veine rétinienne thrombophlébittis et embolie pulmonaire).
Système nerveux central: mal de têtes drowsiness blurred vision transient blindness speech impairment including dysarthria et aphasia hemiparesis paresis et convulsions have also occurred following administration of methotrexate. Following low doses there have been occasional reports of transient subtle cognitive dysfunction mood alteration unusual cranial sensations leukoencephalopathy or encephalopathy.
Hépatobiliaire: troubles hépatotoxicité hépatite aiguë fibrose chronique et cirrhose diminue dans les élévations de l'enzyme hépatique de l'albumine sérique.
Infection: Il y a eu des rapports de cas d'infections opportunistes parfois mortelles chez les patients recevant un traitement au méthotrexate pour les maladies néoplasiques et non néoplasiques. La pneumonie de pneumocystis carinii était l'infection opportuniste la plus courante. Il a également été signalé des infections à la pneumonie Sépless Nocardiose Histoplasmose Cryptococcose Herpès Zoster H. Hépatite simplex et disséminé H. simplex.
Système musculo-squelettique: fracture de contrainte.
Ophtalmique: Conjonctivite Changements visuels graves de l'étiologie inconnue.
Système pulmonaire: fibrose respiratoire insuffisance respiratoire pneumonite interstitielle; Des décès ont été signalés et une maladie pulmonaire obstructive interstitielle chronique s'est parfois produite.
Peau: Érythèmes éruptions éruptères Prurit Urticaire Photosensibilité Changement pigmentaire ALOPECICE Ecchymose Télangiectasie Acné Furunculose Erythème multiforme Nécrolyse épidermique toxique Stevens-Johnne Syndrome Nécrose cutanée Ulcérite cutanée et exfolition.
Système urogénital: néphropathie sévère ou insuffisance rénale azotémie cystite hématurie; Oogenèse défectueuse ou spermatogenèse Oligospermie transitoire Dysfonctionnement menstruel Décharge vaginale et gynécomastie; Infertilité avortement défaut fœtal.
D'autres réactions plus rares liées ou attribuées à l'utilisation du méthotrexate telles que la vascularite de la nodulose arthralgie / myalgie perte de libido / impuissance diabète ostéoporose morte de mort subite lymphomes réversibles syndrome de la lyse tumorale nécrose et ostéonécrose des tissus mous. Des réactions anaphylactoïdes ont été rapportées.
Réactions indésirables dans les études de polyarthrite rhumatoïde en double aveugle
Les incidences approximatives de méthotrexate attribuées (c.-à-d. Rate de placebo ont soustraité) les effets indésirables dans des études en double aveugle de 12 à 18 semaines sur les patients (n = 128) avec une polyarthrite rhumatoïde traitée avec une faible dose orale (7,5 à 15 mg / semaine) de méthotrexate de pouls sont répertoriées ci-dessous. Pratiquement tous ces patients étaient sous des médicaments anti-inflammatoires non stéroïdiens concomitants et certains prenaient également de faibles doses de corticostéroïdes. L'histologie hépatique n'a pas été examinée dans ces études à court terme. (Voir PRÉCAUTIONS .)
Incidence supérieure à 10%: La fonction hépatique élevée teste 15% de nausées / vomissements 10%.
Incidence 3% à 10%: Stomatite thrombocytopénie (nombre de plaquettes inférieur à 100000 / mm³).
Incidence 1% à 3%: Éruption cutanée / prurit / dermatite diarrhée alopécie leucopénie (WBC moins de 3000 / mm³) étourdissements de pancytopénie.
Deux autres essais contrôlés sur les patients (n = 680) atteints de polyarthrite rhumatoïde sur 7,5 mg - 15 mg / semaines oraux ont montré une incidence de pneumonite interstitielle de 1%. (Voir PRÉCAUTIONS .)
D'autres réactions moins courantes ont inclus une diminution des maux de tête hématocrite infection des respiratoires supérieures anorexie arthralgias douleur thoracique toussant l'inconfort de la dyurie oculaire de l'infection de la fièvre épistaxis transpirant des acouphènes et des débits vaginaux.
Réactions indésirables dans le psoriasis
Il n'y a pas d'essais récents contrôlés par placebo chez les patients atteints de psoriasis. Il existe deux rapports de littérature (Roenigk 1969 et Nyfors 1978) décrivant les grandes séries (n = 204 248) des patients atteints de psoriasis traités par du méthotrexate. Les dosages variaient jusqu'à 25 mg par semaine et le traitement a été administré jusqu'à quatre ans. À l'exception de la photosensibilité de l'alopécie et de la combustion des lésions cutanées (chacune de 3% à 10%), les taux de réaction indésirables dans ces rapports étaient très similaires à ceux des études de polyarthrite rhumatoïde. Des érosions de plaque rarement douloureuses peuvent apparaître.
Réactions indésirables dans les études JRA
Les incidences approximatives des effets indésirables rapportés chez les patients pédiatriques atteints de JRA traités avec des doses hebdomadaires orales de méthotrexate (5 à 20 mg / m² / semaine ou 0,1 à 0,65 mg / kg / semaine) étaient les suivantes (pratiquement tous 14%; réactions gastro-intestinales (par exemple, nausées vomissements diarrhée) 11%; stomatite 2%; leukopénie 2%; Maux de tête 1,2%; alopécie 0,5%; étourdissements 0,2%; et éruption cutanée 0,2%. Bien qu'il y ait une expérience avec l'administration jusqu'à 30 mg / m² / semaine dans JRA, les données publiées pour des doses supérieures à 20 mg / m² / semaine sont trop limitées pour fournir des estimations fiables des taux de réaction négative.
Interactions médicamenteuses for Rheumatrex
Il a été rapporté que l'administration concomitante de certains AINS présentant un traitement à forte dose de méthotrexate augmente et prolonge les taux sériques de méthotrexate entraînant des décès par toxicité hématologique et gastro-intestinale sévère.
La prudence doit être utilisée lorsque les AINS et les salicylates sont administrés en concomitance avec des doses plus faibles de méthotrexate. Ces médicaments réduisent la sécrétion tubulaire de méthotrexate dans un modèle animal et peuvent améliorer sa toxicité.
Malgré les interactions potentielles, les études du méthotrexate chez les patients atteints de polyarthrite rhumatoïde ont généralement inclus une utilisation simultanée de schémas posologiques constants des AINS sans problèmes apparents. Il faut cependant apprécier que les doses utilisées dans la polyarthrite rhumatoïde (7,5 à 20 mg / semaine) sont quelque peu inférieures à celles utilisées dans le psoriasis et que des doses plus importantes pourraient entraîner une toxicité inattendue.
Le méthotrexate est partiellement lié à l'albumine sérique et la toxicité peut être augmentée en raison du déplacement par certains médicaments tels que le salicylate phénylbutazone phénytoïne et les sulfonamides. Le transport tubulaire rénal est également diminué par le probénécide; L'utilisation de méthotrexate avec ce médicament doit être soigneusement surveillée.
Oral antibiotics such as tetracycline chloramphenicol et nonabsorbable broad spectrum antibiotics may decrease intestinal absorption of methotrexate or interfere with the enterohepatic circulation by inhibiting bowel flora et suppressing metabolism of the drug by bacteria.
Les pénicillines peuvent réduire la clairance rénale du méthotrexate; Une augmentation des concentrations sériques de méthotrexate avec une toxicité hématologique et gastro-intestinale concomitante a été observée avec du méthotrexate. L'utilisation de méthotrexate avec des pénicillines doit être soigneusement surveillée.
Le potentiel d'augmentation de l'hépatotoxicité lorsque le méthotrexate est administré avec d'autres agents hépatotoxiques n'a pas été évalué. Cependant, l'hépatotoxicité a été signalée dans de tels cas. Par conséquent, les patients recevant une thérapie concomitante avec le méthotrexate et d'autres hépatotoxines potentielles (par exemple, les rétinoïdes azathioprine rétinoïdes sulfasalazine) devraient être étroitement surveillés pour un éventuel risque accru d'hépatotoxicité.
Le méthotrexate peut diminuer la clairance de la théophylline; Les niveaux de théophylline doivent être surveillés lorsqu'ils sont utilisés simultanément avec le méthotrexate.
Certains effets secondaires tels que les plaies buccales peuvent être réduits par la supplémentation en folate par du méthotrexate.
Il a été signalé que le triméthoprime / sulfa-méthoxazole a rarement augmenté la suppression de la moelle osseuse chez les patients recevant du méthotrexate probablement par un effet antifolate additif.
Avertissements pour rhumatrex
Voir Avertissements en boîte .
Les formulations et les diluants de méthotrexate contenant des conservateurs ne doivent pas être utilisés pour le traitement par méthotrexate intrathécal ou à forte dose.
Précautions pour rhumatrex
Général
Le méthotrexate a le potentiel d'une toxicité grave. (Voir Avertissements en boîte .) Toxic effects may be related in frequency et severity to dose or frequency of administration but have been seen at all doses. Because they can occur at any time during therapy it is necessary to follow patients on methotrexate closely. Most adverse reactions are reversible if detected early. When such reactions do occur the drug should be reduced in dosage or discontinued et appropriate corrective measures should be taken. If necessary this could include the use of leucovorin calcium et/or acute intermittent hemodialysis with a high-flux dialyzer. (Voir Sur-ladosage .) If methotrexate therapy is reinstituted it should be carried out with caution with adequate consideration of further need for the drug et with increased alertness as to possible recurrence of toxicity.
La pharmacologie clinique du méthotrexate n'a pas été bien étudiée chez les personnes âgées. En raison de la diminution de la fonction hépatique et rénale ainsi qu'une diminution des réserves de folate dans cette population, des doses relativement faibles doivent être prises en compte et ces patients doivent être étroitement surveillés pour les premiers signes de toxicité.
Tests de laboratoire
Les patients subissant un traitement au méthotrexate doivent être étroitement surveillés afin que les effets toxiques soient détectés rapidement. L'évaluation de base devrait inclure un Nombre de sang complet avec des essais de fonctions de fonction rénale et des plaquettes différentiels et des plaquettes et une radiographie pulmonaire. Pendant la thérapie de la polyarthrite rhumatoïde et la surveillance du psoriasis de ces paramètres est recommandée: l'hématologie au moins la fonction rénale mensuelle et la fonction hépatique tous les 1 à 2 mois. Une surveillance plus fréquente est généralement indiquée pendant le traitement antinéoplasique. Au cours des doses initiales ou changeantes ou pendant les périodes de risque accru de taux sanguin élevé de méthotrexate (par exemple, une déshydratation), une surveillance plus fréquente peut également être indiquée.
Des anomalies de test de la fonction hépatique transitoire sont observées fréquemment après l'administration de méthotrexate et ne sont généralement pas provoquées de modification du traitement au méthotrexate. Les anomalies de test de la fonction hépatique persistante et / ou la dépression de l'albumine sérique peuvent être des indicateurs d'une toxicité grave du foie et nécessitent une évaluation. (Voir PRÉCAUTIONS Toxicité du système d'organes Hépatique .)
Une relation entre les tests de fonction hépatique anormaux et la fibrose ou la cirrhose du foie n'a pas été établie pour les patients atteints de psoriasis. Des anomalies persistantes dans les tests de la fonction hépatique peuvent précéder l'apparition de la fibrose ou de la cirrhose dans la population de polyarthrite rhumatoïde.
Les tests de fonction pulmonaire peuvent être utiles si une maladie pulmonaire induite par le méthotrexate est suspectée, surtout si des mesures de base sont disponibles.
Mutagenèse de la carcinogenèse et altération de la fertilité
Aucune donnée humaine contrôlée n'existe sur le risque de néoplasie avec le méthotrexate. Le méthotrexate a été évalué dans un certain nombre d'études animales pour le potentiel cancérigène avec des résultats non concluants. Bien qu'il existe des preuves que le méthotrexate provoque des dommages chromosomiques aux cellules somatiques animales et aux cellules de la moelle osseuse humaine, la signification clinique reste incertaine. Le lymphome non hodgkinien et d'autres tumeurs ont été signalés chez les patients recevant du méthotrexate oral à faible dose. Cependant, il y a eu des cas de lymphome malin survenant pendant le traitement avec du méthotrexate oral à faible dose qui ont régressé complètement après le retrait du méthotrexate sans nécessiter un traitement anti-lymphome actif. Les avantages doivent être pesés avec les risques potentiels avant d'utiliser le méthotrexate seul ou en combinaison avec d'autres médicaments, en particulier chez les patients pédiatriques ou les jeunes adultes. Le méthotrexate provoque un avortement d'embryotoxicité et des défauts fœtaux chez l'homme. Il a également été signalé qu'il provoque une altération de l'oligospermie de fertilité et du dysfonctionnement menstruel chez l'homme pendant et pendant une courte période après l'arrêt du traitement.
Grossesse
Psoriasis et rheumatoid arthrite: Methotrexate is in Grossesse Category X. Voir Contre-indications .
Mères qui allaitent
Voir Contre-indications .
Usage pédiatrique
La sécurité et l'efficacité chez les patients pédiatriques n'ont été établies que dans la chimiothérapie du cancer et dans la polyarthrite rhumatoïde juvénile à cours polyarticulaire.
Des études cliniques publiées évaluant l'utilisation du méthotrexate chez les enfants et les adolescents (c.-à-d. Les patients âgés de 2 à 16 ans) avec JRA ont démontré une sécurité comparable à celle observée chez les adultes atteints de polyarthrite rhumatoïde. (Voir Pharmacologie clinique Effets indésirables et Posologie et administration .)
Utilisation gériatrique
Les études cliniques du méthotrexate n'ont pas inclus un nombre suffisant de sujets âgés de 65 ans et plus pour déterminer s'ils réagissent différemment des sujets plus jeunes. En général, la sélection de la dose pour un patient âgé doit être prudente reflétant la plus grande fréquence de diminution de la fonction hépatique et rénale des réserves de folate de la maladie concomitante ou une autre thérapie médicamenteuse (c'est-à-dire qui interfère avec la fonction rénale du méthotrexate ou du métabolisme du folate) dans cette population (voir (voir PRÉCAUTIONS: Interactions médicamenteuses ). Étant donné que le déclin de la fonction rénale peut être associé à une augmentation des événements indésirables et que les mesures sériques de la créatinine peuvent être excessives sur la fonction rénale chez les méthodes plus précises (c'est-à-dire la clairance de la créatine). Les taux sériques de méthotrexate peuvent également être utiles. Les patients âgés doivent être étroitement surveillés pour les premiers signes de moelle hépatique et de toxicité rénale. Dans les situations d'utilisation chronique, certaines toxicités peuvent être réduites par la supplémentation en folate. L'expérience post-marketing suggère que la survenue de la thrombocytopénie et de la pneumonite de la moelle osseuse peut augmenter avec l'âge. Voir Avertissements en boîte et Effets indésirables .
Toxicité du système d'organes
Gastro-intestinal
Si des vomissements de diarrhée ou de stomatite se produisent, ce qui peut entraîner une déshydratation que le méthotrexate doit être interrompu jusqu'à ce que la récupération se produise. Le méthotrexate doit être utilisé avec une extrême prudence en présence d'une maladie de l'ulcère gastro-duodénologique ou d'une colite ulcéreuse.
Hématologique
Le méthotrexate peut supprimer l'hématopoïèse et provoquer une anémie anémie aplasique pancytopénie leukopénie neutropénie et / ou thrombocytopénie. Chez les patients atteints de tumeurs malignes et de troubles hématopoïétiques préexistants, le médicament doit être utilisé avec prudence le cas échéant. Dans des essais cliniques contrôlés dans la polyarthrite rhumatoïde (n = 128) leucopénie (WBC <3000/mm³) was seen in 2 patients thrombocytopenia (platelets < 100000/mm³) in 6 patients et pancytopenia in 2 patients.
Dans le psoriasis et la polyarthrite rhumatoïde, le méthotrexate doit être arrêté immédiatement en cas de baisse significative de la numération sanguine. Dans le traitement des maladies néoplasiques, le méthotrexate ne doit être poursuivi que si le bénéfice potentiel justifie le risque de myélosuppression sévère. Les patients atteints de granulocytopénie et de fièvre profonds doivent être évalués immédiatement et nécessitent généralement des antibiotiques parentéraux à large spectre.
À quelle fréquence pouvez-vous prendre la Cambie
Hépatique
Le méthotrexate a le potentiel d'hépatotoxicité aiguë (transaminases élevées) et chronique (fibrose et cirrhose). La toxicité chronique est potentiellement mortelle; Il s'est généralement produit après une utilisation prolongée (généralement deux ans ou plus) et après une dose totale d'au moins 1,5 gramme. Dans les études sur les patients psoriasiques, l'hépatotoxicité semblait être fonction de la dose cumulative totale et semblait être améliorée par l'alcoolisme obésité diabète et âge avancé. Un taux d'incidence précis n'a pas été déterminé; Le taux de progression et de réversibilité des lésions n'est pas connu. Une prudence spéciale est indiquée en présence de lésions hépatiques préexistantes ou de fonction hépatique altérée.
Dans la fonction hépatique du psoriasis, les tests, y compris l'albumine sérique, doivent être effectués périodiquement avant le dosage, mais sont souvent normaux face au développement de la fibrose ou de la cirrhose. Ces lésions ne peuvent être détectables que par biopsie. La recommandation habituelle est d'obtenir une biopsie hépatique à 1) la pré-parhérapie ou peu de temps après le début de la thérapie (2 à 4 mois) 2) une dose cumulative totale de 1,5 gramme et 3) après chaque 1,0 à 1,5 gramme supplémentaire. La fibrose modérée ou toute cirrhose entraîne normalement l'arrêt du médicament; La fibrose légère suggère normalement une biopsie répétée en 6 mois. Les résultats histologiques plus légers tels que le changement gras et l'inflammation du portail à faible teneur sont une pré-séthhérapie relativement courante. Bien que ces changements légers ne soient généralement pas une raison pour éviter ou interrompre la thérapie de méthotrexate, le médicament doit être utilisé avec prudence.
Dans l'âge de la polyarthrite rhumatoïde, l'utilisation du méthotrexate et la durée du traitement ont été signalées comme facteurs de risque d'hépatotoxicité; D'autres facteurs de risque similaires à ceux observés dans le psoriasis peuvent être présents dans la polyarthrite rhumatoïde mais n'ont pas été confirmés à ce jour. Des anomalies persistantes dans les tests de la fonction hépatique peuvent précéder l'apparition de la fibrose ou de la cirrhose dans cette population. Il existe une expérience combinée signalée chez 217 patients atteints de polyarthrite rhumatoïde avec des biopsies hépatiques avant et pendant le traitement (après une dose cumulée d'au moins 1,5 g) et chez 714 patients atteints d'une biopsie uniquement pendant le traitement. Il y a 64 (7%) cas de fibrose et 1 (0,1%) cas de cirrhose. Sur les 64 cas de fibrose, 60 ont été jugés légers. La coloration à la réticuline est plus sensible pour la fibrose précoce et son utilisation peut augmenter ces chiffres. On ne sait pas si une utilisation encore plus longue augmentera ces risques.
Des tests de fonction hépatique doivent être effectués au départ et à des intervalles de 4 à 8 semaines chez les patients recevant du méthotrexate pour la polyarthrite rhumatoïde. Une biopsie hépatique de prétraitement doit être réalisée pour les patients ayant des antécédents de consommation excessive d'alcool, des valeurs de test de la fonction hépatique de base de base ou une infection chronique de la fonction hépatique ou une infection chronique. Pendant la thérapie, la biopsie hépatique doit être effectuée s'il y a des anomalies de test de fonction hépatique persistante ou s'il y a une diminution de l'albumine sérique en dessous de la plage normale (dans le cadre d'une polyarthrite rhumatoïde bien contrôlée).
Si les résultats d'une biopsie hépatique montrent des changements légers (Roenigk grades I IIIIA), le méthotrexate peut être poursuivi et le patient surveillé conformément aux recommandations énumérées ci-dessus. Le méthotrexate doit être interrompu chez tout patient qui affiche des tests de fonction hépatique constamment anormaux et refuse la biopsie hépatique ou chez tout patient dont la biopsie hépatique montre des changements modérés à graves (Roenigk grade IIIB ou IV).
Infection ou états immunologiques
Le méthotrexate doit être utilisé avec une extrême prudence en présence d'une infection active et est généralement contre-indiqué chez les patients présentant des preuves manifestes ou de laboratoire de syndromes d'immunodéficience. L'immunisation peut être inefficace lorsqu'elle est donnée pendant le traitement au méthotrexate. L'immunisation avec des vaccins à virus vivant n'est généralement pas recommandée. Il y a eu des rapports d'infections disséminées par la vaccina après une immunisation de la variole chez les patients recevant un traitement par méthotrexate.
L'hypogammaglobulinémie a été signalée rarement.
Les infections opportunistes potentiellement mortelles, en particulier la pneumonie de Pneumocystis carinii, peuvent survenir avec un traitement par méthotrexate. Lorsqu'un patient présente des symptômes pulmonaires, la possibilité d'une pneumonie de pneumocystis carinii doit être envisagée.
Pulmonaire
Pulmonaire symptoms (especially a dry nonproductive cough) or a nonspecific pneumonitis occurring during methotrexate therapy may be indicative of a potentially dangerous lesion et require interruption of treatment et careful investigation. Although clinically variable the typical patient with methotrexate induced lung disease presents with fever cough dyspnea hypoxemia et an infiltrate on chest Xray; infection (including pneumonia) needs to be excluded. This lesion can occur at all dosages.
Rénal
Le méthotrexate peut causer des dommages rénaux qui peuvent entraîner insuffisance rénale aiguë . La néphrotoxicité est principalement due à la précipitation du méthotrexate et du 7-hydroxyméthotrexate dans les tubules rénaux. Une attention particulière à la fonction rénale, notamment une alcalinisation d'urine hydratation adéquate, et la mesure du méthotrexate sérique et des niveaux de créatinine sont essentielles pour une administration sûre.
Peau
Des réactions dermatologiques sévères parfois mortelles, notamment la nécrolyse épidermique toxique, le syndrome exfoliative de la dermatite exfoliative et l'érythème multiforme ont été signalés chez les enfants et les adultes à quelques jours suivant l'administration par voie intraveineuse ou intrathécale intrathécale intramusculaire orale. Des réactions ont été notées après des doses intermédiaires ou élevées à faible ou multiple de méthotrexate chez les patients atteints de maladies néoplasiques et non néoplasiques.
Autres précautions
Le méthotrexate doit être utilisé avec une extrême prudence en présence de la débilité.
Le méthotrexate sort lentement à partir des compartiments d'espace troisième (par exemple, épanchements pleuraux ou ascite). Il en résulte une demi-vie de plasma terminal prolongé et une toxicité inattendue. Chez les patients présentant des accumulations d'espace importantes, il est conseillé d'évacuer le liquide avant le traitement et de surveiller les taux plasmatiques de méthotrexate.
Les lésions du psoriasis peuvent être aggravées par une exposition concomitante au rayonnement ultraviolet. La dermatite de radiation et les coups de soleil peuvent être rappelés par l'utilisation de méthotrexate.
Surdosage Information for Rheumatrex
La leucovorine est indiquée pour diminuer la toxicité et contrecarrer l'effet des sur-doseurs administrés par inadvertance du méthotrexate. L'administration de leucovorine devrait commencer aussi rapidement que possible. À mesure que l'intervalle de temps entre l'administration de méthotrexate et l'initiation de la leucovorine augmente l'efficacité de la leucovorine dans la contre-toxicité diminue. La surveillance de la concentration sérique de méthotrexate est essentielle pour déterminer la dose optimale et la durée du traitement par la leucovorine.
En cas de surdosage massif, l'hydratation et l'alcalinisation urinaire peuvent être nécessaires pour empêcher la précipitation du méthotrexate et / ou de ses métabolites dans les tubules rénaux. De manière générale, ni l'hémodialyse ni la dialyse péritonéale ne sont démontrées pour améliorer l'élimination du méthotrexate. Cependant, une clairance efficace du méthotrexate a été signalée avec une hémodialyse intermittente aiguë en utilisant un dialyseur à flux élevé (Wall SM et al: Am J Kidney Dis 28 (6): 846-854 1996).
Dans l'expérience post-commercialisation, une surdose avec du méthotrexate s'est généralement produite avec l'administration orale et intrathécale, bien que une surdose intraveineuse et intramusculaire ait également été signalée.
Les rapports de surdose buccale indiquent souvent une administration quotidienne accidentelle au lieu d'une semaine (doses uniques ou divisées). Les symptômes couramment rapportés après une surdose orale comprennent les symptômes et les signes rapportés à des doses pharmacologiques, en particulier la réaction hématologique et gastro-intestinale. Par exemple, la leucopénie thrombocytopénie anémie pancytopénie de la moelle osseuse suppression mucosite stomatite ulcération orale nausée nausées vomissements gastro-intestinaux saignement gastro-intestinal. Dans certains cas, aucun symptôme n'a été signalé. Il y a eu des rapports de décès après une surdose. Dans ces cas, des événements tels que la septicémie ou l'insuffisance rénale du choc septique et l'anémie aplasique ont également été signalés.
Contre-indications for Rheumatrex
Le méthotrexate peut provoquer une mort fœtale ou des effets tératogènes lorsqu'il est administré à une femme enceinte. Le méthotrexate est contre-indiqué chez les femmes enceintes atteints de psoriasis ou de polyarthrite rhumatoïde et ne doit être utilisée dans le traitement des maladies néoplasiques que lorsque le bénéfice potentiel l'emporte sur le risque pour le fœtus. Les femmes en potentiel de procréation ne doivent pas être démarrées sur le méthotrexate tant que la grossesse n'est exclue et doit être pleinement conseillé du risque grave pour le fœtus (voir PRÉCAUTIONS ) devraient devenir enceintes pendant leur traitement. La grossesse doit être évitée si l'un des partenaires reçoit du méthotrexate; pendant et pendant un minimum de trois mois après le traitement pour les patients masculins et pendant et pendant au moins un cycle ovulatoire après traitement pour les patientes. (Voir Avertissements en boîte .)
En raison du potentiel de réactions indésirables graves du méthotrexate chez les nourrissons alimentés par le sein, il est contre-indiqué chez les mères infirmières.
Les patients atteints de psoriasis ou de polyarthrite rhumatoïde atteints d'une maladie hépatique alcoolique de l'alcoolisme ou d'une autre maladie hépatique chronique ne devraient pas recevoir de méthotrexate.
Les patients atteints de psoriasis ou de polyarthrite rhumatoïde qui ont des preuves manifestes ou de laboratoire de syndromes d'immunodéficience ne devraient pas recevoir de méthotrexate.
Les patients atteints de psoriasis ou de polyarthrite rhumatoïde qui ont des dyscrasies sanguins préexistants tels que l'hypoplasie de la moelle osseuse thrombocytopénie ou une anémie significative ne devraient pas recevoir de méthotrexate.
Les patients présentant une hypersensibilité connue au méthotrexate ne devraient pas recevoir le médicament.
Pharmacologie clinique for Rheumatrex
Le méthotrexate inhibe l'acide dihydrofolique réductase. Les dihydrofolates doivent être réduits à des tétrahydrofolates par cette enzyme avant de pouvoir être utilisés comme porteurs de groupes à un carbone dans la synthèse des nucléotides purines et du thymidylate. Par conséquent, le méthotrexate interfère avec la réparation de la synthèse de l'ADN et la réplication cellulaire. Les tissus activement proliférants tels que les cellules malignes des cellules fœtales de la moelle osseuse des cellules buccales et intestinales et les cellules de la vessie urinaire sont en général plus sensibles à cet effet du méthotrexate. Lorsque la prolifération cellulaire dans les tissus malins est supérieure à celle de la plupart des tissus normaux, le méthotrexate peut altérer la croissance maligne sans dommages irréversibles aux tissus normaux.
Le mécanisme d'action dans la polyarthrite rhumatoïde est inconnu; Cela peut affecter la fonction immunitaire. Deux rapports décrivent in vitro L'inhibition du méthotrexate de l'absorption des précurseurs de l'ADN par des cellules mononucléaires stimulées et une autre décrit dans la correction partielle de la polyarthrite animale par le méthotrexate de l'hyporesponivité des cellules de la rate et a supprimé la production d'IL 2. D'autres laboratoires n'ont cependant pas pu démontrer des effets similaires. La clarification de l'effet du méthotrexate sur l'activité immunitaire et sa relation avec l'immunopathogenèse rhumatoïde attendent d'autres études.
Chez les patients atteints de polyarthrite rhumatoïde, les effets du méthotrexate sur l'enflure articulaire et la sensibilité peuvent être observés dès 3 à 6 semaines. Bien que le méthotrexate améliore clairement les symptômes de l'inflammation (raideur de gonflement de la douleur), il n'y a aucune preuve qu'il induit une rémission de la polyarthrite rhumatoïde et un effet bénéfique a été démontré sur les érosions osseuses et d'autres changements radiologiques qui entraînent une altération de l'incapacité et de la déformation fonctionnel de l'utilisation articulaire.
La plupart des études sur le méthotrexate chez les patients atteints de polyarthrite rhumatoïde sont relativement à court terme (3 à 6 mois). Des données limitées d'études à long terme indiquent qu'une amélioration clinique initiale est maintenue pendant au moins deux ans avec une thérapie continue.
Dans le psoriasis, le taux de production de cellules épithéliales dans la peau est considérablement augmentée sur la peau normale. Ce différentiel dans les taux de prolifération est la base de l'utilisation du méthotrexate pour contrôler le processus psoriasique.
Dans un essai contrôlé par un placebo en double aveugle de 6 mois de 127 patients pédiatriques atteints de polyarthrite rhumatoïde juvénile (JRA) (âge moyen de 10,1 ans; tranche d'âge de 2,5 à 18 ans Durée moyenne de la maladie 5,1 ans) sur des antécédents anti-inflammatoires non stéroïdiens (NSIDSIDS) et / ou de méthotrexate de pré-prédisone étant donné une semaine à un DSIDS oral) et / ou de la pré-principale du méthotrexate étant donné une semaine à un DOSE Oral L'amélioration par rapport au placebo mesurée soit par l'évaluation globale du médecin, soit par un composite patient (réduction de 25% du score de sévérité articulaire, plus l'amélioration des évaluations globales des parents et des médecins de l'activité de la maladie.) Plus des deux tiers des patients de cet essai ont été traités par un sous-groupe polyarticulaire JRA et la plus grande réponse numérique. L'écrasante majorité des patients restants avaient un JRA à cours systémique. Tous les patients ne répondaient pas aux AINS; Environ l'on utilisait des corticostéroïdes à faible dose. Le méthotrexate hebdomadaire à une dose de 5 mg / m² n'était pas significativement plus efficace que le placebo dans cet essai.
Pharmacocinétique
Absorption
Chez l'adulte, l'absorption orale semble être dépendante de la dose. Les taux sériques maximaux sont atteints en une à deux heures. À des doses de 30 mg / m² ou moins de méthotrexate est généralement bien absorbée avec une biodisponibilité moyenne d'environ 60%. L'absorption de doses supérieure à 80 mg / m² est nettement moins possible d'un effet de saturation.
Chez les patients pédiatriques leucémiques, l'absorption orale du méthotrexate semble également dépendante de la dose et aurait varié considérablement (23% à 95%). Une différence de vingt fois entre les niveaux de pic les plus élevés et les plus bas (CMAX: 0,11 à 2,3 micromolaires après une dose de 20 mg / m²) a été signalé. Une variabilité interindividuelle significative a également été notée dans le temps de la concentration de pointe (TMAX: 0,67 à 4 heures après une dose de 15 mg / m²) et la fraction de dose absorbée. L'absorption de doses supérieure à 40 mg / m² a été significativement inférieure à celle des doses plus faibles. Il a été démontré que la nourriture retarde l'absorption et réduit la concentration maximale. Le méthotrexate est généralement complètement absorbé par les routes parentérales de l'injection. Après l'injection intramusculaire, les concentrations sériques de picment se produisent en 30 à 60 minutes. Comme chez les patients pédiatriques leucémiques, une large variabilité interindividuelle des concentrations plasmatiques de méthotrexate a été rapportée chez les patients pédiatriques atteints de JRA. Après l'administration orale de méthotrexate à des doses de 6,4 à 11,2 mg / m² / semaine chez les patients pédiatriques avec des concentrations sériques moyennes de JRA était de 0,59 micromolaire (plage de 0,03 à 1,40) à 1 heure 0,44 micromolaire (plage 0,01 à 1,00) à 2 heures et 0,29 micromolaire (plage 0,06 à 0,58) à 3 heures. Chez les patients pédiatriques recevant du méthotrexate pour une leucémie lymphocytaire aiguë (6,3 à 30 mg / m²) ou pour JRA (3,75 à 26,2 mg / m²), la demi-vie terminale aurait varie de 0,7 à 5,8 heures ou 0,9 à 2,3 heures respectivement.
Distribution
Après administration intraveineuse, le volume initial de distribution est d'environ 0,18 L / kg (18% du poids corporel) et le volume de distribution à l'état d'équilibre est d'environ 0,4 à 0,8 L / kg (40% à 80% du poids corporel). Le méthotrexate est en concurrence avec des folates réduits pour le transport actif à travers les membranes cellulaires au moyen d'un seul processus de transport actif médié par le transporteur. Aux concentrations sériques supérieures à 100 micromolaires, la diffusion passive devient une voie majeure par laquelle des concentrations intracellulaires efficaces peuvent être obtenues. Le méthotrexate dans le sérum est à environ 50% lié aux protéines. Les études de laboratoire démontrent qu'il peut être déplacé de l'albumine plasmatique par divers composés, notamment des sulfonamides salicylates tétracyclines chloramphénicol et de la phénytoïne.
Le méthotrexate ne pénètre pas dans la barrière du liquide sanguin dans les quantités thérapeutiques lorsqu'elle est administrée par voie orale ou parentérale. Des concentrations élevées de LCR du médicament peuvent être atteintes par l'administration intrathécale.
Chez les chiens, les concentrations de liquide synovial après le dosage oral étaient plus élevées dans les articulations non inflammées. Bien que les salicylates n'étaient pas interférés avec cette pénétration avant le traitement de la prednisone réduit la pénétration dans les articulations enflammées au niveau des articulations normales.
Métabolisme
Après l'absorption, le méthotrexate subit un métabolisme hépatique et intracellulaire en formes polyglutamées qui peuvent être converties en méthotrexate par des enzymes hydrolases. Ces polyglutamates agissent comme des inhibiteurs de la dihydrofolate réductase et de la thymidylate synthétase. De petites quantités de polyglutamates de méthotrexate peuvent rester dans les tissus pendant de longues périodes. La rétention et l'action médicamenteuse prolongée de ces métabolites actifs varient selon les différents tissus et tumeurs. Une petite quantité de métabolisme au 7-hydroxyméthotréxate peut se produire à des doses couramment prescrites. L'accumulation de ce métabolite peut devenir significative aux doses élevées utilisées dans le sarcome ostéogénique. La solubilité aqueuse du 7-hydroxyméthotexate est de 3 à 5 fois plus bas que le composé parent. Le méthotrexate est partiellement métabolisé par la flore intestinale après l'administration orale.
Demi-vie
La demi-vie terminale signalée pour le méthotrexate est d'environ trois à dix heures pour les patients recevant un traitement pour le psoriasis ou la polyarthrite rhumatoïde ou un traitement antinéoplasique à faible dose (moins de 30 mg / m²). Pour les patients recevant des doses élevées de méthotrexate, la demi-vie terminale est de huit à 15 heures.
Quel type de pilule est G3721
Excrétion
Rénal excretion is the primary route of elimination et is dependent upon dosage et route of administration. With IV administration 80% to 90% of the administered dose is excreted unchanged in the urine within 24 hours. There is limited biliary excretion amounting to 10% or less of the administered dose. Enterohepatic recirculation of methotrexate has been proposed.
Rénal excretion occurs by glomerular filtration et active tubular secretion. Nonlinear elimination due to saturation of renal tubular reabsorption has been observed in psoriatic patients at doses between 7.5 et 30 mg. Impaired renal function as well as concurrent use of drugs such as weak organic acids that also undergo tubular secretion can markedly increase methotrexate serum levels. Excellent correlation has been reported between methotrexate clearance et endogenous creatinine clearance.
Les taux de dégagement de méthotrexate varient considérablement et sont généralement diminués à des doses plus élevées. La clairance du médicament retardée a été identifiée comme l'un des principaux facteurs responsables de la toxicité du méthotrexate. Il a été postulé que la toxicité du méthotrexate pour les tissus normaux dépend davantage de la durée de l'exposition au médicament plutôt que du niveau de pointe atteint. Lorsqu'un patient a retardé l'élimination du médicament en raison de la fonction rénale compromise, une troisième épanchement de l'espace ou d'autres provoques les concentrations sériques de méthotrexate peuvent rester élevées pendant des périodes prolongées.
Le potentiel de toxicité des régimes à forte dose ou de l'excrétion retardée est réduit par l'administration de calcium de leucovorine pendant la phase finale de l'élimination du plasma de méthotrexate. La surveillance pharmacocinétique des concentrations sériques de méthotrexate peut aider à identifier les patients à haut risque de toxicité du méthotrexate et à aider à un ajustement approprié du dosage de la leucovorine. Les lignes directrices de surveillance des taux sériques de méthotrexate et d'ajustement du dosage de la leucovorine pour réduire le risque de toxicité de méthotrexate sont fournis ci-dessous en dose et en administration.
Le méthotrexate a été détecté dans le lait maternel humain. Le rapport de concentration maternel / plasma le plus élevé atteint était de 0,08: 1.
Informations sur les patients pour rhumatrex
Les patients doivent être informés des premiers signes et symptômes de toxicité de la nécessité de voir leur médecin rapidement s'ils se produisent et de la nécessité d'un suivi étroit, y compris des tests de laboratoire périodiques pour surveiller la toxicité.
Le médecin et le pharmacien devraient souligner au patient que la dose recommandée est prise chaque semaine dans la polyarthrite rhumatoïde et le psoriasis et que l'utilisation quotidienne erronée de la dose recommandée a conduit à une toxicité mortelle. Les patients doivent être encouragés à lire la feuille d'instructions du patient dans le pack de dose. Les prescriptions ne doivent pas être écrites ou remplies sur une base de PRN.
Les patients doivent être informés de l'avantage et du risque potentiels dans l'utilisation du méthotrexate. Le risque d'effets sur la reproduction doit être discuté avec des patients masculins et féminins prenant du méthotrexate.